Туберозный склероз
Туберо́зный склеро́з (ТС, болезнь Бурневилля — Прингла) — наследственное заболевание, характеризующееся образованием множественных доброкачественных опухолей (гамартом) в различных органах и системах. По мере прогрессирования заболевания эти опухоли увеличиваются в размерах, что приводит к нарушению работы поражённых органов и в некоторых случаях может иметь жизнеугрожающие последствия[3][4].
Что важно знать
История
История изучения туберозного склероза (ТС) началась в 1862—1863 годах, когда немецкий патологоанатом Фридрих Даниэль фон Реклингхаузен впервые описал множественные опухоли сердца и патологические изменения в головном мозге при вскрытии умершего младенца. Значительный вклад в изучение ТС внёс французский невролог Дезире-Маглуар Бурневиль, который в 1880 году подробно охарактеризовал неврологические симптомы и структурные изменения мозга у девочки с эпилептическими приступами, умственной отсталостью и кожными проявлениями. Дальнейшее развитие понимания болезни связано с британским дерматологом Джоном Джеймсом Принглом, который в 1890 году впервые описал характерные кожные изменения на лице пациентов, назвав их «врождённая аденома сальных желёз». Именно благодаря работам этих учёных заболевание получило название «болезнь Бурневилля — Прингла»[3].
Позднее исследователи обратили внимание на системный характер поражений при ТС. В 1908 году Фогт выделил классическую триаду симптомов: аденомы сальных желёз, эпилептические припадки и умственная отсталость. Дополнил клиническую картину офтальмолог Ян ван дер Хёвен, который в 1920 году описал патогномоничные изменения на глазном дне — симптом «тутовой ягоды» (факому) и предложил термин «факоматоз» для обозначения этой группы заболеваний[3].
Классификация
Этиология
ТС представляет собой аутосомно-доминантное заболевание с генетической гетерогенностью, характеризующееся неполной пенетрантностью и вариабельной экспрессивностью. Примерно в 68 % случаев болезнь возникает вследствие спонтанных (de novo) мутаций, что особенно характерно для рано дебютирующих форм. В основе развития заболевания лежит мутация в гене TSC[4].
На основании типа мутации выделют:
- ТС 1-го типа (около 10—30 % случаев) связан с мутациями гена TSC1, расположенного в локусе 9q34. Этот ген кодирует белок гамартин;
- ТС 2-го типа (большинство случаев) обусловлен мутациями гена TSC2, расположенного в локусе 16p13. Этот ген кодирует туберин.
Несмотря на высокую пенетрантность, заболевание проявляется с разной степенью тяжести даже среди родственников с одинаковой мутацией, что отражает его вариабельную экспрессивность[4].
Патогенез
Комплекс TSC1/TSC2 играет ключевую роль в процессе кортикального развития и контроле роста клеток. На различных этапах формирования центральной нервной системы, включая морфогенез, клеточную адгезию и миграцию, критически важна точная регуляция взаимодействия туберина и гамартина. Мутации в любом из этих генов нарушают развитие предшественников нейронов в период между 7-й и 20-й неделями гестации, что приводит к следующим последствиям[5]:
- нарушение клеточного деления;
- аномальная дифференцировка клеток;
- дисрегуляция контроля их размера;
- нарушение клеточной миграции.
В норме гамартин и туберин функционируют как единый комплекс, подавляя фосфатидилинозитол-3-киназный (PI3K) инсулин-активируемый сигнальный путь, включающий мишень рапамицина у млекопитающих (mTOR) и каскад нижележащих киназ с факторами трансляции. Это подавление необходимо для контроля синтеза белка, роста и пролиферации клеток. При мутациях в TSC1 или TSC2 возникает гиперактивация mTOR-пути и связанных с ним киназных каскадов, что приводит к неконтролируемому клеточному росту и размножению[5].
Гамартин и туберин формируют ГТФазу, который ингибирует Rheb — ГТФазу, активирующую mTOR. Повреждение любого из генов TSC нарушает функцию этого комплекса, объясняя сходные клинические проявления при мутациях в TSC1 или TSC2[5].
Кроме того, мутации генов TSC оказывают влияние на структуру нейронов и синапсов, а также на нейротрансмиссию. Это может приводить к фундаментальным изменениям в нейронных сетях, дисбалансу возбуждения и торможения, что клинически проявляется эпилепсией, умственной отсталостью и аутизмом[5].
В лёгочной ткани ТС проявляется картиной лимфангиолейомиоматоза (ЛАМ). Она характеризуется диффузным двусторонним разрастанием в лёгких гладкомышечноподобных клеток. Гистологически выделяют два типа клеток ЛАМ: мелкие веретеновидные клетки с эозинофильной цитоплазмой и более крупные эпителиоидоподобные клетки с обильной цитоплазмой. Клетки формируют микроскопические узелки, в состав которых также входят лимфатические сосуды и лимфоциты. Характерное разрушение эластических волокон и коллагена базальной мембраны происходит за счёт секреции матриксных металлопротеиназ. Важной особенностью является постоянное наличие в клетках ЛАМ рецепторов к половым гормонам[6].
В головном мозге туберы содержат гигантские диспластические нейроны и астроциты. Субэпендимальные узлы, обнаруживаемые более чем у 80 % пациентов с ТС, преимущественно формируются вдоль стенок боковых и третьего желудочков головного мозга. Примерно в 5—15 % случаев эти узлы трансформируются в субэпендимальные гигантоклеточные астроцитомы[6].
Среди множества кожных проявлений ТС выделяются характерные гистологические особенности: концентрический фиброз и утолщение коллагена, сосудистая гиперплазия, пролиферация фибробластов и уменьшение эластических волокон. Наиболее патогномоничным признаком является перифолликулярный фиброз, сопровождающийся атрофией и компрессией кожных придатков[6].
Эпидемиология
Распространённость заболевания колеблется в диапазоне от 1:6000 до 1:10000. Наследование происходит по аутосомно-доминантному типу, при этом около 80 % случаев обусловлены впервые возникшими (de novo) мутациями[3].
Диагностика
Для ТС характерно поражение различных органов и систем:
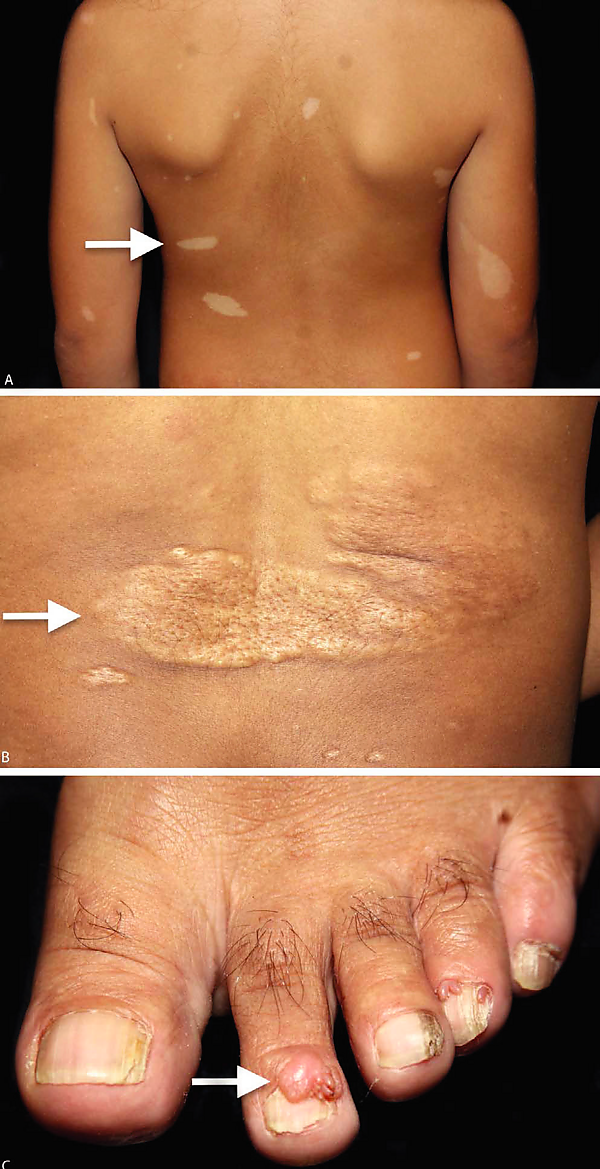
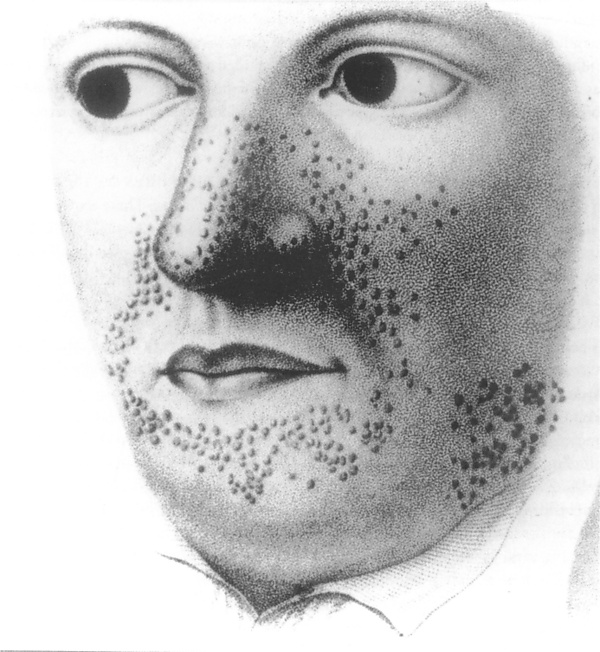
- Гипопигментированные пятна — наиболее распространённое кожное проявление, обнаруживаемое примерно у 90 % больных в виде светлых участков кожи. Фиброзные цефалические бляшки чаще всего локализуются на лбу, но могут появляться на любом участке лица или волосистой части головы, представляя собой гладкие или бугристые образования телесного, розового, красного или коричневого цвета. Ангиофибромы лица встречаются у 75 % пациентов и обычно располагаются по типу «бабочки» в скуловой области. Фибромы также часто встречаются и могут появляться после травм, причём около 90 % из них локализуются на пальцах ног[6].
- ЛАМ преимущественно развивается у женщин репродуктивного возраста. Большинство пациентов с ЛАМ не имеют симптомов, и заболевание обнаруживается только при инструментальном обследовании. Возможными симптомами могут быть боль в груди или одышка, которая при внезапном появлении может свидетельствовать о спонтанном пневмотораксе. Хилоторакс также является возможным проявлением и может сопровождаться прогрессирующей одышкой[6].
- Поражения сердца встречаются у 50—70 % пациентов в различные периоды жизни. По данным исследований, рабдомиомы сердца были вторым по частоте проявлением ТС в младенчестве и раннем детском возрасте после эпилептических приступов. У большинства детей с ТС заболевание протекает без клинических проявлений со стороны сердечно-сосудистой системы. Симптоматика рабдомиом варьирует в зависимости от возраста ребёнка, размеров и локализации опухолевых образований. Наиболее частыми клиническими проявлениями становятся: сердечная недостаточность, аритмии, гидроперикад и кардиомегалия. В медицинской литературе описаны летальные исходы, связанные как с прогрессирующей сердечной недостаточностью, так и с фатальными нарушениями сердечного ритма[4][6].
- Почечные ангиомиолипомы встречаются у 55—75 % пациентов, причём их распространённость увеличивается с возрастом. Эти образования часто протекают бессимптомно, но могут проявляться болью в боку, внутрибрюшным кровотечением, гематурией или пальпируемым болезненным образованием в животе[6].
- При туберозном склерозе гамартомы сетчатки выявляются более чем у половины пациентов. Эти образования могут быть как односторонними, так и двусторонними, причём билатеральное поражение встречается примерно у 50 % больных. Характерно, что данные изменения можно обнаружить уже в первые дни жизни ребёнка. В большинстве случаев гамартомы протекают бессимптомно, оставаясь стабильными на протяжении жизни или постепенно регрессируя. Однако у пациентов с крупными образованиями может наблюдаться потеря полей зрения. В редких случаях возможно развитие осложнений, приводящих к снижению зрения: субретинальная экссудация, макулярный отёк, кровоизлияния в стекловидное тело и глаукома[4].
- При туберозном склерозе наблюдаются разнообразные поражения желудочно-кишечного тракта, затрагивающие ротовую полость, печень, селезёнку, поджелудочную железу и прямую кишку. Характерными проявлениями в полости рта являются узловые образования — фибромы и папилломы, преимущественно локализующиеся на переднем крае дёсен (чаще верхней челюсти), а также на губах, слизистой щёк, языке и небе. Практически у всех пациентов отмечаются дефекты зубной эмали. Со стороны кишечника наиболее часто (в 50—78 % случаев) выявляются полипы прямой кишки[4].
- Эндокринные нарушения при ТС преимущественно связаны с опухолевым поражением желёз внутренней секреции. Наиболее характерны ангиомиолипомы надпочечников (25 % случаев), реже встречаются одиночные или множественные аденомы коркового слоя[4].
- При туберозном склерозе костные изменения наблюдаются у 40—50 % пациентов. Наиболее характерным проявлением являются очаги склероза в костях свода черепа, преимущественно в лобной и теменной областях. Эти округлые образования диаметром от 0,2 до 2 см обычно становятся заметными после 10 лет. Аналогичные склеротические очаги обнаруживаются в телах позвонков и тазовых костях, с типичной локализацией в области крестцово-подвздошных сочленений. Особенностью периферических склеротических изменений тазовых костей является их диффузный характер с нечёткими границами, что иногда приводит к ошибочной диагностике остеобластических метастазов[4].
Компьютерная и магнитно-резонансная томография головного мозга проводятся для выявления субэпендимальных гигантоклеточных астроцитом. Эти методы также позволяют оценить количество и локализацию кортикальных туберов. В некоторых случаях могут обнаруживаться сосудистые диспластические изменения[7].
Ультразвуковое исследование почек проводится для оценки динамики ангиомиолипом и кист, что позволяет своевременно принять решение о хирургическом вмешательстве до развития почечной недостаточности[7].
Эхокардиография позволяет выявить рабдомиомы сердца[7].
Позитронно-эмиссионная томография позволяет идентифицировать эпилептогенные туберы в головном мозге[7].
Молекулярно-генетическое исследование позволяет выявить мутации в генах TSC1 и TSC2 методом секвенирования в 70—80 % случаев. Однако отсутствие выявленной мутации не исключает диагноз[7].
Первичные (большие) признаки[4]:
- ангиофибромы лица (не менее 3) или фиброзные бляшки на лбу;
- гипопигментные пятна (не менее 3 и не менее 5 мм в диаметре);
- нетравматические околоногтевые фибромы (не менее 2);
- участок «шагреневой кожи»;
- множественные гамартомы сетчатки;
- корковые дисплазии (не менее 3);
- субэпендимальные узлы (не менее 2);
- субэпендимальная гигантоклеточная астроцитома;
- рабдомиомы сердца множественные или одиночные;
- лимфангиолейомиоматоз лёгких;
- множественные ангиомиолипомы почек (не менее 2).
Вторичные (малые) признаки[4]:
- многочисленные углубления в эмали зубов (не менее 3);
- фибромы в полости рта (не менее 2);
- гамартомы внутренних органов;
- ахроматический участок сетчатой оболочки глаза;
- пятна типа конфетти на коже;
- множественные кисты почек.
Достоверный диагноз устанавливается при выявлении либо двух больших (первичных) диагностических признаков, либо одного большого признака в сочетании с двумя малыми (вторичными)[4].
Вероятный диагноз может быть рассмотрен при наличии одного большого признака, либо сочетания одного большого и одного малого признака, либо двух и более малых признаков[4].
Диагностические критерии были утверждены на Международной консенсусной конференции по ТС в 2012 году. Особое значение в диагностике имеет генетическое подтверждение: обнаружение патогенной мутации в генах TSC1 или TSC2 является абсолютным диагностическим критерием, достаточным для однозначной постановки диагноза туберозного склероза независимо от клинических проявлений[4].
Дифференциальная диагностика
Дифференциальная диагностика ТС проводится со следующими состояниями[4][6]:
- нейрофиброматоз I типа;
- нейрофиброматоз II типа;
- синдром Луи — Бар;
- болезнь Гиппеля — Линдау;
- синдром Стерджа — Вебера;
- синдром Бёрта — Хогга — Дьюба;
- множественная эндокринная неоплазия 1-го типа;
- витилиго;
- синдром Ваарденбурга;
- гипомеланоз Ито;
- синдром Фогта — Коянаги — Харада;
- синдром Гольтца;
- синдром Блоха — Сульцбергера;
- синдром Олье.
Осложнения
К возможным осложнениям ТС относятся[6]:
- почечно-клеточный рак;
- рецидивирующий пневмоторакс;
- обструктивная гидроцефалия;
- рефрактерная эпилепсия;
- стоматит;
- пневмония;
- гиперлипидемия;
- гипергликемия;
- миелосупрессия.
Лечение
Для контроля эпилепсии при ТС часто применяют антиконвульсанты. Однако примерно у трети пациентов отмечается фармакорезистентность, требующая хирургического вмешательства. Экстренные нейрохирургические операции могут потребоваться при осложнениях, таких как гидроцефалия. Согласно международным рекомендациям 2012 года, симптомные субэпендимальные гигантоклеточные астроцитомы, вызывающие обструктивную гидроцефалию, подлежат хирургической резекции. Для бессимптомных субэпендимальных гигантоклеточных астроцитомы препаратами выбора являются ингибиторы mTOR[6].
При ангиомиолипомах размером более 3,5 см рекомендуется артериальная эмболизация для предотвращения нефрэктомии и снижения риска почечных осложнений. Для образований менее 3 см первой линией терапии считаются ингибиторы mTOR[6].
У 7—10 % пациентов с лёгочными проявлениями развивается хилоторакс. Традиционные подходы включают безжировую диету, торакоцентез, плевродез или лигирование грудного протока. Однако современные исследования подтверждают эффективность сиролимуса в контроле этого осложнения. В некоторых случаях на фоне прогрессирующей дыхательной недостаточности из-за обширного поражения может потребоваться трансплантация лёгких[6].
При наличии симптомов проводится стандартная терапия сердечной недостаточности и нарушений ритма в зависимости от конкретного клинического проявления. При отсутствии тяжёлых клинических проявлений и успешной медикаментозной терапии, как правило, наблюдается положительная динамика с постепенным восстановлением сердечной функции. Это связано с естественным регрессом опухолевых образований и пропорциональным ростом сердца по мере развития ребёнка[4].
Прогноз
Прогноз при ТС вариабелен и зависит от индивидуальных проявлений заболевания. Каждый пациент имеет уникальную клиническую картину и, соответственно, различное течение болезни[6].
Показатели смертности при ТС существенно превышают общепопуляционные. Долгосрочные исследования демонстрируют уровень смертности от 4,8 до 8,3 % при периоде наблюдения от 8 до 17,4 года. Основными причинами летальных исходов являются[6]:
- осложнения эпилептического статуса;
- кровотечения из почечных ангиомиолипом;
- бронхопневмония;
- осложнения ЛАМ;
- неонатальная сердечная недостаточность, связанная с рабдомиомами сердца.
Для пациентов, перенёсших трансплантацию лёгких по поводу ЛАМ, пятилетняя выживаемость составляет около 65 %[6].
Диспансерное наблюдение
Согласно рекомендациям международного консенсуса по туберозному склерозу, пациенты нуждаются в пожизненном мониторинге для своевременного выявления характерных проявлений заболевания. Диспансерное наблюдение проводится по следующим рекомендациям[8]:
- Контроль неврологических проявлений включает:
- магнитно-резонансную томографию головного мозга каждые 1—3 года у бессимптомных пациентов младше 25 лет;
- углублённое нейропсихологическое обследование в ключевые возрастные периоды:
- 0—3 года;
- 3—6 лет;
- 6—9 лет;
- 12—16 лет;
- 18—25 лет.
- рутинная электроэнцефалография при подозрении на эпилептическую активность.
- Мониторинг почечных проявлений:
- магнитно-резонансная томография брюшной полости каждые 1—3 года (пожизненно) для оценки ангиомиолипом и кист;
- ежегодная оценка функции почек и артериального давления.
- Кардиологический мониторинг:
- эхокардиография каждые 1—3 года у бессимптомных детей до регресса рабдомиом;
- электрокардиография каждые 3—5 года у бессимптомных пациентов всех возрастов.
- Мониторинг лёгочных проявлений:
- компьютерная томография каждые 5—10 лет у пациентов группы риска по ЛАМ.
- Офтальмологический мониторинг:
- ежегодный осмотр при выявленных ранее изменениях или симптомах;
- дополнительные исследования при появлении новых жалоб.
Профилактика
Не разработана.
Примечания
- ↑ Disease Ontology (англ.) — 2016.
- ↑ Monarch Disease Ontology release 2018-06-29sonu — 2018-06-29 — 2018.
- ↑ 1 2 3 4 Монахов К. Н., Романова О. Л., Амелина П. О., Молодых К. Ю., Астахов Ю. С., Нечипоренко П. А., Атласова Л. К. Туберозный склероз (рус.) // Вестник дерматологии и венерологии : журнальная статья. — 2017. — Т. 93, № 5. — С. 82–88. — doi:10.25208/0042-4609-2017-93-5-82-88.
- ↑ 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 Дорофеева М. Ю., Белоусова Е. Д., Пивоварова А. М. Рекомендации по диагностике и лечению туберозного склероза (рус.) // Журнал неврологии и психиатрии им. С.С. Корсакова : журнальная статья. — 2014. — Т. 114, № 3. — С. 58–74.
- ↑ 1 2 3 4 Paolo Curatolo, Roberta Bombardieri, Sergiusz Jozwiak. Tuberous sclerosis // The Lancet. — 2008-08. — Т. 372, вып. 9639. — С. 657–668. — ISSN 0140-6736. — doi:10.1016/s0140-6736(08)61279-9.
- ↑ 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 Rout P., Zamora E.A., Aeddula N.R. Tuberous Sclerosis (англ.) // StatPearls [Internet] : электронный ресурс. — Treasure Island (FL): StatPearls Publishing, 2025. — Январь.
- ↑ 1 2 3 4 5 David Neal Franz. Tuberous Sclerosis Complex (англ.). Medscape (6 ноября 2024).
- ↑ Darcy A. Krueger, Hope Northrup, Hope Northrup et all. Tuberous Sclerosis Complex Surveillance and Management: Recommendations of the 2012 International Tuberous Sclerosis Complex Consensus Conference // Pediatric Neurology. — 2013-10. — Т. 49, вып. 4. — С. 255–265. — ISSN 0887-8994. — doi:10.1016/j.pediatrneurol.2013.08.002.
Литература
- Тарасенко Григорий Николаевич, Кузьмина Юлиана Валентиновна, Григорьева Екатерина Борисовна, Кузнецова Алина Александровна. Туберозный склероз // Российский журнал кожных и венерических болезней. — 2015. — № 2.
- Важбин Л. Б., Белова Н. И., Лезвинская Е. М., Стрибук П. В. Туберозный склероз // Российский журнал кожных и венерических болезней. — 2013. — № 1.
- Мосин Илья Михайлович, Дорофеева Марина Юрьевна, Балаян Инна Григорьевна, Яркина Оксана Сергеевна. Офтальмологические проявления туберозного склероза // Российский вестник перинатологии и педиатрии. — 2012. — № 5.
- Янус Григорий Аркадьевич, Суспицын Евгений Николаевич, Дорофеева Марина Юрьевна, Имянитов Евгений Наумович. Молекулярная диагностика туберозного склероза // Педиатр. — 2013. — № 1.
Ссылки
- Дорофеева М. Ю., Страхова О. С. и др. Туберозный склероз. Lvrach.ru
- Сакович Р. А., Чиж Г. В. Туберозный склероз. // Новости лучевой диагностики 2002, № 1-2. С. 74-76
- Туберозный склероз. Pedklin.ru