Синдром Фацио — Лонде
Синдро́м Фаци́о — Ло́нде (СФЛ, дефици́т перено́счика рибофлави́на, синдром Бра́уна — Виале́тто — Ван Ла́эра) — очень редкое неврологическое заболевание, при котором развивается прогрессирующее поражение периферических и черепных нервов. Это приводит к мышечной слабости, бульбарным расстройствам, потере слуха и зрения, а также сенсорной атаксии. Заболевание возникает из-за нарушения работы транспортёра рибофлавина, отвечающего за доставку витамина B2 из кишечника в клетки организма. Основная причина патологии — мутации в генах SLC52A1, SLC52A2 и SLC52A3. Лечение заключается в назначении высоких доз рибофлавина, что помогает компенсировать его дефицит и замедлить прогрессирование болезни[1].
Общие сведения
История
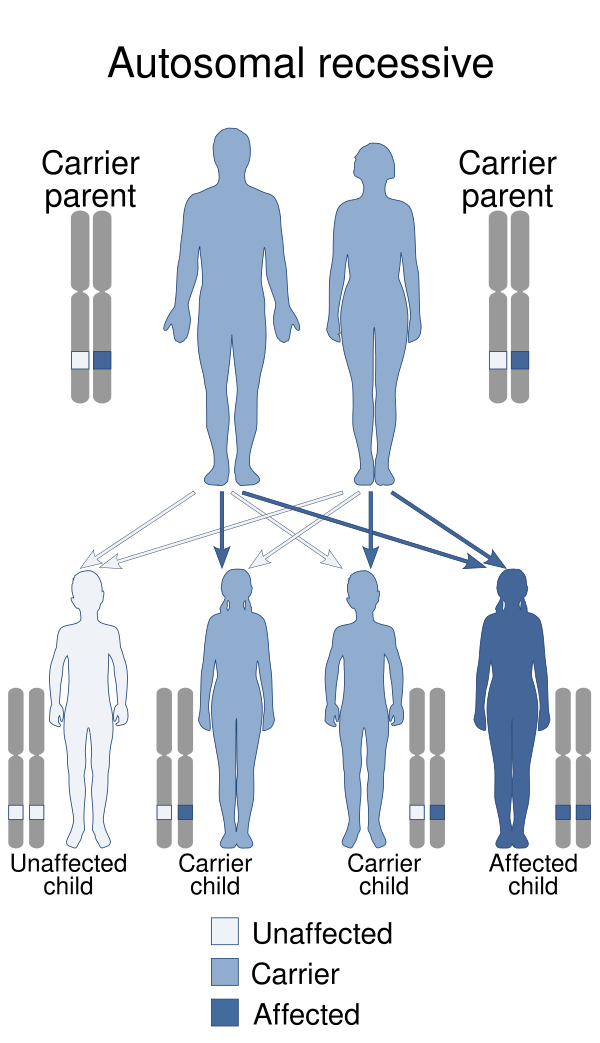
Изучение этого заболевания началось в конце XIX века, причём исследования велись одновременно в Европе и США. В 1892 году итальянский патолог Евгенио Фацио описал случай болезни у матери и её четырёхлетнего сына, у которых наблюдались симптомы бульбарного паралича. Два года спустя французский врач Поль Лонде зафиксировал аналогичное состояние у брата и сестры, чьи родители состояли в близком родстве. Впоследствии это заболевание получило название синдром Фацио — Лонде (СФЛ). Примерно в тот же период американский невролог Чарльз Браун описал новую форму бокового амиотрафического синдрома. Позже исследования Виалетто и Лаэра подтвердили, что эта болезнь имеет аутосомно-рецессивный тип наследования, и она была названа синдром Брауна — Виалетто — Ван Лаэра. Со временем из-за сходства клинических проявлений и механизмов развития оба синдрома объединили под общим названием — дефицит переносчика рибофлавина. Ключевой этап в изучении болезни наступил в 2010—2012 годах, когда была установлена его генетическая природа — мутации в генах SLC52A1, SLC52A2 и SLC52A3, приводящие к нарушению транспорта рибофлавина[1].
Классификация
В зависимости от гена, в котором происходит мутация, СФЛ классифицируется на три типа[2][3]:
- 1-й тип — крайне редкое состояние, описан всего 1 случай. Проявляется в младенческом возрасте в виде генерализованных или фокальных тонико-клонических судорог, метаболического ацидоза и гипераммониемии, с положительной реакцией на терапию рибофлавином. Связан с мутацией в гене SLC52A1;
- 2-й тип — встречается в 40 % случаев, характерная клиническая картина включает мышечную слабость в руках и шее, потерю зрения, нарушение слуха и сенсорную атаксию. Связан с мутацией в гене SLC52A2;
- 3-й тип — встречается в более чем 50 % случаев, характерно большее распространение паралича голосовых связок, а мышечная слабость имеет генерализованный характер. Связан с мутацией в гене SLC52A3.
Этиология
Патогенез
Рибофлавин и его активные формы — флавинмононуклеотид и флавинадениндинуклеотид — являются ключевыми участниками важнейших клеточных процессов. Они играют критическую роль в энергетическом обмене в митохондриях, реакциях на окислительный стресс, а также участвуют в синтезе других витаминов и кофакторов. Гены SLC52A1, SLC52A2 и SLC52A3 отвечают за синтез трансмембранных белков-переносчиков рибофлавина. Эти транспортные белки обеспечивают всасывание витамина B2 в желудочно-кишечном тракте, а также его обратное поглощение в почечных канальцах. После проникновения в клетку рибофлавин преобразуется в активные формы флавинмононуклеотида и флавинадениндинуклеотида, которые затем используются в различных биохимических процессах. При мутациях нарушается работа транспортных белков, что приводит к клеточному дефициту рибофлавина. Возникающая митохондриальная дисфункция вызывает энергетический дефицит, который особенно губителен для нейронов. В результате развивается тяжёлое нейродегенеративное поражение нервной системы[1].
Эпидемиология
С 2010 года в медицинской литературе отмечается рост числа пациентов с генетически подтверждённым диагнозом СФЛ. Точная распространённость СФЛ остаётся неизвестной. По имеющимся оценкам, это состояние встречается примерно у 1 человека на 1 000 000 населения. Хотя большинство пациентов с СФЛ 2-го или 3-го типа имеют симптомы в раннем возрасте, при 3-м типе описаны случаи с поздним началом (10—30 лет). Заболевание одинаково часто встречается у мужчин и женщин[3][4].
Диагностика
Клиническая картина у пациентов с СФЛ при дебюте обычно включает нарушение слуха и сенсорную атаксию, за которыми следуют прогрессирующая слабость верхних конечностей, атрофия зрительного нерва, бульбарные нарушения и дыхательная недостаточность. Дыхательные нарушения, обусловленные нейрогенным параличом диафрагмы, часто являются ранним проявлением. Многие пациенты демонстрируют эпизоды задержки дыхания в течение первого года заболевания. Интервал между началом заболевания и появлением моторных нарушений варьирует, но обычно составляет 1—2 года. У некоторых пациентов фактором для манифестации или ухудшения симптомов служит провоцирующее событие, например травма или инфекция[3].
Слабость мимических мышц, вызванная дегенерацией VII черепного нерва, отмечается у 55 % пациентов с СФЛ 3 типа[3].
Признаки бульбарного паралича встречаются часто, отмечаясь более чем у 50 % пациентов. У большинства наблюдаются дизартрия и нарушения питания вследствие дисфагии. При неврологическом осмотре часто выявляются атрофия и фасцикуляции языка[3].
Другие вариабельные проявления включают[3]:
- электромиография выявляет признаки хронической частичной денервации. Скорость проведения по моторным нервам обычно остаётся в норме[3].
- электроэнцефалография может показывать избыточную тета-активность или замедление основной активности[3].
- магнитно-резонансная томография головного мозга обычно без патологических изменений, однако у небольшого числа пациентов наблюдаются атрофия мозжечка, повышенная интенсивность сигнала на T2-взвешенных изображениях в области мозжечка, коры, подкорковых структур и ствола мозга[3].
Исследование концентрации ацилкарнитинов в крови методом тандемной масс-спектрометрии показывает накопление ацилкарнитинов с короткой и средней цепью[1].
Подтвердить диагноз позволяет молекулярное тестирование на мутации в генах SLC52A1, SLC52A2 или SLC52A3 методом полимеразной цепной реакции или секвенирования нового поколения[1].
Дифференциальная диагностика
Дифференциальная диагностика СФЛ проводится со следующими состояниями[3]:
- синдром ахалазии-аддисонизма-алакримии (синдром Оллгрова);
- боковой амиотрофический склероз;
- недостаточность ацил-КоА-дегидрогеназы с неонатальным началом;
- спинальная мышечная атрофия.
Лечение
Не существует специфического лечения СФЛ. Основной метод терапии — пожизненное применение высоких доз рибофлавина, демонстрирующее высокую клиническую эффективность. Такое патогенетическое лечение, назначаемое сразу после установления диагноза, способствует улучшению двигательных функций и нормализации нейрофизиологических параметров[1].
Важным компонентом терапии является диета с повышенным содержанием рибофлавина. Особое внимание питанию следует уделять беременным и кормящим женщинам с данным заболеванием для профилактики развития дефицита витамина у ребёнка[1].
В рамках поддерживающей терапии при тяжёлых формах заболевания может потребоваться[1]:
- установка гастростомы при выраженной дисфагии;
- кохлеарная имплантация при потере слуха.
При дыхательных нарушениях часто необходима искусственная вентиляция лёгких. В некоторых случаях выполняется трахеостомия[5].
Отдельные клинические случаи описывают применение глюкокортикостероидов и внутривенных иммуноглобулинов, однако эти методы показали низкую эффективность — после кратковременной стабилизации обычно следует прогрессирование заболевания[5].
Важную роль играют реабилитационные мероприятия[5]:
- логопедическая коррекция;
- эрготерапия;
- физиотерапия.
Сколиоз у пациентов с СФЛ может потребовать хирургическую коррекцию при необходимости[5].
Прогноз
Прогноз заболевания напрямую определяется своевременностью диагностики и началом лечения. У пациентов, не получающих терапию, наблюдается стремительное прогрессирование заболевания с неблагоприятным исходом. Своевременно назначенное лечение высокими дозами рибофлавина предотвращает выраженную нейродегенерацию, в большинстве случаев способствуя стабилизации состояния и обеспечивая нормальные темпы психомоторного развития у детей[1].
Клинические наблюдения показывают, что раннее начало терапии существенно улучшает долгосрочный прогноз, позволяя минимизировать неврологический дефицит и сохранить качество жизни пациентов. Особенно важным является начало лечения в досимптоматический период или на ранних стадиях заболевания, когда ещё не развились необратимые изменения нервной системы[1].
Диспансерное наблюдение
После начала терапии рибофлавином рекомендуется проводить контрольные обследования каждые 3 и 6 месяцев, включая[3]:
- стандартный физикальный и неврологический осмотр;
- определение концентрации рибофлавина, флавинадениндинуклеотида и флавинмононуклеотида в крови;
- анализ ацилкарнитинового профиля крови.
В дальнейшем для детей старшего возраста и взрослых достаточно наблюдения раз в полгода, тогда как для детей младшего возраста требуется более частый мониторинг состояния[3].
Профилактика
Не разработана.
Примечания
- ↑ 1 2 3 4 5 6 7 8 9 10 11 Масленников Д.Н. Генокарта — генетическая энциклопедия (рус.). www.genokarta.ru. Дата обращения: 9 мая 2025.
- ↑ 1 2 Marisa A. O'Brien, Susan M. Culican, Marwan S. Shinawi, Craig M. Zaidman. Child Neurology: Five-Year Update on Siblings With Riboflavin Transporter Deficiency // Neurology. — 2024-12-10. — Т. 103, вып. 11. — ISSN 1526-632X 0028-3878, 1526-632X. — doi:10.1212/wnl.0000000000209969.
- ↑ 1 2 3 4 5 6 7 8 9 10 11 12 Cali E., Dominik N., Manole A. et al. Riboflavin Transporter Deficiency (англ.) // GeneReviews® : Электронный ресурс. — 2021. — 8 апрель.
- ↑ B. Jaeger, E. Hoytema van Konijnenburg, M. A. Groenveld, M. Langeveld, N. I. Wolf, A. M. Bosch. Riboflavin transporter deficiency, the search for the undiagnosed: a retrospective data mining study (англ.) // Orphanet Journal of Rare Diseases. — 2024-11-01. — Vol. 19, iss. 1. — ISSN 1750-1172. — doi:10.1186/s13023-024-03428-y.
- ↑ 1 2 3 4 Riboflavin Transporter Deficiency (англ.). National Organization for Rare Disorders (31 января 2019).
Литература
- Селивёрстов Ю. А., Клюшников С. А., Иллариошкин С. Н. Спинальные мышечные атрофии: понятие, дифференциальная диагностика, перспективы лечения // Нервные болезни. — 2015. — № 3.
- Евтушенко С. К., Морозова Т. М., Шестова Е. П., Омельяненко А. А., Симонян В. А., Луцкий И. С. Спинальные мышечные атрофии и боковой амиотрофический склероз как проявление болезни двигательного нейрона у детей // Международный неврологический журнал. — 2013. — № 6 (60).