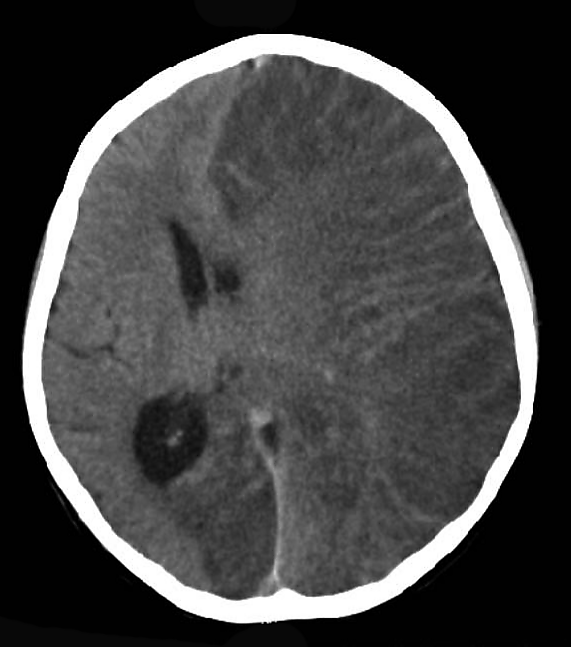
Аутоиммунный энцефалит
Аутоимму́нный энцефали́т (АЭ) — включает в себя группу неврологических заболеваний, при которых преимущественно поражается серое вещество головного мозга. В основе их патогенеза лежит выработка аутоантител, направленных против внутриклеточных или внеклеточных структур нервной системы, которые воспринимаются как антигены. Среди аутоиммунных энцефалитов различают две основные формы: паранеопластическую, возникающую на фоне злокачественных опухолей, и идиопатическую, которая развивается независимо от наличия иного заболевания[1].
История
В 1961 году Рассел предложил механизм неврологического повреждения при паранеопластических синдромах, связанный с образованием аутоантител, спровоцированным реакцией иммунной системы на определённые типы рака. Позже, в 1968 году, Корселлис и его коллеги описали нескольких пациентов с раком лёгких, у которых также развились неврологические симптомы — потеря памяти, нейропсихиатрические нарушения и судороги — без признаков метастазов в мозг. При патологоанатомическом исследовании обнаружили значительное воспалительное поражение структур лимбической системы и назвали это новое состояние «лимбическим энцефалитом»[2].
В 1981 году Джон Ньюсом-Дэвис впервые подтвердил аутоиммунный механизм паранеопластического неврологического расстройства, успешно вылечив три случая миастенического синдрома Ламберта — Итона с помощью плазмафереза и иммуносупрессивной терапии кортикостероидами. В 1990 году Познер сравнил профили сыворотки и спинномозговой жидкости у 18 пациентов до и после плазмафереза, сделав вывод, что аутоантитела при паранеопластическом синдроме могут синтезироваться непосредственно в спинномозговой жидкости[2].
В 2001 году Лигуори и Бакли независимо друг от друга представили клинические случаи двух пациентов с обратимым лимбическим энцефалитом, ассоциированным с антителами к потенциал-зависимым калиевым каналам. Наконец, в 2005 году Дальмау и его коллеги описали энцефалит, связанный с аутоантителами к NMDA-рецепторам, у 12 пациентов с NMDA-энцефалитом[2].
Классификация
По этиологии аутоиммунный энцефалит (АЭ) делится на три группы[3][4]:
- паранеопластический АЭ — при котором поражение нервной системы происходит на фоне подлежащего онкологического заболевания;
- идиопатический АЭ — при котором поражение нервной системы происходит первично, без выявленной предшествующей болезни;
- АЭ на фоне системного аутоиммунного заболевания (расширенная классификация).
В зависимости от поражённого антигена, АЭ делится на[4]:
- АЭ с поражением внутриклеточных антигенов нейронов с выработкой соответствующих антител (антинейрональное ядерное антитело 1-го типа, антитела к коллапсин-опосредующему белку 5, антитела к глутаматдекарбоксилазе, антитела к амфифизину и др.);
- АЭ с поражением поверхностных антигенов нейронов с выработкой антител к ним (NMDA-рецептор, потенциал-зависимые калиевые и кальциевые каналы, рецептор ГАМК, AMPA-рецептору, глутаматному рецептору 1-го и 3-го типа).
Этиология
Паранеопластический АЭ возникает, когда антигены, общие для опухолевых клеток и нормальных нейрональных клеток, провоцируют антитело-опосредованную атаку на структуры нервной системы. Чаще всего паранеопластические синдромы ассоциированы с мелкоклеточным раком лёгкого, но также могут развиваться при нейробластоме, герминогенных опухолях яичка, раке молочной железы, лимфоме Ходжкина, тимоме и незрелых тератомах яичников[4].
Этиология идиопатического АЭ неизвестна[3].
Патогенез
Развитие АЭ во многом зависит от локализации антигенов нервной клетки, которые вовлекаются в патологический процесс. Эти антигены могут находиться внутри нейронов (в цитоплазме или ядре) либо на их мембранах и в синапсах. Соответственно, антитела делятся на две основные группы: нейрональные (направленные против внутриклеточных структур) и мембранные/синаптические (действующие на поверхностные белки нейронов).
Наиболее изучен механизм АЭ, при котором иммунный ответ запускается антигенами опухолевых клеток. На сегодня известно более 30 видов нейрональных антител, которые можно разделить на три категории:
- Антитела, встречающиеся как при паранеопластических, так и при идиопатических АЭ, — воздействуют на внеклеточные мембранные белки.
- Антитела, преимущественно ассоциированные с идиопатическими АЭ, — могут быть направлены как на мембранные, так и на внутриклеточные структуры и редко связаны с опухолями.
- Антитела к внутриклеточным антигенам активируют цитотоксические Т-клетки, что приводит к необратимому повреждению нейронов. При этом наблюдаются некроз клеток, дегенерация аксонов, глиоз и активация микроглии, но без демиелинизации.
- Антитела к мембранным и синаптическим антигенам нарушают функцию рецепторов и ионных каналов, вызывая потенциально обратимую дисфункцию нейронов при своевременной иммунотерапии.
- Антитела к внутриклеточным синаптическим антигенам могут сочетать оба механизма — как Т-клеточную цитотоксичность, так и прямое воздействие на антиген[1].
Эпидемиология
Эпидемиологические данные по АЭ остаются неполными из-за вариабельной клинической картины и множества возможных мишеней для антител. Заболеваемость АЭ среди взрослого населения колеблется от 0,7 до 12,6 случая на 100 000 человек, причём патология встречается как у взрослых, так и у детей. Наиболее изученной формой является АЭ с антителами к NMDA-рецептору. Согласно крупному многоцентровому исследованию, 80 % пациентов с этим диагнозом составили женщины, средний возраст дебюта заболевания — 21 год. При этом у 38 % обследованных был выявлен сопутствующий опухолевый процесс, чаще всего — тератома яичников[5].
Диагностика
АЭ представляет собой гетерогенную группу заболеваний, характеризующихся широким спектром неврологических и психиатрических симптомов. Клинические проявления зависят от специфичности антител и мишеней их воздействия, однако можно выделить ключевые синдромы, характерные для этих состояний[6]:
- Поведенческие нарушения: многих пациентов наблюдаются агрессия, раздражительность, лабильность настроения, галлюцинации и выраженные нарушения цикла сна и бодрствования. Затем к ним присоединяются спутанность сознания, амнезия и судороги.
- Когнитивные нарушения: в острой фазе у пациентов часто отмечаются дезориентация, спутанность сознания, конфабуляции и амнезия, особенно при поражении структур лимбической системы.
- Судорожный синдром: судороги встречаются при большинстве форм АЭ.
- Двигательные расстройства: двигательные нарушения варьируют в зависимости от типа антител. Могут наблюдаться полиморфная гиперкинезия, хорея, стереотипия и дистония, особенно в области лица и рта, гиперэкплексия, миоклонус и офтальмоплегия.
- Дисфункция вегетативной нервной системы: колебания артериального давления, тахи- и брадиаритмии, ортостатическая гипотензия и нарушение потоотделения часто встречаются при АЭ.
- Болевой синдром: для пациентов с АЭ характерна нейропатическая боль.
При этом имеется ряд особенностей клинической картины в зависимости от патогенетического механизма[4]:
- Анти-Hu энцефалит (ассоциированный с антителами к нейрональному ядерному антигену 1-го типа) представляет собой наиболее распространённую паранеопластическую форму аутоиммунного энцефалита. Клиническая картина включает три основных синдрома: паранеопластический энцефаломиелит, подострую сенсорную нейропатию и паранеопластическую дегенерацию мозжечка. Хотя судороги не являются доминирующим симптомом, у части пациентов может развиться особый тип фокальных моторных приступов с вовлечением лица и дистальных отделов конечностей, повторяющихся каждые несколько секунд или минут.
- Анти-Ma энцефалит (ассоциирован с антителами к паранеопластическому антигену человека Ма2) у молодых пациентов встречается при опухолях яичка, у пожилых пациентов — ассоциирован с мелкоклеточным раком лёгкого или раком молочной железы. Неврологические симптомы (лимбические, диэнцефальные или стволовые нарушения) обычно предшествуют выявлению опухоли. Классическая картина лимбического энцефалита встречается лишь у 26 % пациентов, тогда как поражение ствола мозга чаще проявляется офтальмоплегией (92 %).
- Анти-CV2 энцефалит (ассоциированный с белком CRMP5) — редкий подтип, связанный с мелкоклеточным раком лёгкого и тимомой. Клинически проявляется хореиформными гиперкинезами.
- Анти-GAD энцефалит (ассоциирован с антителами к глутаматдекарбоксилазе) редко встречается при опухолевых процессах, но часто встречается при сахарном диабете 1-го типа. Клиническая картина включает классический лимбический энцефалит с поражением височных долей, синдром «ригидного человека» и раннее развитие эпилептических приступов.
- Анти-NMDA энцефалит (ассоциирован с антителами к NMDA-рецептору) — клиническая картина заболевания имеет чёткую стадийность развития симптомов. Первоначально у пациентов наблюдается продромальный период с гриппоподобными симптомами, включая лихорадку, недомогание, головные боли и анорексию. Затем развиваются психиатрические нарушения, такие как тревога, депрессия, шизофреноподобные состояния и психоз. По мере прогрессирования заболевания присоединяется дисфункция височных долей, проявляющаяся амнезией и судорожными приступами. В конечной стадии развиваются вегетативная дисфункция, дистония и выраженная энцефалопатия.
- Анти-VGKC энцефалит (ассоциирован с антителами к потенциал-зависимым калиевым каналам): практически у всех пациентов с этим заболеванием наблюдается раннее развитие фармакорезистентной эпилепсии, что объясняется высокой концентрацией калиевых каналов в лимбических структурах головного мозга, определяющей их значительный эпилептогенный потенциал.
- Анти-AMPA энцефалит (ассоциирован с антителами к альфа-амино-3-гидрокси-5-метил-4-изоксазолпропионовой кислоте) представляет собой редкий подтип АЭ, который характеризуется подострым началом исключительно психиатрических симптомов.
В общем анализе ликвора выявляются плеоцитоз, повышенный уровень белка, наличие специфических олигоклональных иммуноглобулинов[1].
При биохимическом анализе крови характерно повышение концентрации С-реактивного белка[1].
При проведении магнитно-резонансной томографии головного мозга у пациентов с паранеопластическим АЭ характерно выявление гиперинтенсивных очагов на Т2-взвешенных изображениях и в режиме FLAIR. Эти патологические изменения преимущественно локализуются в сером веществе — как в поверхностных отделах коры, так и в глубоких структурах, а также распространяются на прилежащие участки белого вещества. Подобная картина отражает типичное для паранеопластического АЭ поражение центральной нервной системы, при котором аутоиммунный процесс затрагивает как нейрональные структуры серого вещества, так и проводящие пути белого вещества. Особенностью является симметричность и множественность очагов, что помогает дифференцировать эти изменения от других патологических процессов в центральной нервной системе[1].
Современные диагностические критерии аутоиммунного энцефалита включают три ключевых положения[1]:
1. Временные характеристики заболевания:
- острое начало неврологической симптоматики;
- либо подострое развитие симптомов (в течение периода менее 12 месяцев).
2. Обязательные признаки воспалительного процесса в центральной нервной системе (достаточно наличия одного из перечисленных):
- характерные изменения цереброспинальной жидкости: лимфоцитарный плеоцитоз, повышенный уровень белка, увеличение концентрации иммуноглобулинов G, наличие специфических олигоклональных иммуноглобулинов;
- патологические изменения при магнитно-резонансной томографии: выявление гиперинтенсивных очагов на Т2-взвешенных изображениях, аномальные сигналы в режиме FLAIR.
3. Дифференциально-диагностические требования:
- обязательное исключение альтернативных причин неврологической симптоматики: инфекционный энцефалит, черепно-мозговые травмы, метаболические нарушения, токсические воздействия, опухолевые процессы в центральной нервной системе, демиелинизирующие заболевания.
Дифференциальная диагностика
Основные дифференциальные диагнозы аутоиммунного энцефалита[5][6]:
- инфекционный энцефалит;
- височная глиома;
- болезнь Крейтцфельдта — Якоба;
- метаболические энцефалопатии;
- энцефалопатия Хашимото;
- менингоэнцефалиты;
- острое нарушение мозгового кровообращения;
- опухоли головного мозга;
- рассеянный склероз;
- болезнь Альцгеймера;
- токсические энцефалопатии;
- аутоиммунные системные заболевания (волчаночный энцефалит, нейросаркоидоз);
- острые психотические состояния;
- аффективные расстройства;
- наследственные метаболические нарушения.
Осложнения
К возможным осложнениям относятся[5]:
- когнитивные нарушения;
- расстройства сна;
- гиперкинезы;
- вегетативная дисфункция;
- стойкая амнезия;
- коматозное состояние;
- эпилептический статус.
Лечение
Лечение аутоиммунного энцефалита включает иммуносупрессивную терапию и, при наличии новообразования, его хирургическое удаление. Терапевтическая стратегия основана на принципах лечения аутоиммунных заболеваний с целью элиминации патогенных антител. Важно подчеркнуть, что терапию следует начинать незамедлительно при подозрении на диагноз, не дожидаясь результатов анализа на антитела, поскольку раннее начало лечения ассоциировано с лучшими клиническими исходами.
Оптимальное ведение пациентов требует мультидисциплинарного подхода с участием неврологов, ревматологов и онкологов. Первая линия терапии включает кортикостероиды, внутривенные иммуноглобулины и плазмаферез, которые могут применяться как по отдельности, так и в комбинации. Плазмаферез в особенности показан пациентам с тяжёлыми формами заболевания, сопровождающимися выраженной вегетативной дисфункцией, рефрактерными судорогами или синдромом центральной гиповентиляции.
При недостаточной эффективности терапии первой линии переходят к препаратам второй линии, таким как ритуксимаб и циклофосфамид, которые могут использоваться как монотерапия или в комбинации. Особое внимание следует уделить онкологическому скринингу — при выявлении злокачественного новообразования его удаление или химиотерапия не только способствуют улучшению неврологической симптоматики, но и предотвращают рецидивы АЭ[5].
Примечания
Литература
- Полонский Е. Л., Скулябин Д. И., Лапин С. В., Красаков И. В., Тихомирова О. В., Назаров В. Д., Мошникова А. Н., Литвиненко И. В., Слащёва И. М., Маматова Н. Т., Захарова Н. И., Соколова Н. А., Мазинг А. В., Лямина А. В., Белозёрова Ю. Б. Полиморфизм аутоиммунного энцефалита // Анналы клинической и экспериментальной неврологии. — 2019. — № 2.
- Мурашко Алексей Андреевич. Психические нарушения при аутоиммунных энцефалитах // Социальная и клиническая психиатрия. — 2021. — № 1.
- Рамазанов Ганипа Рамазанович, Шевченко Евгений Владимирович, Бардина Елена Михайловна, Коригова Хеди Валерьевна, Ковалёва Элла Александровна, Ахматханова Лиана Хаваж- Баудиновна, Алиев Илгар Садыхович, Синкин Михаил Владимирович. Аутоиммунный энцефалит. Анализ серии случаев // Журнал им. Н. В. Склифосовского «Неотложная медицинская помощь». — 2023. — № 4. — doi:10.23934/2223-9022-2023-12-4-683-689.