Болезнь двигательного нейрона
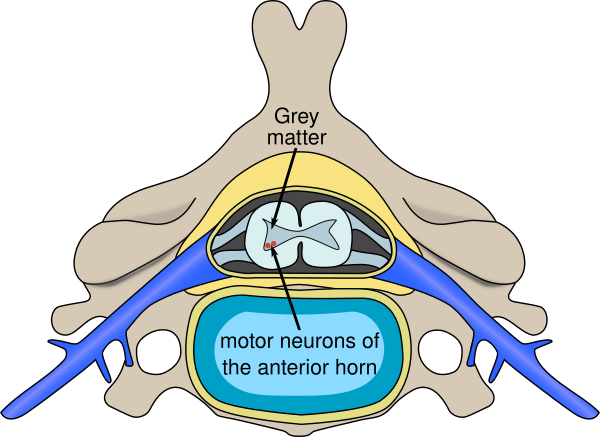
Боле́знь дви́гательного нейро́на (БДН) — общий термин для группы тяжёлых прогрессирующих нейродегенеративных заболеваний, при которых поражаются клетки передних рогов спинного мозга и двигательные ядра черепных нервов ствола мозга. Наиболее распространённой и изученной формой БДН является боковой амиотрофический склероз (БАС). В основе патогенеза БАС и других форм БДН лежат множественные клеточные нарушения, сбои в метаболизме РНК, накопление белковых агрегатов, дисфункция митохондрий, нарушения везикулярного транспорта и аксонального движения, окислительный стресс, дефицит нейротрофической поддержки и активация микроглии. Подавляющее большинство случаев БДН носят спорадический характер, тогда как семейные формы встречаются реже — в 5—10 % случаев[2].
Что важно знать
История
История изучения БДН начинается с первых клинических описаний в XIX веке. В 1830 году Чарльз Белл описал пациента с прогрессирующей слабостью конечностей и языка, обнаружив патологические изменения в передних отделах спинного мозга. Франсуа Аран в 1850 году ввёл термин «прогрессирующая мышечная атрофия», отметив атрофию мелких мышцы кисти, а также «фибриллярные подёргивания» — раннее описание фасцикуляций. Среди его наблюдений был семейный случай БДН, где болезнь отмечалась у сестры и двух дядь по материнской линии. Дюшенн и Крювелье в 1853 году описали бульбарный паралич с атрофией мышц и фибриллярными сокращениями, при этом Крювелье предположил, что атрофия передних корешков первична, а мышечная атрофия вторична[3].
Жан-Мартен Шарко в период с 1865 по 1874 год систематизировал наблюдения за пациентами парижского госпиталя Сальпетриер. В 1865 году он описал случай со спастичностью и склерозом боковых столбов спинного мозга, а в 1874 году ввёл термин «sclérose latérale amyotrophique» (БАС), объединив признаки поражения боковых канатиков (спастичность) и дегенерации передних рогов (атрофия мышц). Шарко также отдельно изучал бульбарную форму и инфантильный паралич с поражением передних рогов. Вильгельм Эрб в 1875 году добавил понятие «первичный латеральный склероз» (ПЛС) после описания пациента со спастическим парапарезом, перешедшим в БАС[3].
В конце XIX века произошла интеграция понятий. Жозеф Дежерин в 1883 году объединил бульбарный паралич и БАС в одну нозологию. Уильям Говерс в 1892 году предложил концепцию спектра болезней двигательного нейрона, включив в него ПМА, бульбарный паралич и БАС. В этот период велись дискуссии о первичности поражения — Шарко и его ученики считали первичным склероз боковых столбов, тогда как Говерс полагал, что дегенеративные процессы в двигательных нейронах происходят одновременно[3].
В XX веке Уолтер Рассел Брейн в 1933 году ввёл объединяющий термин «болезнь двигательного нейрона». Что касается семейных форм, первые описания появились у Арана в 1873 году, отметившего аутосомно-доминантное наследование в одном случае ПМА. В 1880 году Уильям Ослер описал семью из Вермонта с 13 случаями прогрессирующей мышечной атрофии в двух поколениях — позже в этой семье была выявлена мутация в гене супероксиддисмутазы-1. После открытия этой мутации в 1993 году было обнаружено множество других генов, связанных с БАС[3].
Классификация
Согласно британской классификации в термин БДН объединены три основные формы заболевания[4]:
- Боковой амиотрофический склероз (БАС): самая распространённая форма, характеризуется сочетанным поражением верхних и нижних мотонейронов, что приводит к смешанной симптоматике (мышечная слабость, атрофия, спастичность).
- Прогрессирующая мышечная атрофия (ПМА): преимущественно поражаются нижние мотонейроны; на поздних стадиях могут появляться отдельные признаки поражения верхних мотонейронов.
- Первичный латеральный склероз: самая редкая форма БДН, в основном затрагивает только верхние мотонейроны, имеет наиболее благоприятный прогноз по сравнению с другими формами, со временем могут развиваться некоторые симптомы поражения нижних мотонейронов.
Согласно классификации американского национального института неврологических расстройств и инсульта в понятие БДН включены[5]:
- Боковой амиотрофический склероз.
- Спинальные мышечные атрофии.
- Первичный латеральный склероз.
- Прогрессирующая мышечная атрофия.
- Болезнь Кеннеди.
- Постполиомиелитический синдром.
Этиология
Современные исследования указывают на генетическую основу развития БДН. Четыре ключевых гена — C9ORF72, TARDBP, SOD1 и FUS — связаны с 70 % случаев семейной формы БАС. Всего же более 25 генов и локусов ассоциированы с предрасположенностью к этому заболеванию. Помимо генетических факторов, важную роль могут играть нарушения регуляции микроРНК и работы ионных каналов, приводящие к эксайтотоксичности. Семейные формы БАС характеризуются неполной пенетрантностью и плейотропным действием генов, тогда как спорадические случаи чаще связаны с олигогенным и полигенным наследованием. Среди экологических факторов риска наиболее убедительные данные имеются в отношении курения и военной службы, тогда как связь с физическими нагрузками и травмами головы остаётся недоказанной. Также изучается потенциальная роль различных токсинов, например, цианотоксинов, в развитии этого заболевания[6].
Патогенез
Повреждение двигательных нейронов развивается из-за сложного комплекса нарушений внутриклеточных процессов, вызванных генетическими мутациями. Эти мутации затрагивают ключевые клеточные механизмы — нарушают белковый гомеостаз (гены SIGMAR1, CHMP2B, C9ORF72), вызывают сбои в метаболизме РНК (гены SETX, FUS, ANG), приводят к митохондриальной дисфункции (гены SOD1, CHCHD10, TARDBP), нарушают везикулярный транспорт (гены SOD1, ALS2, FIG4), ухудшают репарацию ДНК (гены NEK1, C21ORF2, SPG11) и усиливают окислительный стресс (мутации в генах SOD1, ALS2, TARDBP). Особенно критичными считаются нарушения белкового обмена и РНК-метаболизма, которые вместе с нейрональной гиперактивностью и аксональной дисфункцией играют центральную роль в развитии патологии. Эти каскадные нарушения приводят к постепенному отмиранию аксонов двигательных нейронов — сначала аксон теряет способность поддерживать нервные окончания, затем сокращается и полностью отключает иннервацию мышцы. Когда процесс затрагивает нижние двигательные нейроны, это вызывает мышечную денервацию, а при поражении верхних двигательных нейронов приводит к потере супраспинального контроля с развитием гипертонуса и спастичности. Вся эта сложная цепочка молекулярных и клеточных нарушений в конечном итоге проявляется прогрессирующей дегенерацией двигательных нейронов и характерной клинической картиной заболевания[6].
При макроскопическом исследовании патологических образцов выявляются атрофические изменения скелетных мышц и моторной коры, гиалиноз и склероз кортикоспинального и кортикобульбарного трактов, истончение подъязычного нерва и вентральных корешков. Микроскопически в поражённых скелетных мышцах обнаруживаются признаки денервации и реиннервации с формированием групп атрофированных и угловатых мышечных волокон[6].
Эпидемиология
БДН представляет собой распространённое нейродегенеративное заболевание с распространённостью 1—2 случая на 100 000 человек. Заболевание обычно проявляется в позднем среднем возрасте. Примерно 90 % случаев БДН носят спорадический характер, тогда как оставшиеся 10 % являются наследственными[4].
Диагностика
Диагностика БДН основывается на тщательном клиническом осмотре. При оценке мышечной слабости необходимо учитывать следующие параметры: асимметричный или симметричный характер, преимущественное поражение проксимальных или дистальных отделов, преобладание симптомов в верхних или нижних конечностях, наличие или отсутствие бульбарных нарушений[6].
При БАС у 60—80 % пациентов заболевание начинается с поражения конечностей, тогда как у 20—30 % первыми появляются бульбарные симптомы в виде дизартрии и дисфагии (часто сопровождающиеся эмоциональной лабильностью). В редких случаях дебют заболевания проявляется слабостью дыхательной мускулатуры. У части больных первоначально преобладают симптомы поражения верхних мотонейронов (гиперрефлексия и спастическая слабость), а признаки вовлечения нижних мотонейронов (гипотония, фасцикуляции и мышечная атрофия) присоединяются по мере прогрессирования болезни[6].
Первые симптомы обычно возникают асимметрично в дистальных отделах конечностей и могут проявляться затруднениями мелкой моторики, а также нарушениями походки, неустойчивостью и частыми падениями, что приводит к постепенной утрате повседневных навыков. Прогрессирующая дисфагия вызывает снижение потребления пищи и потерю веса. При БАС также отмечается гиперкатаболическое состояние, механизмы развития которого остаются неясными. Развитие дизартрии существенно затрудняет коммуникацию с окружающими[6].
Дыхательная недостаточность может проявляться одышкой, а также головными болями и спутанностью сознания[6].
В этой группе больных также все чаще выявляют поведенческие изменения: апатию, изменения личности и настроения, расторможенность и навязчивые действия. При БАС обычно не наблюдается выраженных вегетативных нарушений, значительно ухудшающих качество жизни, хотя поражение верхних мотонейронов может сопровождаться более серьёзными вегетативными расстройствами[6].
Клинические проявления и естественное течение СМА варьируются в зависимости от фенотипа и классифицируются на несколько типов. Для всех типов СМА характерно сохранение когнитивных функций — пациенты демонстрируют нормальный или выше среднего уровень интеллекта[7]:
- тип 0 (врождённая СМА) проявляется в неонатальном периоде выраженной гипотонией, дыхательной недостаточностью, резкой слабостью и снижением двигательной активности плода с развитием артрогрипоза. Летальный исход обычно наступает при рождении или в течение первого месяца жизни;
- тип I (болезнь Верднига — Гоффмана) дебютирует в первые 6 месяцев жизни отсутствием контроля головы, гипотонией и арефлексией. Характерна «поза лягушки» в положении лёжа, парадоксальное дыхание из-за слабости межрёберных мышц и бочкообразная грудная клетка. Наблюдаются трудности с глотанием, фасцикуляции языка, аспирация и задержка развития. Без респираторной поддержки большинство пациентов не доживают до 2 лет;
- тип II (промежуточная форма) проявляется в 6—18 месяцев — пациенты могут сидеть, но имеют прогрессирующую проксимальную слабость с преимущественным поражением ног, сколиоз, контрактуры суставов и ригидность нижней челюсти. Развивается рестриктивная болезнь лёгких;
- тип III (мягкая форма) начинается после 18 месяцев с проксимальной слабости в ногах. Пациенты сохраняют способность к передвижению, ожидаемая продолжительность жизни не снижается;
- тип IV (взрослая форма) дебютирует после 21 года лёгкой слабостью в ногах с постепенным прогрессированием. Не влияет на продолжительность жизни.
Для ПМА характерно постепенное нарастание признаков поражения нижних мотонейронов. В 20—30 % случаев в течение 5—10 лет от начала заболевания могут появиться и симптомы поражения верхних мотонейронов. Типичные проявления включают прогрессирующий вялый паралич, мышечную атрофию, снижение или отсутствие сухожильных рефлексов, а также фасцикуляции. На момент постановки диагноза обычно наблюдается асимметричная слабость и атрофия дистальных отделов конечностей. Вовлечение аксиальной или дыхательной мускулатуры редко встречается на начальных стадиях. Когнитивные нарушения, связанные с поражением верхних мотонейронов, при ПМА наблюдаются крайне редко[6].
ПЛС обычно проявляется в среднем возрасте около 50 лет — на десятилетие раньше спорадического БАС и на десятилетие позже наследственных спастических параплегий. В 90 % случаев заболевание начинается с постепенного поражения нижних конечностей, пациенты отмечают «потерю плавности» или устойчивости при ходьбе. У остальных 10 % наблюдается бульбарный дебют с дизартрией, гнусавостью голоса и эмоциональной лабильностью. Дисфагия возможна, но редко достигает степени, требующей гастростомии, как при БАС. Необходимость в респираторной поддержке возникает крайне редко. Заболевание медленно прогрессирует с вовлечением верхних конечностей[8].
Неврологический осмотр выявляет только признаки поражения верхних мотонейронов (спастичность, гиперрефлексия) без симптомов повреждения нижних мотонейронов (фасцикуляции, атрофии). Характерна особая картина слабости: в верхних конечностях страдают разгибатели, в нижних — сгибатели, однако жалобы пациентов обычно включают комбинацию повышения тонуса, нарушения координации и умеренной слабости[8].
Хотя при ПЛС обычно наблюдается симметричное поражение ног, существует крайне редкий гемиплегический вариант (синдром Миллса), характеризующийся медленно прогрессирующей восходящей слабостью, начинающейся с дистальных отделов одной ноги. В 30 % случаев возможно последующее вовлечение противоположной стороны. Могут отмечаться лёгкие чувствительные нарушения и бульбарные симптомы. Однако редкость описаний этого варианта вызывает сомнения в его самостоятельности как отдельной нозологической формы[8].
Среди дополнительных неврологических симптомов при ПЛС чаще всего встречаются нарушения мочеиспускания, экстрапирамидные признаки и когнитивные расстройства. Наиболее типичны апатия, дисфункция лобных долей и речевые расстройства. Также могут наблюдаться нарушения движения глаз, особенно плавного слежения[8].
Болезнь Кеннеди (спинально-бульбарная мышечная атрофия) проявляется прогрессирующей мышечной слабостью и атрофией конечностей с преимущественным проксимальным поражением ног (90 % случаев), бульбарными нарушениями (дизартрия, дисфагия у 80 % пациентов, фасцикуляции языка с характерной срединной бороздой), тремором рук, мышечными судорогами и фасцикуляциями. Характерны андрогенные нарушения: гинекомастия, снижение фертильности, атрофия яичек, эректильная дисфункция. У более половины пациентов наблюдаются сенсорные нарушения (парестезии в дистальных отделах), у 40 % — дизурия, у 22 % — обструктивное апноэ сна. Дыхательная недостаточность встречается редко. Отличительные особенности — сохранение сухожильных рефлексов на ранних стадиях и медленное прогрессирование симптомов[9].
Возникает после перенесённого полиомиелита и виремии примерно в 1 % случаев. Полиовирус избирательно размножается и разрушает двигательные нейроны ствола мозга, спинного мозга и моторной коры, вызывая паралитический полиомиелит. Сопутствующие неврологические симптомы включают асимметричную слабость различных мышц, затруднение глотания, миалгии, потерю поверхностных и глубоких сухожильных рефлексов, а также нарушения функции кишечника и мочевого пузыря[10].
Элетронейромиография: помогает оценить характер поражения, выявить демиелинизацию или блок моторной проводимости, а также обнаружить субклинические сенсорные нарушения[11].
Магнитно-резонансная томография головного и спинного мозга: проводится по клиническим показаниям для исключения миелопатии, полирадикулопатий и других структурных поражений центральной нервной системы, которые могут имитировать симптомы БДН. Особое внимание уделяется кортикоспинальным трактам и передним рогам спинного мозга[11].
Молекулярно-генетический анализ[11]:
- генетическое тестирование (включающее панельную диагностику и дополнительный анализ экспансий повторов C9ORF72 с помощью Саузерн-блоттинга для определения длины повторов) проводится только у пациентов с семейным анамнезом (включая деменции и психические расстройства);
- тестирование на мутации в гене андрогенного рецептора и гене SMN1 следует проводить при изолированном поражении нижних мотонейронов, вызывающем клиническое подозрение на спинально-бульбарную мышечную атрофию или спинальную мышечную атрофию.
С целью исключения миастении, паранеопластических синдромов, демиелинизирующих и других аутоиммунных неврологических заболеваний, имитирующих БДН, проводится иммунологический анализ с выявлением: антинуклеарных антител, анти-dsDNA, онконевральных антител, антимиелин-ассоциированного гликопротеина, антител к ацетилхолиновым рецепторам, антитела к мышечно-специфической тирозинкиназе, антитела к потенциал-зависимым калиевым и кальциевым каналам[11].
Дифференциальная диагностика
Дифференциальная диагностика БДН проводится со следующими заболеваниями[6][12]:
- дегенеративная спондилогенная миелорадикулопатия;
- мультифокальная моторная невропатия;
- миастения;
- дефицит гексозаминидазы;
- митохондриальные заболевания;
- синдром Олгрова;
- болезнь Лафора;
- наследственная спастическая параплегия;
- адренолейкодистрофия;
- лучевая миелопатия;
- тиреотоксикоз;
- гиперпаратиреоз;
- отравление свинцом;
- отравление ртутью;
- дефицит меди;
- болезнь Лайма;
- парапротеинемическая невропатия;
- синдром Шегрена;
- полимиозит;
- опухоли спинного мозга;
- пояснично-крестцовые радикулопатии;
- паранеопластические заболевания;
- лимфопролиферативные заболевания;
- неврит плечевого сплетения (синдром Парсонейджа — Тёрнера);
- болезнь Хираямы;
- первично-прогрессирующий рассеянный склероз;
- метаболические миелопатии (B12-дефицитная, медь-дефицитная).
Осложнения
К возможным осложнениям БДН относятся[6]:
- дыхательная недостаточность;
- атрофия дыхательных мышц;
- тяжёлая дисфагия;
- аспирация;
- кожные инфекции;
- пролежни;
- тромбоз глубоких вен.
Лечение
Имеются несколько основных векторов терапии БДН[11]:
- модифицирующая болезнь фармакотерапия: в Европе из этой группы препаратов одобрен только рилузол в качестве модифицирующего болезнь лечения. Он действует как блокатор потенциал-зависимых натриевых каналов и достоверно увеличивает выживаемость;
- неинвазивная вентиляция лёгких может увеличить выживаемость и улучшить качество жизни пациентов с хронической дыхательной недостаточностью на фоне БАС , особенно у пациентов с преимущественно спинальными симптомами. Неинвазивную вентиляцию лёгких следует начинать при появлении симптомов хронической гиповентиляции;
- профилактика пневмонии включает физиотерапию, контроль образования слизи в дыхательных путях, лечение сиалореи;
- сиалорея, возникающая из-за нарушения глотания, требует лечения для предотвращения социальной стигматизации и пневмонии. Варианты лечения включают пирензепин, спрей ипратропия бромида, трансдермальный пластырь со скополамином, амитриптилин, сублингвальное применение 1 % глазных капель атропина, введение ботулотоксина в околоушные и поднижнечелюстные слюнные железы. При резистентной сиалорее может применяться фракционированное облучение слюнных желёз;
- профилактика тромбоза глубоких вен проводится низкомолекулярными гепаринами, а при противопоказаниях — пероральными антикоагулянтами в сниженных дозах;
- лечение дисфагии: проводится посредством установки гастростомы или желудочного зонда.
Прогноз
Большинство пациентов с БАС умирают от дыхательной недостаточности в течение трёх лет с момента появления первых симптомов заболевания. Прогрессирующая слабость и атрофия мышц конечностей и дыхательной мускулатуры являются основными причинами развития дыхательной недостаточности[6].
Примечания
Литература
- Рушкевич Ю. Н., Лихачёв С. А. Современные представленияо болезни двигательного нейрона // Медицинские новости. — 2019. — № 1 (292).
- Рушкевич Ю. Н., Лихачёв С. А. Эпидемиологические характеристики болезни двигательного нейрона // Медицинские новости. — 2018. — № 3 (282).
- Костенко В. В. Характеристика болевого синдрома при болезни двигательного нейрона // Международный неврологический журнал. — 2020. — № 2.