Миастенические синдромы
Миастени́ческие синдро́мы — группа болезней, проявляющихся патологической слабостью и быстрой утомляемостью мышц в результате нарушенной передачи нервных импульсов. Причинами могут быть мутации, эндокринные болезни и опухоли. Распространённость врождённых миастенических синдромов в мире 2,8—14,8 случая на 1 млн населения[1]; синдрома Ламберта — Итона 2-3 случая на 1 млн населения[2]. Для лечения используют ингибиторы ацетилхолинэстеразы, 3,4-диаминопиридин, эфедрин, альбутерол[3], внутривенный иммуноглобулин, иммунодепрессанты, моноклональные антитела, плазмаферез[4].
Что важно знать
Классификация
- D48.9 Новообразование неопределённого или неизвестного характера неуточнённое
- Миастенический синдром при неопластическом заболевании
- E14.4 Неспецифический сахарный диабет с неврологическими осложнениями
- Миастенический синдром при сахарном диабете
- E34.9 Эндокринное расстройство неуточнённое
- Миастенический синдром при эндокринной болезни
- G70.9 Нарушение нервно-мышечного синапса неуточнённое
- G73.0* Миастенические синдромы при эндокринных болезнях
- Миастенические синдромы при диабетической амиотрофии
- Миастенические синдромы при тиреотоксикозе [гипертиреозе]
- G73.1* Синдром Ламберта — Итона
- G73.2* Другие миастенические синдромы при опухолевом поражении
- G73.3* Миастенические синдромы при других болезнях, классифицированных в других рубриках[5][6]
- 2F7Z Новообразования неопределённого характера неуточнённой локализации
- Миастенический синдром при неопластическом заболевании неопределённого характера
- 2F9Z Новообразования неизвестного характера неуточнённой локализации
- Миастенический синдром при неопластическом заболевании неизвестного характера
- 8C61 Врождённые миастенические синдромы
- 8C62 Синдром Ламберта — Итона
- 8C6Y Другие уточнённые Myasthenia gravis или другие определённые болезни нервно-мышечного синапса
- Миастенические синдромы
- Миастенические синдромы при болезнях эндокринной системы
- Миастенические синдромы при гипертиреозе
- Миастенические синдромы при диабетической амиотрофии
- Миастенические синдромы при тиреотоксикозе [гипертиреозе][7]
Этиология
Причины врождённых миастенических синдромов: мутации генов, экспрессируемых в нервно-мышечном соединении. На январь 2023 года зарегистрировано 35 генов: COLQ, CHRN, RAPSN, DOK7, SLC5A7, LAMβ2, AGRN, CHAT[1][8] и др.[3][9] Причины синдрома Ламберта — Итона: опухоли, гаплотип HLA-B8-DR3[4]. К миастеническим синдромам могут приводить эндокринные болезни[7].
Патогенез
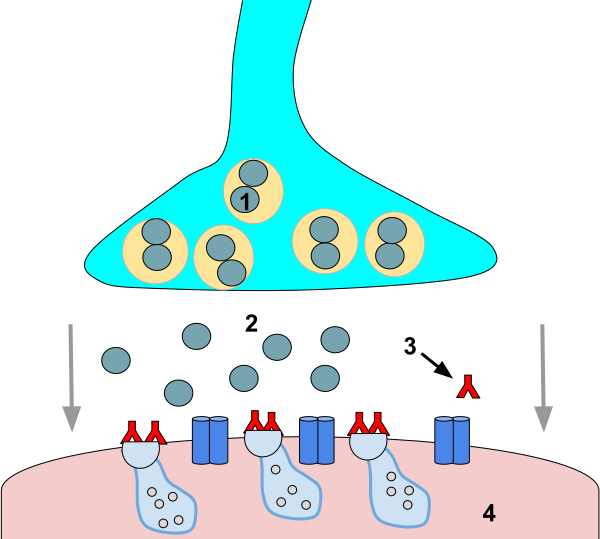
У пациентов с врождённым миастеническим синдромом мутации изменяют структуру белков, участвующих в разных этапах синаптической передачи нервно-мышечных импульсов. Нервно-мышечная передача нарушается уже в раннем эмбриональном периоде и приводит к тяжёлым врождённым миопатиям. Пресинаптическую передачу нарушают мутации генов высокоаффинного натрия (SLC5A7[2]), холинацетилтрансферазы (CHAT); синаптическую — мутации генов коллагенового хвоста ацетилхолинэстеразы (COLQ), β2-цепи ламинина (LAMβ2) и агрина (AGRN); постсинаптическую — мутации генов цитоплазматического белка Dok-7 (DOK7[2]), субъединиц ацетилхолина и рапсина (RAPSN)[1], никотиновых ацетилхолиновых рецепторов (CHRN)[2].
Синдром Ламберта — Итона развивается в результате аутоиммунного нарушения нервно-мышечной передачи. Патогенез связан с аутоантителами к потенциалзависимым кальциевым каналам пресинаптической мембраны нервно-мышечного соединения типа P/Q. Ряд исследователей обнаруживали антитела к N- и L- типу каналов. Кроме специфических аутоантител, выявляются и антитела против слизистой оболочки желудка, ткани щитовидной железы, клеток Пуркинье и других нейрональных структур.
Эпидемиология
Распространённость врождённых миастенических синдромов в мире 2,8—14,8 случая на 1 млн населения. Самый редкий и тяжёлый из них — пресинаптическая врождённая миастения, тип 20, обусловленная мутацией в гене SLC5A7. На 2021 описано 10 генетически подтверждённых случаев[8]. По данным на 2025 год, 85 % врождённых миастенических синдромов связаны мутациями гена RAPSN и DOK7; 10 % случаев связаны мутацией генов COLQ, LAMβ2 или AGRN; 5 % — с мутацией гена CHAT[1]. Распространённость синдрома Ламберта — Итона 2-3 случая на 1 млн населения[2]. Мужчины болеют в 1,5 раза чаще, чем женщины. Возраст больных 14—80 лет. Рак выявляют в 52—75 % случаев (мелкоклеточная карцинома, плоскоклеточный рак бронха, ретиркулосаркома, лейкоз, рак молочной железы, желудка, лёгкого, тимуса, почки). От первых проявлений синдрома до обнаружения опухоли в среднем проходит 3 года[10].
Диагностика
Проявления врождённых миастенических синдромов могут варьировать даже в одной семье. Суточные колебания мышечной силы нехарактерны. У некоторых пациентов не бывает глазных симптомов. Обычно заболевание проявляется в первые 2 года жизни, иногда — сразу после рождения с временным ослаблением до подросткового или взрослого возраста[9]. Пациенты с врождёнными миастеническими синдромами могут не отвечать на введение антихолинэстеразных препаратов. Течение болезни флюктуирующее, клиническая картина напоминает другие болезни, протекающие с мышечной гипотонией, поэтому синдромы часто остаются нераспознанными. Заподозрить болезнь можно по характерным симптомам:
- сниженная подвижность плода;
- задержка моторного развития;
- сила мышц конечностей снижается при физических нагрузках и повышается в покое;
- ослабленное дыхание может требовать респираторной поддержки;
- птоз верхнего века, офтальмоплегия, сходящееся косоглазие;
- бульбарные нарушения (нарушение сосания, глотания, дизартрия), назолалия;
- слабость мимической мускулатуры[8].
Типичные признаки синдрома Ламберта — Итона:
- слабость и утомляемость проксимальных отделов ног и тазового пояса, которые проявляются утиной походкой;
- мышечная слабость верхних конечностей выражена слабо;
- увеличение мышечной силы при выполнении физических нагрузок, из-за чего жалобы на слабость расходятся с результатами тестов мышечной силы;
- пониженные саливация и потоотделение;
- ортостатическая гипотензия;
- парестезии;
- импотенция;
- сухожильные рефлексы отсутствуют или ослаблены;
- глазные симптомы или бульбарные нарушения возникают редко и слабо выражены[10].
Для оценки общего состояния пациентов выполняют:
- молекулярно-генетическое исследование — для определения мутации[8];
- гистологическое исследование биоптатов мышц[10];
- определение антител к рецептору ацетилхолина, мышечно-специфической тирозинкиназе и белку 4[9], родственному рецептору липопротеинов[3];
- определение активности креатинкиназы в сыворотке крови — повышается при мутации в гене GMPPB[3].
Выполняют:
- декремент-тест;
- пробу с физической нагрузкой или тетанизацией мышцы — для диагностики синдрома Ламберта — Итона;
- игольчатую электромиографию;
- исследования проводящей функции нервов[9];
- электромиографию одиночного мышечного волокна — при врождённых миастенических синдромах определяется снижение амплитуды М-ответа при нормальной скорости проведения по нерву[8]; при синдроме Ламберта — Итона определяется низкая амплитуда М-ответа, инкремент амплитуды последующих М-ответов в серии при высокочастотной стимуляции более 200 %, инкремент амплитуды М-ответа в ответ на второй из пары стимулов в межимпульсном интервале от 50 до 20 мс, посттетаническое облегчение более 200 %[10];
- фармакологическую пробу с ингибитором ацетилхолинэстеразы — при некоторых подтипах синдрома врождённой миастении может наблюдаться положительная реакция[3];
- холодовую пробу;
- компьютерную или магнитно-резонансную томографию — для диагностики опухолей[9].
Дифференциальная диагностика
Состояния, от которых необходимо дифференцировать:
- миастения[9];
- полинейропатия;
- полирадикулопатия[4].
Осложнения
Могут развиться: дыхательная недостаточность, апноэ[3], сухость во рту, запор, дисфагия, эректильная дисфункция, потеря массы тела. Повышается риск падений, переломов и аспирационной пневмонии[4].
Лечение
Немедикаментозные методы лечения и реабилитации используют в дополнении к медикаментозному лечению: физиотерапия, трудотерапия, логопедическая терапия, ортопедические приспособления, инвалидное кресло, чрескожная гастростомическая трубка, искусственная вентиляция лёгких[3].
Выбор лекарственного средства зависит от вида миастенического синдрома. Для лечения больных врождёнными синдромами используют ингибиторы ацетилхолинэстеразы, 3,4-диаминопиридин, эфедрин, альбутерол[3]. В случаях синдрома Ламберта — Итона дополнительно применяют внутривенный иммуноглобулин и иммунодепрессанты, моноклональные антитела, плазмаферез[4].
Прогноз
Диспансерное наблюдение
Профилактика
Не разработана.
Примечания
Литература
- Санадзе А. Г. Миастения и миастенические синдромы. — 3-е изд., перераб. и доп. — Москва: ГЭОТАР-Медиа, 2024. — 280 с. — ISBN 978-5-9704-8215-5.
Ссылки
- Всероссийское общество неврологов, Союз реабилитологов России. Миастения. Рубрикатор клинических рекомендаций. Министерство здравоохранения Российской Федерации (15 декабря 2025). Дата обращения: 19 декабря 2025.
- Abicht A., Müller J. S., Lochmüller H. Congenital Myasthenic Syndromes Overview. GeneReviews. University of Washington (23 декабря 2021). Дата обращения: 19 декабря 2025.
| Правообладателем данного материала является АНО «Интернет-энциклопедия «РУВИКИ». Использование данного материала на других сайтах возможно только с согласия АНО «Интернет-энциклопедия «РУВИКИ». |