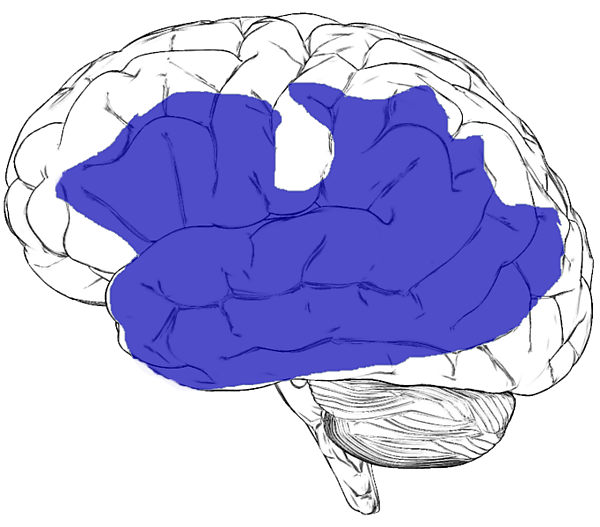
Первичная прогрессирующая афазия
Перви́чная прогрессирующая афазия (ППА) представляет собой гетерогенную группу нейродегенеративных заболеваний, относящихся к фокальным дегенерациям головного мозга. Её ключевым и первоначально изолированным проявлением выступает прогрессирующая утрата речевых функций, включая нарастающий дефицит поиска слов, ухудшение понимания речи и расстройство фразообразования. В течение как минимум двух лет эти языковые нарушения развиваются при относительной сохранности других когнитивных сфер. Заболевание имеет неуклонно прогрессирующий характер, и на поздних стадиях к клинической картине могут присоединяться иные когнитивные, поведенческие и двигательные нарушения. Эффективного лечения ППА не существует[1][2].
Что важно знать
История
Впервые нейродегенеративная афазия была описана Арнольдом Пиком в 1892 году, однако сам термин «первичная прогрессирующая афазия» был предложен лишь в 1987 году для выделения этого состояния в отдельную нозологическую единицу, отличную от болезни Альцгеймера. Изначально заболевание рассматривалось как единый синдром с центральным симптомом в виде аномии, но впоследствии в его структуре были определены три основных клинических варианта. Окончательное закрепление этого разделения произошло в 2011 году с появлением диагностических критериев, подробно описывающих специфические клинические и нейровизуализационные признаки, характерные для каждого из вариантов[2].
Классификация
Выделяют три клинических варианта ППА аграмматический, семантический и логопенический[2].
Этиология
Три варианта первичной ППА вследствие нейродегенеративных изменений в различных областях головного мозга. Семантический и аграмматический варианты чаще связаны с лобно-височной дегенерацией, тогда как логопенический тип по своим патологическим признакам ближе к болезни Альцгеймера. Семантический вариант преимущественно затрагивает передние отделы височной доли. Агрмматический вариант поражает нижнюю лобную извилину и прилегающие области прецентральной коры. Логопенический вариант вовлекает левые задние отделы верхней и средней височных извилин, а также нижнюю теменную дольку. Этиология заболевания различается в зависимости от клинического варианта[3]:
- аграмматический вариант чаще всего связан с патологией тау-белка (4R тау), характерной для лобно-височной дегенерации. В части случаев также обнаруживается патология белка TDP-43 типа А. В редких случаях его причиной могут быть мутации в генах проогранулина или C9orf72, однако проспективные исследования показывают, что генетические мутации редко являются причиной этого варианта. Иногда в основе аграматической ППА может лежать и патология болезни Альцгеймера;
- семантический вариант почти в 75-100 % случаев обусловлен накоплением патологических агрегатов белка TDP-43 типа С. У оставшейся части пациентов он ассоциирован с патологией лобно-височной дегенерации. Семантический вариант наиболее последовательно связан с патологическими изменениями в левой (доминантной) височной доле;
- логопедический вариант: в подавляющем большинстве случаев (до 95 %) причина это болезнь Альцгеймера. Данный вариант признан одним из возможных фокальных и ранних проявлений этого заболевания. Значительно реже в основе могут лежать другие патологии, такие как деменция с тельцами Леви, а также изменения белков TDP-43 и тау.
Определённые нейроразвивающие факторы могут повышать риск развития ППА. Например, у людей с нарушениями развития речи, такими как дислексия, ППА, особенно её логопенический вариант, диагностируется чаще. Это может объясняться общими когнитивными (например, фонологический дефицит) и анатомическими (вовлечение задних отделов теменно-височной коры) особенностями, характерными как для дислексии, так и для логопенической ППА[4].
В научной литературе не выявлено достоверных факторов внешней среды, связанных с риском развития этого заболевания. О роли генетических факторов свидетельствует положительный семейный анамнез нейродегенеративных заболеваний, который отмечается у 20-40 % пациентов с ППА[4].
Патогенез
Патогенез ППА преимущественно связан с тремя основными процессами: накоплением патологических форм тау-белка, агрегацией белка TDP-43 или альцгеймеровской патологией, каждый из которых в разной степени преобладает в различных клинических вариантах заболевания. Одной из ключевых причин нейродегенерации является накопление патологических агрегатов тау-белка. Этот высокорастворимый белок, ассоциированный с микротрубочками, играет важную роль в их стабилизации и полимеризации. Заболевания, в которых тау-патология считается основной причиной нейродегенерации, относят к первичным тауопатиям. Патологические формы тау-белка различаются по количеству консервативных повторов в домене, связывающемся с микротрубочками: выделяют 3R и 4R тау. Мутации в гене MAPT на 17-й хромосоме приводят к образованию аномальных включений тау-белка в клетках, что нарушает их функцию и может провоцировать заболевание[3][5].
Другим частым патологическим субстратом служат отложения белка TDP-43. Выделяют четыре его подтипа (A, B, C, D), некоторые из которых могут быть связаны с генными мутациями. Например, тип A в ряде случаев ассоциирован с мутациями в гене проогранулина, также расположенном на 17-й хромосоме. Эти мутации снижают выработку проогранулина, что способствует формированию нейрональных агрегатов TDP-43. В очень редких случаях к патологии приводит мутация в самом гене TARDBP, кодирующем белок TDP-43[5].
Наконец, у части пациентов, особенно с логопеническим вариантом ППА, в основе заболевания лежит болезнь Альцгеймера. Для неё характерно сочетание внутриклеточных нейрофибриллярных клубков из гиперфосфорилированного тау-белка и внеклеточных амилоидных бляшек, состоящих из бета-амилоида[5].
Эпидемиология
ППА встречается повсеместно, без чёткой географической привязки. Распространённость заболевания оценивается в пределах от 1 до 7 случаев на 100 000 человек, при этом на её долю приходится 0,5-2,5 % всех нейродегенеративных диагнозов. Заболевание манифестирует в среднем в возрасте около 60 лет, обычно в диапазоне от 45 до 70 лет. Средняя продолжительность болезни составляет около 8 лет, но может варьироваться от 4 до 14 лет[4].
Что касается гендерного распределения, данные противоречивы. В то время как одни исследования указывают на преобладание мужчин, другие отмечают равное соотношение или даже преобладание женщин. Существуют исследования, указывающие на то, что соотношение может различаться в зависимости от клинического варианта: мужчины чаще болеют семантическим вариантом, а женщины — аграмматическим. Также отмечается, что после 80 лет заболевание значительно чаще встречается у мужчин[4].
Диагностика
Выделяются три канонических клинико-анатомических варианта ППА[6]:
- аграмматический вариант характеризуется нарушением речевой продукции с артикуляционными и/или грамматическими ошибками;
- семантический вариант проявляется утратой словарного запаса и нарушением знания слов из-за более широкого дефицита семантической памяти;
- логопенический вариант отличается паузами при поиске слов, аномией и нарушением вербальной (фонологической) рабочей памяти, что выражается в непропорциональных трудностях при повторении фраз по сравнению с отдельными словами.
Однако клиническая практика и данные исследований показывают, что до трети случаев не укладываются в критерии одного канонического синдрома. Такие случаи могут описываться как «атипичная», «смешанная» или «неклассифицируемая» ППА. Это может быть связано с фрагментарной или смешанной симптоматикой, наличием выраженных нелингвистических нарушений или динамическим характером болезни, поскольку дефициты при разных синдромах со временем имеют тенденцию сходиться. Внутри каждого синдрома также наблюдается значительная индивидуальная вариабельность по темпу, последовательности и выраженности симптомов, особенно при нефлюентном варианте[6].
Существует подход к дальнейшему разделению синдромов на субсиндромы. Например, внутри аграмматического варианта выделяют первично прогрессирующую апраксию речи, где ведущим является моторно-артикуляционный дефект без изначальных языковых нарушений, и прогрессирующую аграмматическую афазию без апраксии речи. Реже встречается первично прогрессирующая динамическая афазия с изолированным нарушением генерации развёрнутой речи. Для логопенического варианта также описаны субсиндромы с разным соотношением аномии, агрaмматизма и других признаков, при этом этот вариант часто сопровождается нелингвистическими когнитивными проблемами (эпизодическая память, праксис, зрительно-пространственные функции) уже на ранних стадиях, сближаясь с типичной картиной болезни Альцгеймера[6].
В ходе болезни к языковым нарушениям часто присоединяются другие симптомы: при аграмматическом варианте может развиться атипичный паркинсонизм, напоминающий прогрессирующий надъядерный паралич или кортикобазальный синдром; для семантического варианта характерны поведенческие изменения, сходные с поведенческим вариантом лобно-височной дегенерации; а при логопеническом варианте рано проявляются нейропсихиатрические симптомы, такие как тревога. Даже на ранних стадиях возможны более тонкие изменения, например, обеднение чувства юмора или социальная самоизоляция[6].
Пациенты с ППА часто испытывают трудности со слухом в шумной обстановке и хуже понимают акустически деградированную речь, что наиболее выражено при логопеническом и аграмматическом вариантах. Для каждого синдрома описаны и более специфические слуховые дефициты: нарушение восприятия высоты тона, тембра и ритма при аграмматическом варианте; агнозия на звуки окружающей среды и фонагнозия (нарушение узнавания голосов) при семантическом варианте; нарушение восприятия фонем при логопеническом варианте. Встречаются и атипичные случаи с доминированием слуховых нарушений, такие как прогрессирующая словесная глухота. Это позволяет рассматривать синдромы ППА как комплексные расстройства коммуникации, в которых языковой дефицит тесно связан с нарушением обработки сложных звуков[6].
Патологические изменения при магнитно-резонансной томографии отличаются в зависимости от варианта ППА[4]:
- у пациентов с аграмматическим вариантом ППА, как правило, выявляется атрофия и гипометаболизм, в первую очередь затрагивающие доминантную заднюю лобную долю. Эпицентром поражения считается левая нижняя лобная извилина. Также отмечается атрофия серого вещества в островковой коре, премоторных областях, дополнительной моторной зоне и стриатуме. Диффузионно-взвешенная визуализация показывает вовлечение дорсального языкового пути;
- при семантическом варианте ППА определяется атрофия и гипометаболизм в передних отделах височных долей, особенно в височных полюсах. Повреждения обычно более выражены в левом полушарии на ранних стадиях болезни;
- логопенический вариант ППА характеризуется повреждениями, локализованными в задних отделах верхней и средней височных извилин, а также в нижней теменной дольке. Данная картина атрофии соответствует классической анатомической модели фонологической петли и сильно напоминает паттерн, наблюдаемый при болезни Альцгеймера с ранним началом.
Диагностические критерии ППА являются следующими[4]:
- Критерии включения (должны присутствовать все):
- основным клиническим признаком являются трудности с речью и языком (афазия);
- именно языковой дефицит является основной причиной нарушения повседневной активности;
- афазия является ведущим и первичным дефектом в начале заболевания и на его начальных стадиях.
- Критерии исключения (должны отсутствовать все):
- нарушения речи могут быть объяснены не нейродегенеративным заболеванием нервной системы, сосудистым поражением, опухолью или иной медицинской проблемой;
- когнитивные расстройства объясняются психиатрическим заболеванием;
- на первом плане в начальной стадии болезни находятся нарушения эпизодической памяти, зрительного восприятия или зрительно-пространственных функций;
- в начальной стадии болезни доминируют поведенческие расстройства.
Дифференциальная диагностика
Дифференциальная диагностика ППА проводится со следующими заболеваниями[3]:
- болезнь Альцгеймера;
- ишемическая афазия (последствие инсульта);
- опухоль головного мозга;
- лобно-височная деменция.
Осложнения
Осложнения ППА включают[3]:
- развитие депрессии;
- снижение критики и нарушения суждений;
- неадекватное социальное поведение;
- в редких случаях может развиться паркинсонизм, гиперрефлексия или кортикобазальный синдром.
Лечение
Специфического лекарственного лечения для ППА не существует. Занятия с логопедом могут принести значительную пользу. Этот вид терапии считается наиболее эффективным вмешательством при ППА, особенно для уменьшения симптомов апраксии речи[3].
Перспективным направлением для улучшения результатов логопедических занятий считается транскраниальная стимуляция постоянным током. Её высокий профиль безопасности и неинвазивность оправдывают дальнейшие исследования с целью оценки потенциала метода для усиления эффекта поведенческих вмешательств и замедления темпов угасания языковых функций[3].
Прогноз
ППА является неизлечимым прогрессирующим заболеванием, в результате которого пациенты со временем полностью теряют способность говорить, читать и понимать устную речь. Первоначально клиническая картина обычно ограничивается афазическими и апраксическими симптомами, однако по мере прогрессирования болезни (как правило, не ранее чем через 8-12 лет от начала) присоединяются другие когнитивные и поведенческие нарушения. Из-за значительной гетерогенности заболевания точный индивидуальный прогноз установить сложно[3].
Средняя продолжительность жизни после постановки диагноза составляет от 3 до 12 лет. Показатели выживаемости от момента появления симптомов различаются в зависимости от варианта заболевания: при семантическом варианте она составляет в среднем 12 лет, а при логопеническом варианте — 7.6 лет. Наиболее частой непосредственной причиной смерти является аспирационная пневмония[3].
Диспансерное наблюдение
Профилактика
Не разработана.
Примечания
Литература
- Belder C. R. S., Marshall C. R., Jiang J. et al. Primary progressive aphasia: six questions in search of an answer (англ.) // Journal of Neurology. — 2024. — Vol. 271. — P. 1028—1046. — doi:10.1007/s00415-023-12030-4.
- Ortiz G. G., González-Usigli H., Nava-Escobar E. R. et al. Primary Progressive Aphasias: Diagnosis and Treatment (англ.) // Brain Sciences. — 2025. — Vol. 15, no. 3. — P. 245. — doi:10.3390/brainsci15030245.
- Ахмадуллина Д. Р., Федотова Е. Ю. Первичная прогрессирующая афазия: варианты и основные речевые домены // Анналы клинической и экспериментальной неврологии. — 2024. — Т. 18, № 4. — С. 68—75. — doi:10.17816/ACEN.1067.
- Михайлов В. А., Коцюбинская Ю. В., Сафонова Н. Ю., и др. Первичная прогрессирующая афазия // Неврология, нейропсихиатрия, психосоматика. — 2019. — № 1. — С. 4—11.