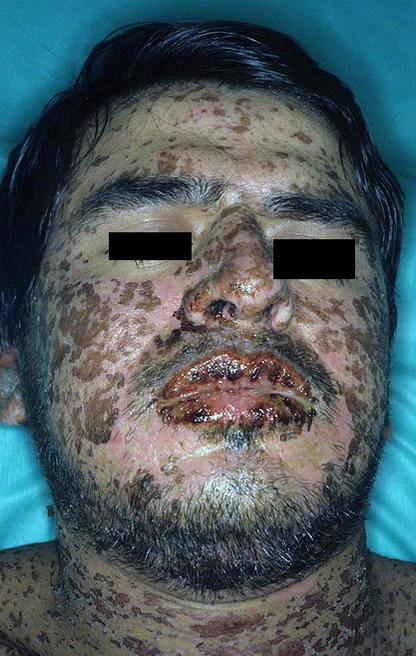
Синдром Стивенса — Джонсона
Синдро́м Сти́венса — Джо́нсона (англ. Stevens — Johnson syndrome) — тяжёлая острая токсико-аллергическая реакция гиперчувствительности, характеризующаяся поражением кожи и слизистых оболочек с развитием буллёзно-эрозивных изменений. Заболевание относится к группе тяжёлых системных аллергических реакций замедленного типа и сопровождается выраженными нарушениями общего состояния. В большинстве случаев синдром развивается на фоне приёма лекарственных препаратов, реже — в связи с инфекционными агентами. Клиническое течение синдрома Стивенса — Джонсона отличается острым началом и быстрым прогрессированием. Заболевание сопровождается лихорадкой, выраженной интоксикацией, поражением кожи и слизистых оболочек не менее чем двух анатомических областей. Характерным является развитие множественных полиморфных высыпаний с образованием пузырей, эрозий и участков отслойки эпидермиса, а также тяжёлое поражение слизистых оболочек полости рта, глаз, половых органов и других анатомических зон. Синдром может развиваться в любом возрасте, однако чаще наблюдается у взрослых, преимущественно у лиц старше 40 лет, а также у пациентов с иммунодефицитными и онкологическими заболеваниями. Заболевание сопровождается значительным риском летального исхода, особенно при обширном поражении кожи и слизистых оболочек. Существенное значение имеют ранняя диагностика и своевременное начало терапии, поскольку задержка в установлении диагноза напрямую связана с ухудшением прогноза.
Что важно знать
История
Синдром Стивенса — Джонсона длительное время рассматривался как одно из тяжёлых проявлений многоформной экссудативной эритемы. Первое описание многоформной эритемы было представлено Фердинандом фон Геброй в 1866 году. В 1922 году американские врачи Альберт Мейсон Стивенс и Фрэнк Чамблисс Джонсон опубликовали наблюдение двух клинических случаев у подростков, характеризовавшихся генерализованной сыпью, сохраняющейся лихорадкой, поражением слизистой оболочки полости рта и тяжёлым гнойным конъюнктивитом. Первоначально данные случаи были ошибочно расценены как геморрагическая форма кори. Авторы обратили внимание на ряд особенностей клинической картины, отличавших её от многоформной эритемы, включая характер кожных высыпаний, отсутствие субъективных ощущений, длительное течение лихорадки и выраженное поражение слизистых оболочек. Несмотря на выявленную лейкопению, в ранних наблюдениях предполагалась инфекционная природа заболевания неустановленной этиологии. В 1950 году Томас предложил классификацию многоформной эритемы, выделив её малую и большую формы. В течение последующих десятилетий синдром Стивенса — Джонсона рассматривался как синоним тяжёлой формы многоформной эритемы. Пересмотр представлений о природе заболевания произошёл в 1990-е годы, когда Бастюи и Ружо показали, что эритема многоформная и синдром Стивенса — Джонсона являются самостоятельными нозологическими формами. Было предложено ограничить термин «многоформная эритема» случаями с типичными мишеневидными элементами или отёчными папулами с возможным поражением слизистых оболочек, что соответствовало первоначальному описанию фон Гебры. В 1956 году А. Лайелл описал пациентов с обширным отслоением эпидермиса, клинически напоминающим ожог кожи, и ввёл термин «токсический эпидермальный некролиз». В дальнейшем, на основании анализа накопленных клинических данных, в 1993 году экспертной группой были сформулированы диагностические критерии, согласно которым синдром Стивенса — Джонсона и токсический эпидермальный некролиз были объединены в единый патологический спектр, различающийся по степени тяжести поражения кожи и слизистых оболочек[2][3].
Классификация
Классификация синдрома Стивенса — Джонсона и токсического эпидермального некролиза основана на площади отслоения эпидермиса по отношению к общей поверхности тела пациента, а также на характере кожных высыпаний[2].
В соответствии с современными представлениями выделяют следующие клинические формы синдрома Стивенса — Джонсона — токсического эпидермального некролиза[2][3]:
- синдром Стивенса — Джонсона, при котором площадь отслоения эпидермиса составляет не более 10 % поверхности тела;
- переходная (перекрёстная) форма синдрома Стивенса — Джонсона — токсического эпидермального некролиза, характеризующаяся поражением кожи в пределах 10—30 % поверхности тела;
- токсический эпидермальный некролиз, сопровождающийся массивным отслоением эпидермиса с поражением более 30 % поверхности тела.
Данная классификация используется для определения степени тяжести заболевания, оценки прогноза и выбора тактики ведения пациентов[2].
Этиология
Синдром Стивенса — Джонсона чаще всего развивается на фоне приёма лекарственных препаратов, однако в части случаев причинный фактор установить не удаётся, и заболевание расценивают как идиопатическое. Описано более 100 лекарственных средств различных фармакологических групп, ассоциированных с развитием синдрома. К числу наиболее часто упоминаемых относятся противосудорожные препараты, включая карбамазепин и фенобарбитал, противоподагрические средства, прежде всего аллопуринол, сульфаниламиды, антибиотики, включая пенициллины, цефалоспорины, фторхинолоны и карбапенемы, нестероидные противовоспалительные средства, в том числе пироксикам, а также антиретровирусные препараты, применяемые при ВИЧ-инфекции[4]. В качестве возможных триггеров также описаны вакцины, парацетамол, витамины и другие средства, влияющие на метаболизм, местные анестетики, барбитураты, противоэпилептические препараты и героин[2][5].
Помимо лекарственных факторов, значимую роль могут играть инфекционные агенты. В качестве возможных причин указаны вирусы простого герпеса 1-го и 2-го типов, аденовирус, цитомегаловирус, энтеровирусы, вирус Эпштейна — Барр, вирусы гепатита A и B, кори, ветряной оспы, гриппа, паротита, полиовирус и ВИЧ. Среди бактериальных агентов упоминаются микоплазмы, риккетсии, возбудитель пситтакоза, туберкулёзная палочка, протеи, сальмонелла, возбудитель туляремии, гонококк, бруцелла, иерсиния, бета-гемолитический стрептококк группы A, дифтерийная палочка, микобактерии. Также обнаруживаются возбудители грибковых и протозойных инфекций. Более чем в половине случаев заболевание развивается на фоне инфекций верхних дыхательных путей[2][5].
Риск развития синдрома повышают аутоиммунные и онкологические заболевания, ВИЧ-инфицирование и семейные случаи заболевания, что связывают с генетической предрасположенностью, включая различные типы HLA[6]. Удельный вклад причинных факторов отличается в разных возрастных группах: у детей чаще имеет значение инфекция, у взрослых — лекарственные средства и новообразования. Для лекарственно-индуцированных форм характерен латентный интервал между началом приёма препарата и появлением клинических проявлений, который обычно составляет от 4 до 28 дней и может достигать 2—8 недель. После 8 недель терапии риск развития синдрома считается несущественным[2].
Патогенез
Патогенез синдрома Стивенса — Джонсона связан с массивной гибелью базальных кератиноцитов кожи и эпителия слизистых оболочек, что приводит к отслойке эпидермиса от дермы и формированию буллёзно-эрозивных поражений. Заболевание рассматривается как иммунопатологическая реакция гиперчувствительности замедленного типа, опосредованная Т-лимфоцитами, с ведущей ролью цитотоксических CD8+клеток. В патологический процесс также вовлекаются натуральные киллеры. Активация Т-клеточного звена развивается в ответ на воздействие лекарственного препарата или инфекционного агента и сопровождается выраженной цитотоксической реакцией[7].
Гибель кератиноцитов реализуется преимущественно через Fas-опосредованный путь апоптоза и перфорин/гранзим-зависимый механизм. Существенную роль играет взаимодействие Fas-рецептора с Fas-лигандом, а также участие фактора некроза опухоли альфа, который способен индуцировать апоптоз как напрямую, так и через активацию цитотоксических Т-лимфоцитов[5][6]. Важным медиатором повреждения считается гранулизин — цитотоксический белок, высвобождаемый Т-киллерами. Установлено, что его концентрация в содержимом пузырей коррелирует с тяжестью заболевания, что позволяет рассматривать гранулизин как один из ключевых эффекторов апоптоза. Массовая гибель кератиноцитов поддерживает воспалительную реакцию и обусловливает прогрессирование кожно-слизистых поражений[4][7].
Формирование иммунного ответа, приводящего к развитию синдрома, объясняется несколькими патогенетическими концепциями. Согласно гипотезе гаптен/прогаптен, лекарственное вещество ковалентно связывается с белками сыворотки крови, образуя иммуногенный комплекс, который распознаётся системой HLA и презентируется Т-лимфоцитам. В рамках концепции фармакологического взаимодействия предполагается прямое связывание препарата с молекулами HLA без предварительного ковалентного соединения с белками, что также приводит к активации Т-клеток. Теория «изменённого пептида» предполагает, что лекарственное средство изменяет представление собственных пептидов в комплексе с HLA, вследствие чего они распознаются иммунной системой как чужеродные[3][8].
Установлена роль генетической предрасположенности, связанной с определёнными аллелями HLA, в частности HLA-B, которые ассоциированы с повышенным риском развития синдрома при воздействии триггерных факторов. Совокупность иммунных, генетических и клеточных механизмов приводит к неконтролируемому апоптозу кератиноцитов, лежащему в основе клинических проявлений синдрома Стивенса — Джонсона[3][9].
Эпидемиология
Синдром Стивенса — Джонсона относится к редким заболеваниям. Заболеваемость составляет в среднем от 1 до 6 случаев на 1 миллион населения в год. Заболевание может развиваться в любом возрасте. Описаны случаи у детей, взрослых и лиц пожилого возраста. Вместе с тем риск его развития возрастает с увеличением возраста. Средний возраст дебюта составляет от 40 до 50 лет. У детей синдром встречается реже, однако для этой возрастной группы характерна более высокая склонность к рецидивированию. Летальность, напротив, выше среди пациентов старших возрастных групп. Синдром Стивенса — Джонсона наблюдается у лиц обоего пола, при этом отмечается умеренное преобладание женщин. Заболевание регистрируется во всех этнических группах, однако более высокая распространённость отмечена среди лиц азиатского происхождения. Существенное увеличение риска развития синдрома выявлено у ВИЧ-инфицированных пациентов, у которых заболеваемость в сотни раз превышает показатели общей популяции. Повышенная частота также характерна для больных системной красной волчанкой, онкологическими заболеваниями и другими состояниями, сопровождающимися нарушением иммунной регуляции. Отмечается сезонность заболевания с увеличением числа случаев в зимний и ранневесенний периоды, что может указывать на роль инфекционных факторов в реализации патологического процесса[10]. Летальность при синдроме Стивенса — Джонсона составляет в среднем 5—12 % и возрастает в пожилом возрасте, при наличии сопутствующих заболеваний и значительной площади поражения кожных покровов[3][6].
Диагностика
Клиническая картина синдрома Стивенса — Джонсона характеризуется острым началом с продромальным периодом, напоминающим инфекцию верхних дыхательных путей. От одного дня до нескольких недель отмечаются фебрильная лихорадка, озноб, недомогание, головная боль, боли в горле, миалгии и артралгии. На этом фоне кожные и слизистые поражения возникают внезапно и прогрессируют стремительно[5][11].
Кожные проявления представлены множественными полиморфными высыпаниями. Сначала появляются багрово-красные пятна с синюшным оттенком, затем элементы приобретают папулёзный, везикулёзный и буллёзный характер. Характерным признаком являются плоские атипичные мишеневидные элементы, в которых центральная зона может быть представлена пузырьком, геморрагиями или некрозом, а периферическая — пятнистой эритемой. Высыпания могут возникать волнообразно, с интервалом в несколько дней, и сохраняться в течение нескольких недель. Поражение чаще локализуется на коже туловища, лица и дистальных отделов конечностей, также могут вовлекаться ладони и подошвы, разгибательные поверхности конечностей и межпальцевые промежутки. В течение нескольких часов на фоне пятен формируются крупные пузыри, которые могут достигать значительных размеров и сливаться. Покрышки пузырей легко разрушаются вследствие отслоения эпидермиса, что соответствует положительному симптому Никольского. После вскрытия пузырей образуются обширные ярко-красные резко болезненные эрозированные мокнущие поверхности, окаймлённые обрывками покрышек. Поражённая кожа предрасположена к инфицированию. На ладонях и стопах могут появляться округлые тёмно-красные пятна с геморрагическим компонентом[6]. В зоне высыпаний отмечаются зуд или жжение, при этом одной из основных жалоб в период манифестации является выраженная генерализованная боль, связанная с поражением кожи[5][4].
Поражение слизистых оболочек является обязательным и по тяжести часто выходит на первый план. Поражение слизистой оболочки полости рта проявляется разлитой эритемой, отёком, пузырями и быстро формирующимися обширными эрозиями, покрытыми желтовато-серым или сероватым фибринозным налётом. Губы и дёсны становятся опухшими, болезненными и кровоточащими. На красной кайме губ формируются толстые буро-коричневые геморрагические корки, при удалении налётов и корок слизистая легко кровоточит. Из-за выраженной болезненности пациенты часто отказываются от приёма пищи и жидкости, отмечают боль и жжение, повышенную чувствительность при глотании, затруднение артикуляции[4][5].
Поражение глаз наблюдается часто и может проявляться блефароконъюнктивитом, тяжёлым катаральным или гнойным конъюнктивитом с развитием пузырьков и эрозий. Отмечается риск изъязвления и рубцовых изменений роговицы, а также увеита. Пациенты предъявляют жалобы на светобоязнь и выраженный дискомфорт[5][6].
Поражение мочеполовой системы встречается более чем у половины больных и проявляется эрозивными изменениями слизистых оболочек с развитием баланита, уретрита и вульвовагинита. Возможны жалобы на болезненное мочеиспускание. Также описано поражение перианальной области и слизистой оболочки заднего прохода с формированием болезненных эрозий. Тяжесть и обширность поражений часто определяется преимущественно эрозивным процессом на слизистых оболочках, особенно в области естественных выходных отверстий[6][4].
Лабораторные исследования используются для оценки общего состояния пациента, выявления осложнений, мониторинга течения заболевания и подбора терапии[10].
В общем анализе крови могут выявляться изменения неспецифического характера. Возможны анемия, снижение количества лимфоцитов, реже — эозинофилия. Выраженная нейтропения рассматривается как неблагоприятный прогностический признак. При присоединении вторичной инфекции отмечается увеличение количества лейкоцитов. В биохимическом анализе крови определяют концентрацию глюкозы, мочевины, креатинина, общего белка, билирубина, активность аминотрансфераз (АЛТ, АСТ), концентрацию С-реактивного белка, показатели кислотно-щелочного состояния. Эти параметры используются для оценки тяжести состояния, функции внутренних органов и контроля проводимой терапии. Исследование функции почек включает также общий анализ мочи с оценкой наличия белка и форменных элементов. При тяжёлом течении возможно выявление признаков нарушения канальцевой функции[6][7].
Микробиологическое исследование проводится при подозрении на инфекционные осложнения. Выполняют микробиологическое исследование отделяемого кожных элементов и слизистых оболочек с определением чувствительности выявленных микроорганизмов к антибактериальным и противогрибковым препаратам. Материал рекомендуется забирать не менее чем с трёх участков поражённой кожи. По показаниям выполняют микробиологическое исследование мочи, мокроты и отделяемого слизистых оболочек[6][10].
Гистологическое исследование биопсийного материала кожи применяется в сложных диагностических случаях. В биоптатах выявляются тотальный некроз кератиноцитов, образование щели над базальной мембраной, субэпидермальное расслоение, вакуольная дегенерация в глубоких слоях эпидермиса и минимальная воспалительная инфильтрация дермы. В инфильтрате преобладают лимфоциты, могут присутствовать макрофаги и дендритные клетки[6]. Прямая иммунофлуоресценция обычно отрицательная, что позволяет исключить аутоиммунные буллёзные дерматозы[7][8].
Инструментальные методы исследования применяются по показаниям и направлены на выявление поражения внутренних органов и осложнений заболевания. Рентгенография органов грудной клетки выполняется при подозрении на поражение дыхательной системы и позволяет выявить признаки пневмонита или иных воспалительных изменений. Бронхоскопия проводится при клинических признаках поражения дыхательных путей с целью оценки состояния слизистой оболочки и выявления участков десквамации[3][7].
Эзофагогастродуоденоскопия и колоноскопия применяются при подозрении на поражение слизистой оболочки желудочно-кишечного тракта. Офтальмологическое обследование является обязательным при вовлечении органов зрения и включает осмотр в щелевой лампе с оценкой состояния конъюнктивы и роговицы, выявлением эрозий, язвенных дефектов и рубцовых изменений. В отдельных случаях для динамического наблюдения может применяться конфокальная микроскопия[3][7].
Дифференциальная диагностика
Дифференциальную диагностику синдрома Стивенса — Джонсона следует проводить со следующими заболеваниями[3][7][12]:
- острый генерализованный экзантематозный пустулёз;
- синдром лекарственной гиперчувствительности;
- многоформная экссудативная эритема;
- стафилококковый синдром ошпаренной кожи;
- вульгарная пузырчатка;
- листовидная пузырчатка;
- острая реакция «трансплантат против хозяина»;
- подострый лучевой дерматит;
- прогрессирующая системная склеродермия;
- врождённая ихтиозиформная эритродермия;
- поздняя кожная порфирия;
- приобретённый буллёзный эпидермолиз;
- линейный IgA-зависимый буллёзный дерматоз;
- паранеопластическая пузырчатка;
- буллёзная форма системной красной волчанки;
- конъюнктивит, вызванный Corynebacterium diphtheriae;
- карцинома сальных желёз;
- аденовирусный конъюнктивит;
- интраэпителиальная эпителиома;
- атопический кератоконъюнктивит;
- химические ожоги;
- эксфолиативный дерматит;
- ожоги глаз и химические повреждения;
- синдром Шёгрена;
- синдром токсического шока;
- трахома;
- вирусная экзантема;
- геморрагический васкулит;
- узелковый полиартериит;
- лихеноидный парапсориаз;
- микроскопический полиартериит;
- болезнь Кавасаки[13];
- тяжёлый энтеровирусный везикулярный фарингит[13];
- острый герпетический гингивостоматит[13];
- тяжёлый афтозный стоматит[13].
Осложнения
Осложнения синдрома Стивенса — Джонсона формируются как в остром периоде заболевания, так и в отдалённые сроки, и в значительной степени определяют прогноз и качество жизни пациентов. В острой фазе наибольшую опасность представляют инфекционные осложнения, обусловленные обширным повреждением кожного покрова и слизистых оболочек. Нарушение барьерной функции кожи способствует быстрому присоединению бактериальной инфекции с развитием сепсиса, который является одной из ведущих причин летального исхода. Возможны поражения дыхательной системы с развитием пневмонии, дыхательной недостаточности и бронхообструктивных нарушений, а также поражение почек и печени с формированием полиорганной недостаточности[3][7].
В отдалённом периоде наиболее часто развиваются офтальмологические осложнения. К ним относятся хронический кератоконъюнктивит, синдром сухого глаза, рубцовые изменения конъюнктивы, симблефарон, трихиаз, неоваскуляризация роговицы и стойкое снижение зрения вплоть до слепоты. Со стороны кожных покровов могут сохраняться участки гипопигментации и гиперпигментации, рубцовые изменения, нарушение роста волос и ногтей. Поражение слизистых оболочек может приводить к формированию стриктур пищевода, рубцовым изменениям половых органов и стойким расстройствам мочеиспускания[7]. У части пациентов отмечаются хронический болевой синдром, астенизация и психоэмоциональные нарушения[3].
Лечение
Лечение синдрома Стивенса — Джонсона проводится исключительно в условиях стационара и требует междисциплинарного подхода с участием дерматовенерологов, реаниматологов, офтальмологов, хирургов, а при необходимости — инфекционистов, пульмонологов, нефрологов и других специалистов. В зависимости от площади поражения кожи и тяжести состояния пациенты госпитализируются в отделения интенсивной терапии или ожоговые центры. Тактика ведения во многом соответствует принципам лечения больных с обширными ожогами[7][13].
Решение о назначении системной терапии принимается с учётом вероятности прогрессирования заболевания, так как на ранних стадиях невозможно точно предсказать максимальную площадь отслойки эпидермиса. В связи с этим всех пациентов следует рассматривать как потенциально подверженных развитию токсического эпидермального некролиза. Терапию необходимо начинать немедленно после установления диагноза с обязательным учётом сопутствующих заболеваний и возможных лекарственных взаимодействий. При отсутствии признаков прогрессирования кожного процесса или поражения слизистых оболочек в течение более 24 часов ожидаемая польза от назначения новой системной терапии должна быть критически оценена. Под прогрессированием понимают дальнейшее распространение эритемы с возможным образованием пузырей и отслойкой эпидермиса. Появление новых пузырей на уже гиперемированных участках не всегда расценивается как прогрессирование. Для объективной оценки динамики рекомендуется маркировать границы эритемы и проводить регулярную фотодокументацию[13].
Ключевым и первоочередным этапом терапии является немедленная отмена предполагаемого причинно-значимого лекарственного препарата. Своевременное прекращение его приёма оказывает существенное влияние на прогноз и снижает риск прогрессирования заболевания. В сомнительных случаях отменяются все препараты, не являющиеся жизненно необходимыми, особенно если их приём был начат в течение предшествующих недель. Основу лечения составляет поддерживающая терапия, направленная на стабилизацию жизненно важных функций, коррекцию водно-электролитных нарушений, профилактику инфекционных осложнений и создание условий для репарации кожи и слизистых оболочек. Применяется инфузионная терапия с использованием растворов натрия хлорида, а также комбинированных электролитных растворов, содержащих калий и магний. Потребность в жидкости у пациентов с синдромом Стивенса — Джонсона, как правило, ниже, чем у больных с термическими ожогами аналогичной площади поражения[6]. Пациенты размещаются в условиях строгой асептики с поддержанием повышенной температуры окружающей среды, которая поддерживается на уровне 30—32 °C[10]. Это позволяет снизить теплопотери, уменьшить метаболический стресс и улучшить условия для заживления кожных покровов[3][8].
Уход за кожей и слизистыми оболочками является важнейшим элементом лечения. Поражённые участки обрабатываются щадящими антисептическими растворами с исключением агрессивного механического воздействия. Предпочтение отдаётся неадгезивным повязкам, в том числе материалам с ионами серебра или вазелиновой пропиткой, что позволяет уменьшить болевой синдром и снизить риск вторичного инфицирования. Используются водный раствор перекиси водорода, раствор хлоргексидина, а также раствор перманганата калия. При лечении детей допускается применение анилиновых красителей, не содержащих спирт, в частности водного раствора бриллиантового зелёного. При колонизации грамотрицательной флорой более уместны йодсодержащие антисептики. Местные антибактериальные препараты и средства для очищения ран с антибиотиками следует избегать, поскольку они могут нарушать баланс флоры кожи и способствовать оппортунистическим инфекциям, включая кандидоз. Отслоившийся эпидермис не удаляют, поскольку он выполняет защитную функцию и способствует реэпителизации. Обработка проводится регулярно с обязательным соблюдением стерильности. При поражении слизистой оболочки полости рта осуществляется бережный уход с применением антисептических растворов и местных анестетиков. На губы несколько раз в сутки наносят белый вазелин или мазь с декспантенолом, при выраженных эрозиях дополнительно используют неадгезивные раневые повязки. Полость рта обрабатывают безспиртовыми антисептическими растворами, особенно после приёма пищи, а перед едой при необходимости применяют местные анестетики. Поражение глаз требует обязательного наблюдения офтальмолога и включает регулярное применение увлажняющих и противовоспалительных средств. В отдельных случаях используются местные иммуномодулирующие препараты. Назначение антибактериальных глазных капель не рекомендуется ввиду риска усугубления синдрома сухого глаза[6][14].
Обезболивающая терапия подбирается индивидуально с учётом выраженности болевого синдрома. При необходимости применяются сильнодействующие анальгетики. Использование нестероидных противовоспалительных препаратов не рекомендуется в связи с их возможной ролью в патогенезе заболевания[15].
Системная терапия включает глюкокортикоиды, внутривенные иммуноглобулины и иммунодепрессанты. Применение системных глюкокортикоидов способно уменьшать выраженность воспалительной реакции, однако сопровождается риском инфекционных осложнений. Наибольшая эффективность отмечается при раннем и кратковременном применении[2]. Внутривенные иммуноглобулины применяются в высоких дозах в первые дни заболевания и способны снижать летальность[7]. Циклоспорин рассматривается как возможный вариант терапии, однако его назначение требует индивидуальной оценки соотношения пользы и риска[6][13].
Антибактериальная терапия не применяется профилактически и показана только при развитии вторичной бактериальной инфекции или признаках сепсиса. Выбор антибактериального препарата осуществляется с учётом результатов микробиологического исследования и клинической картины[8]. При выраженном поражении дыхательных путей может потребоваться респираторная поддержка, включая интубацию и искусственную вентиляцию лёгких. При поражении слизистых оболочек половых органов и формировании синехий показана консультация хирурга или акушера-гинеколога с последующим решением вопроса о хирургической коррекции[6][14].
Назначение системной иммуномодулирующей терапии во время беременности требует особенно взвешенной оценки соотношения пользы и риска. Дети и подростки лечатся по тем же принципам, что и взрослые пациенты[13].
Прогноз
Прогноз при синдроме Стивенса — Джонсона определяется объёмом поражения кожных покровов, выраженностью системных нарушений и своевременностью начала медицинской помощи. Заболевание относится к потенциально жизнеугрожающим состояниям, при которых вероятность летального исхода прямо связана с площадью отслойки эпидермиса и тяжестью общего состояния пациента[3].
Летальность при синдроме Стивенса — Джонсона в среднем составляет 4—5 %, при переходных формах между синдромом Стивенса — Джонсона и токсическим эпидермальным некролизом она возрастает до 15—20 %. У пациентов с поражением более 30 % поверхности тела риск летального исхода может превышать 30—50 %[7][16].
К неблагоприятным прогностическим факторам относятся[3][16]:
- возраст старше 40 лет;
- наличие злокачественных новообразований;
- обширное поражение кожи (более 10 % поверхности тела);
- почечная недостаточность;
- гипергликемия;
- гипоальбуминемия;
- стойкая нейтропения;
- присоединение бактериальной инфекции и развитие сепсиса.
Для объективной оценки прогноза используется шкала SCORTEN, включающая возраст пациента, наличие злокачественного процесса, частоту сердечных сокращений, площадь поражения кожи, концентрацию мочевины, глюкозы и бикарбонатов в сыворотке крови. Увеличение суммарного балла по шкале сопровождается значительным ростом вероятности летального исхода. Дополнительно применяется прогностическая шкала ABCD-10, позволяющая уточнить риск неблагоприятного течения заболевания[16][8].
При своевременной диагностике и адекватной поддерживающей терапии возможно полное заживление кожных поражений в течение 2—3 недель. Однако даже при благоприятном исходе сохраняется риск развития отдалённых осложнений, что требует длительного наблюдения пациентов после перенесённого заболевания[3].
Диспансерное наблюдение
Пациенты, перенёсшие синдром Стивенса — Джонсона, подлежат длительному диспансерному наблюдению. Контроль осуществляется с целью раннего выявления поздних осложнений, оценки функционального состояния органов-мишеней и профилактики рецидивов. Наблюдение должно включать регулярную оценку состояния кожи и слизистых оболочек, офтальмологическое обследование, контроль функции почек и печени, а также мониторинг лабораторных показателей воспаления[7][10].
Особое значение имеет динамическое наблюдение пациентов с поражением глаз, поскольку офтальмологические осложнения могут прогрессировать даже спустя месяцы после перенесённого заболевания. При наличии рубцовых изменений слизистых оболочек требуется наблюдение соответствующих специалистов. Пациентам рекомендуется избегать самолечения и бесконтрольного приёма медикаментов, а также своевременно обращаться за медицинской помощью при появлении любых новых симптомов[7][10].
Профилактика
Профилактика синдрома Стивенса — Джонсона направлена прежде всего на предотвращение повторного воздействия причинно-значимого лекарственного препарата. После перенесённого эпизода заболевания пациенту необходимо пожизненное исключение препарата, вызвавшего развитие синдрома, а также лекарственных средств со сходной химической структурой в связи с высоким риском перекрёстных реакций. Сведения о перенесённом синдроме должны быть обязательно зафиксированы в медицинской документации и доведены до сведения пациента[6].
Рекомендуется информирование пациента о необходимости постоянного контроля при назначении любых лекарственных средств, а также ношение медицинского опознавательного браслета или карточки с указанием диагноза и потенциально опасных препаратов[6]. При назначении новой терапии требуется тщательная оценка соотношения пользы и риска с учётом анамнеза. Особое внимание должно уделяться пациентам с онкологическими заболеваниями, иммунодефицитными состояниями и лицам пожилого возраста, поскольку у данной категории риск развития тяжёлых форм синдрома и неблагоприятного течения выше[7][10].
Примечания
Ссылки
- Research Directions in Genetically-Mediated Stevens-Johnson Syndrome/Toxic Epidermal Necrolysis (англ.) (Архивная копия)