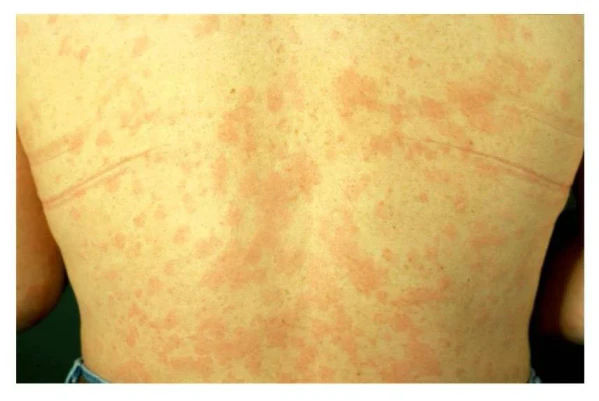
Синдром Шницлер
Синдро́м Шни́цлер (англ. Schnitzler syndrome; хрони́ческая крапи́вница с макроглобулинеми́ей) — редкое аутовоспалительное заболевание, характеризующееся сочетанием хронической рецидивирующей уртикарной сыпи и моноклональной гаммапатии, преимущественно класса IgM. Заболевание сопровождается признаками системного воспаления и ассоциировано с риском развития лимфопролиферативных заболеваний и AA-амилоидоза. Клиническая картина синдрома Шницлер включает рецидивирующие уртикарные высыпания, интермиттирующую лихорадку, боли в костях, мышцах и суставах, лимфаденопатию, гепатомегалию и спленомегалию, а также стойкое повышение показателей воспалительной активности. Моноклональная гаммапатия является характерным лабораторным признаком и может выявляться как одновременно с кожными проявлениями, так и спустя годы после дебюта заболевания. Для синдрома типично позднее начало и хроническое течение без спонтанных ремиссий. В его патогенезе ключевую роль играет активация инфламмасомы и интерлейкин-1-опосредованного воспалительного каскада, что подтверждается высокой эффективностью ингибиторов интерлейкина-1. Несмотря на относительно благоприятное течение у большинства пациентов, синдром Шницлер ассоциирован с риском развития лимфопролиферативных осложнений, что определяет необходимость своевременной диагностики и длительного динамического наблюдения.
Общие сведения
История
История изучения синдрома Шницлер началась в 1972 году, когда французский дерматолог Лилиан Шницлер впервые описала данный клинический феномен. Первоначально заболевание было представлено как сочетание хронической рецидивирующей крапивницы и моноклональной гаммапатии. В 1974 году Шницлер опубликовала дополнительные клинические наблюдения, позволившие более чётко охарактеризовать данное состояние и выделить его в самостоятельную нозологическую форму[2][3].
В дальнейшем было установлено, что ключевыми признаками синдрома являются хроническая уртикарная сыпь и наличие моноклональной гаммапатии неясного значения, чаще представленной иммуноглобулином класса IgM. Со временем в клиническое описание были включены такие проявления, как лихорадка, артралгии, боли в костях и лимфаденопатия, что позволило рассматривать заболевание как системное аутовоспалительное расстройство[3][4].
Диагностические критерии синдрома были сформулированы в 1999 году, что позволило унифицировать подходы к распознаванию заболевания и отличать его от других форм хронической крапивницы и системных воспалительных состояний. Первоначально синдром считался исключительно редким и преимущественно регистрировался в странах Европы, однако с течением времени сообщения о заболевании стали поступать и из других регионов[2].
Этиология
Этиология синдрома Шницлер окончательно не установлена. Заболевание рассматривается как мультифакторное аутовоспалительное состояние, в основе которого лежит дисрегуляция врождённого иммунного ответа. Наследственный характер заболевания не доказан, однако у части пациентов выявляются генетические особенности, которые могут способствовать формированию хронического воспалительного процесса[2][4].
Описано наличие гетерозиготной мутации p.Glu148Gln гена MEFV, кодирующего пирин — белок, участвующий в регуляции активности инфламмасомы. Указанная мутация ассоциирована с нарушением механизмов контроля воспаления, однако не является специфичной для синдрома Шницлер и встречается лишь у ограниченного числа пациентов. Герминальные мутации гена NLRP3, характерные для криопирин-ассоциированных периодических синдромов, при синдроме Шницлер, как правило, не обнаруживаются. В отдельных наблюдениях описан соматический мозаицизм NLRP3, что позволяет рассматривать заболевание как приобретённую форму аутовоспалительной патологии[4][5].
Особое значение придаётся мутации MYD88 p. L265P, которая выявляется у части пациентов с синдромом Шницлер. Данная мутация приводит к конститутивной активации сигнального пути NF-κB и может участвовать в формировании как хронического воспаления, так и моноклональной гаммапатии. Однако её выявление носит непостоянный характер, что указывает на гетерогенность этиологических механизмов заболевания[4][6].
Моноклональная гаммапатия, преимущественно IgM-типа, является обязательным признаком синдрома Шницлер. Её происхождение до конца не установлено. Рассматривается как возможность вторичного формирования парапротеина на фоне длительного воспалительного процесса, так и его потенциальная роль в инициации иммунных нарушений. Отмечено, что в ряде случаев моноклональный компонент выявляется спустя несколько лет после появления клинических симптомов, что косвенно свидетельствует о вторичном характере гаммапатии[4][6].
Патогенез
Патогенез синдрома Шницлер связан с нарушением регуляции врождённого иммунного ответа и патологической активацией инфламмасомы, приводящей к избыточной продукции провоспалительных цитокинов. Ключевую роль в развитии заболевания играет интерлейкин-1-бета, что подтверждается выраженным и быстрым клиническим эффектом ингибиторов интерлейкина-1[2][4].
В норме активация инфламмасомы NLRP3 происходит в два этапа: первичная стимуляция через толл-подобные рецепторы индуцирует синтез про-интерлейкина-1-бета, после чего второй сигнал запускает сборку инфламмасомного комплекса, активацию каспазы-1 и образование биологически активного интерлейкина-1-бета. При синдроме Шницлер данный механизм нарушен, что приводит к персистирующей продукции провоспалительных цитокинов[2][4].
Несмотря на отсутствие стабильных мутаций NLRP3, у пациентов выявляются признаки его функциональной гиперактивации. Отмечается повышение концентраций IL-1-бета, IL-6, IL-18, фактора некроза опухоли альфа. Повышение концентрации IL-18, а также выявление внеклеточных комплексов ASC (apoptosis-associated speck-like protein containing a caspase recruitment domain — апоптоз-ассоциированный белок, содержащий домен рекрутирования каспаз) свидетельствуют об активации каспазы-1 и инфламмасомы. Дополнительно установлено повышение фосфорилирования IRAK-4 — ключевого адаптерного белка сигнальных путей IL-1R и TLR, что подтверждает роль этих сигнальных каскадов в патогенезе заболевания[4][6].
Важную роль играет нейтрофильное воспаление. В очагах поражения выявляются нейтрофильные инфильтраты с признаками лейкоцитоклазии. Активированные нейтрофилы образуют внеклеточные ловушки, способствующие поддержанию воспалительного процесса. Сыворотка пациентов способна индуцировать образование нейтрофильных внеклеточных ловушек, что, вероятно, связано с высокой концентрацией циркулирующих провоспалительных цитокинов[2][4].
Дополнительным патогенетическим механизмом считается активация моноцитов и фибробластов под действием IL-1-бета с повышенной продукцией хемокинов, включая CCL2, что способствует миграции воспалительных клеток в кожу, костную ткань и другие органы. Наряду с этим выявляются изменения адаптивного иммунного ответа, включая функциональные нарушения Т-клеточного звена[4].
Моноклональная гаммапатия рассматривается как один из ключевых, но до конца не объяснённых компонентов заболевания. Она может формироваться вторично на фоне длительного воспаления либо участвовать в поддержании иммунной активации. Обнаружение мутации MYD88 p. L265P у части пациентов указывает на возможную связь между активацией сигнального пути NF-κB, гиперпродукцией цитокинов и риском лимфопролиферативных процессов[4].
Эпидемиология
Синдром Шницлер относится к редким заболеваниям, точная распространённость которого не установлена. Ограниченное число описанных наблюдений обусловлено как истинной редкостью патологии, так и её недостаточной диагностируемостью. Предполагается, что значительная часть случаев остаётся нераспознанной вследствие вариабельности клинических проявлений и длительной задержки в установлении диагноза. В среднем интервал между появлением первых симптомов и постановкой диагноза превышает пять лет. Заболевание встречается во всех этнических группах. Наблюдается незначительное преобладание мужчин, соотношение мужчин и женщин составляет примерно 1,76:1. Возраст пациентов на момент установления диагноза варьирует от 13 до 71 года, при этом средний возраст дебюта заболевания составляет около 51—52 лет[7]. В большинстве случаев синдром развивается у лиц старше 40 лет. Описаны единичные случаи заболевания в молодом возрасте, включая подростковый период, однако такие наблюдения являются редкими. Наибольшее число случаев зарегистрировано в странах Западной Европы, что, вероятно, связано с более высокой настороженностью врачей и лучшей диагностической выявляемостью[2][6].
Диагностика
Синдром Шницлер характеризуется хроническим рецидивирующим течением и многообразием клинических проявлений, обусловленных системным воспалительным процессом. Заболевание, как правило, дебютирует во взрослом возрасте, преимущественно после 40—50 лет, и отличается постепенным прогрессированием симптомов. Наиболее ранним и постоянным проявлением является хроническая уртикарная сыпь, выявляемая практически у всех пациентов. Высыпания представлены розовыми или красными папулами и бляшками, умеренно возвышающимися над поверхностью кожи. Они преимущественно локализуются на туловище и конечностях, реже затрагивают лицо, ладони и подошвы. Отдельные элементы сохраняются от 12 до 48 часов и исчезают без формирования рубцов[7]. В отличие от классической крапивницы зуд выражен слабо либо отсутствует, появляясь лишь у части пациентов спустя несколько лет от начала заболевания. Антигистаминные препараты обычно неэффективны[6][8].
Вторым характерным проявлением является интермиттирующая лихорадка, наблюдаемая у большинства пациентов. Температура тела нередко превышает 38 °C, эпизоды могут длиться от нескольких часов до 1—2 суток и возникать как ежедневно, так и с большими интервалами[7]. Лихорадка может сопровождаться ознобом, ночной потливостью и общей слабостью, однако часто протекает изолированно, без чёткой связи с кожными проявлениями[6][8].
Частыми симптомами являются артралгии и боли в костях. Суставной синдром чаще носит нерезко выраженный характер. Костные боли преимущественно локализуются в области большеберцовых и бедренных костей, костей таза, позвоночника и предплечий[3]. Они могут сопровождаться признаками патологического ремоделирования костной ткани, выявляемыми при инструментальных методах исследования[6][8].
У значительной части пациентов выявляется лимфаденопатия, реже — гепатомегалия и спленомегалия. К дополнительным проявлениям относятся повышенная утомляемость, снижение массы тела, миалгии. В отдельных случаях возможны ангионевротические отёки[6][8].
Лабораторные изменения при синдроме Шницлер отражают наличие системного воспалительного процесса и моноклональной гаммапатии и имеют ключевое значение для подтверждения диагноза. В общем анализе крови выявляются признаки воспалительной реакции, включая повышение скорости оседания эритроцитов, нейтрофильный лейкоцитоз, тромбоцитоз, а также анемию хронического воспаления. В биохимическом анализе крови отмечается повышение концентрации С-реактивного белка[2]. В ряде случаев определяется снижение концентрации компонентов системы комплемента, преимущественно фракции C4[9].
Обязательным лабораторным признаком синдрома является наличие моноклональной гаммапатии. При электрофорезе и иммунофиксации белков сыворотки крови чаще выявляется моноклональный иммуноглобулин класса IgM, преимущественно с κ-цепью. Реже встречаются варианты с IgG или сочетанием иммуноглобулинов. Концентрация моноклонального иммуноглобулина, как правило, невысокая и на ранних этапах заболевания может не достигать диагностически значимых значений, что требует динамического лабораторного наблюдения[2].
В отдельных случаях проводится исследование костного мозга. Морфологическая картина обычно характеризуется неспецифической лимфоцитарной и плазмоцитарной инфильтрацией без признаков злокачественной трансформации. Пункция костного мозга выполняется преимущественно с целью исключения лимфопролиферативных заболеваний[2].
Гистологическое исследование биопсийного материала кожи является важным компонентом диагностики. Для синдрома Шницлер характерна картина нейтрофильного уртикарного дерматоза. В дерме определяется периваскулярный и интерстициальный инфильтрат, представленный преимущественно нейтрофилами, часто с явлениями лейкоцитоклазии. Стенки сосудов при этом сохранены, признаки фибриноидного некроза отсутствуют, отёк дермы выражен слабо либо отсутствует[3]. В ряде случаев обнаруживаются отложения иммуноглобулинов и компонентов комплемента в верхних слоях дермы и в зоне дермоэпидермального соединения[2][4].
Инструментальные методы исследования применяются для выявления костных изменений, оценки активности заболевания и исключения лимфопролиферативных осложнений. Характерной особенностью синдрома Шницлер является патологическое ремоделирование костной ткани. Наиболее часто изменения локализуются в области бедренных и большеберцовых костей, костей таза, позвоночника и ключиц. Наиболее информативным методом выявления костных изменений является сцинтиграфия скелета с технецием-99m. Метод позволяет выявлять участки повышенного накопления радиофармпрепарата, соответствующие зонам воспалительной активности и ремоделирования костной ткани, в том числе при отсутствии клинически выраженного болевого синдрома. Данные сцинтиграфии коррелируют с активностью заболевания и могут использоваться для динамического наблюдения[2][3].
Магнитно-резонансная томография выявляет участки костного склероза, отёка костного мозга и периостита. На Т1-взвешенных изображениях определяется снижение сигнала, на Т2-взвешенных — его повышение, что отражает воспалительные изменения костной ткани. Компьютерная томография применяется для визуализации зон остеосклероза и гиперостоза, однако уступает сцинтиграфии по чувствительности при оценке активности процесса. Позитронно-эмиссионная томография используется преимущественно при подозрении на лимфопролиферативные заболевания или при необходимости дифференциальной диагностики. Для оценки активности синдрома Шницлер её диагностическая значимость низкая[2][3].
При наличии увеличенных лимфатических узлов выполняется ультразвуковое исследование с последующим гистологическим исследованием биопсийного материала при наличии показаний[10].
Диагностика синдрома Шницлер основывается на совокупности клинических, лабораторных и инструментальных данных. Для верификации диагноза используются Страсбургские критерии, которые включают обязательные и дополнительные признаки[7].
К обязательным критериям относятся[7]:
- хроническая уртикарная сыпь;
- наличие моноклональной гаммапатии класса IgM или IgG.
К дополнительным критериям относят[7]:
- рецидивирующую лихорадку;
- повышение концентрации С-реактивного белка и/или нейтрофильный лейкоцитоз;
- признаки патологического ремоделирования костной ткани, выявляемые при сцинтиграфии, магнитно-резонансной томографии или по повышению костной фракции щелочной фосфатазы;
- нейтрофильный инфильтрат в дерме при гистологическом исследовании кожи.
Для установления достоверного диагноза требуется наличие двух обязательных критериев и не менее двух дополнительных при IgM-гаммапатии либо трёх дополнительных при IgG-гаммапатии. Вероятный диагноз допускается при наличии двух обязательных критериев и меньшего числа дополнительных признаков[7].
Дифференциальная диагностика
Дифференциальную диагностику синдрома Шницлер необходимо проводить со следующими заболеваниями[8][10][11]:
- гипокомплементемический уртикарный васкулит;
- криоглобулинемический васкулит;
- синдром гипериммуноглобулинемии D;
- приобретённая недостаточность ингибитора C1;
- семейный холодовой аутовоспалительный синдром;
- синдром CINCA (хронический младенческий неврологический кожно-артикулярный синдром);
- семейная средиземноморская лихорадка;
- TRAPS-синдром (периодический синдром, ассоциированный с рецептором фактора некроза опухоли);
- уртикарный васкулит;
- идиопатическая хроническая крапивница;
- синдром POEMS (полинейропатия, органомегалия, эндокринопатия, моноклональная гаммапатия, поражения кожи);
- макроглобулинемия Вальденстрёма;
- замедленная крапивница от давления[2];
- мастоцитоз;
- лимфома;
- множественная миелома;
- криопирин-ассоциированные периодические синдромы[4];
- амилоидоз[12];
- системная красная волчанка[7];
- болезнь Стилла[7];
- синдром Макла — Уэльса[7];
Осложнения
Осложнения синдрома Шницлер связаны с длительным течением заболевания и персистирующей системной воспалительной активностью. В клинической практике описано развитие лимфопролиферативных заболеваний, включая макроглобулинемию Вальденстрёма, лимфоплазмоцитарную лимфому, множественную миелому и другие В-клеточные лимфомы. Вероятность их возникновения возрастает по мере увеличения продолжительности заболевания и может реализовываться через 10—20 лет от начала клинических проявлений[10]. В ряде случаев наблюдается развитие AA-амилоидоза, обусловленного хроническим воспалением и длительным повышением концентрации сывороточного амилоида A. Данное состояние может сопровождаться поражением внутренних органов и требует своевременного выявления[2][3].
Также описаны поражения периферической нервной системы с формированием сенсорной или моторной нейропатии, развитие анемии и вовлечение почек. Возможны офтальмологические нарушения. Формирование осложнений, как правило, связано с длительным течением заболевания и недостаточным контролем воспалительной активности[2].
Лечение
Лечение синдрома Шницлер включает различные терапевтические подходы и направлено на купирование симптомов и подавление механизмов аутовоспалительного процесса[3][5].
Основу современной терапии составляют препараты, блокирующие интерлейкин-1, поскольку контроль интерлейкин-1-опосредованного воспаления позволяет быстро уменьшать выраженность кожных проявлений и системных симптомов и снижать воспалительную активность. В качестве клинической цели терапии рассматривается стойкое подавление воспаления с нормализацией концентрации сывороточного амилоида A в сыворотке крови и концентрации С-реактивного белка в сыворотке крови. Анакинра является рекомбинантным антагонистом рецептора интерлейкина-1. Препарат связывается с рецептором интерлейкина-1 и препятствует взаимодействию интерлейкина-1-альфа и интерлейкина-1-бета с рецептором без запуска сигнальной трансдукции, что приводит к быстрому клиническому эффекту и уменьшению системной воспалительной активности. Для терапии анакинрой характерна выраженная клиническая динамика в ранние сроки лечения и поддержание эффекта при продолжении терапии. Наиболее типичным нежелательным явлением является реакция в месте инъекции[2][5].
Канакинумаб представляет собой моноклональное антитело к интерлейкину-1-бета. На фоне терапии достигается стойкое подавление воспалительных проявлений с нормализацией концентрации сывороточного амилоида A и С-реактивного белка в сыворотке крови при продолжении лечения[3][5].
Рилонацепт относится к препаратам, связывающим интерлейкин-1-альфа и интерлейкин-1-бета, действуя как «ловушка» и предотвращая их связывание с мембранным рецептором. Для данного варианта терапии также характерно быстрое развитие клинического эффекта. При недостаточном ответе на блокаду интерлейкина-1 может рассматриваться терапия, направленная на интерлейкин-6. Тоцилизумаб применяется как вариант монотерапии либо в сочетании с другими иммуносупрессивными средствами, при этом клинический эффект может быть вариабельным. Ингибиторы фактора некроза опухоли альфа, включая этанерцепт, адалимумаб и инфликсимаб, в большинстве случаев не обеспечивают клинически значимого улучшения и могут сопровождаться усилением симптомов. Терапия, направленная на интерлейкин-17, рассматривается как потенциальный вариант у пациентов с недостаточным ответом на блокаторы интерлейкина-1, с учётом участия интерлейкина-17A и нейтрофильного воспаления в кожных проявлениях заболевания[3][5].
Даже при достижении клинической ремиссии на фоне блокады интерлейкина-1 или интерлейкина-6 моноклональная гаммапатия, как правило, сохраняется, что требует продолжения длительного наблюдения за моноклональным компонентом независимо от выраженности клинического ответа[3][5].
Прогноз
Синдром Шницлер характеризуется хроническим течением без тенденции к спонтанному выздоровлению. На ранних этапах заболевание, как правило, не сопровождается выраженными системными нарушениями и может протекать относительно стабильно, однако по мере увеличения длительности болезни прогноз в значительной степени определяется риском развития лимфопролиферативных осложнений[7].
Вероятность формирования лимфопролиферативных заболеваний, включая макроглобулинемию Вальденстрёма и другие злокачественные лимфоидные неоплазии, постепенно возрастает с течением времени и составляет около 15 % через 10 лет от начала заболевания, достигая 25—30 % при более длительном течении. Несмотря на высокую общую выживаемость, превышающую 90 % в течение 15 лет, отсутствие спонтанных ремиссий, прогрессирующий характер воспалительного процесса и риск поздних осложнений обусловливают необходимость длительного динамического наблюдения и регулярного контроля активности заболевания[2][7].
Диспансерное наблюдение
Пациенты с синдромом Шницлер подлежат длительному динамическому наблюдению. Основными задачами являются контроль активности воспалительного процесса, моноклональной гаммапатии и своевременное выявление признаков лимфопролиферативных заболеваний. Рекомендуется регулярное определение маркеров воспаления, включая концентрацию С-реактивного белка в сыворотке крови, скорость оседания эритроцитов и концентрацию сывороточного амилоида A. Исследования проводятся не реже одного раза в три месяца, а при достижении стойкой клинико-лабораторной ремиссии — не реже двух раз в год[7].
Моноклональная гаммапатия подлежит динамическому контролю с оценкой концентрации иммуноглобулинов в сыворотке крови в зависимости от исходных значений. Увеличение концентрации моноклонального иммуноглобулина, появление лимфаденопатии или системных клинических проявлений требует немедленного углублённого обследования с выполнением пункции костного мозга и, при наличии показаний, биопсии лимфатических узлов[2][7].
Длительное диспансерное наблюдение является обязательным, поскольку риск лимфопролиферативной трансформации сохраняется на протяжении всей жизни пациента и не зависит от выраженности клинических проявлений в конкретный период заболевания[2].
Профилактика
Специфические меры профилактики синдрома Шницлер не разработаны, что обусловлено неясностью этиологических механизмов заболевания. Первичная профилактика невозможна. Основное значение имеют раннее выявление заболевания и своевременное начало терапии, направленной на подавление системного воспаления. Контроль воспалительной активности рассматривается как важнейший фактор, способствующий снижению риска развития AA-амилоидоза и лимфопролиферативных осложнений. Регулярное клиническое наблюдение и лабораторный мониторинг позволяют своевременно выявлять признаки прогрессирования заболевания и корректировать терапевтическую тактику[2][3].