LRP1
Белок 1, подобный рецептору липопротеинов низкой плотности, или рецептор для α2-микроглобулина, или рецептор аполипопротеина E (англ. Low density lipoprotein receptor-related protein 1 (LRP1); alpha-2-macroglobulin receptor (A2MR), apolipoprotein E receptor (APOER), CD369) — мембранный белок семейства рецепторов липопротеинов низкой плотности, участвующий в рецептор-опосредованном эндоцитозе. Продукт гена человека LRP1[5][6][7] LRP1 является сигнальным белком, играющим роль во многих биологических процессах, включая метаболизм липопротеинов, клеточная подвижность и в таких патологиях, как нейродегенеративные заболевания, атеросклероз и рак[8][9]
Общие сведения
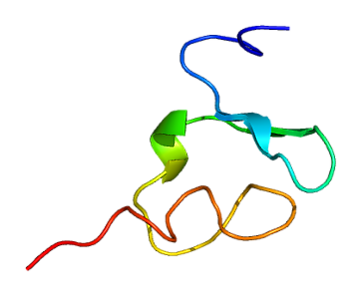
Структура
Ген LRP1 кодирует белок-предшественник с молекулярной массой 600 кДа, который под действием внутриклеточной протеазы фурина расщепляется в транс-отделе аппарата Гольджи на две цепи: альфа-цепь 515 кДа (внеклеточный белок) и бета-цепь 85 кДа (цитоплазматический белок), которые остаются ассоциированы друг с другом нековалентными связями[8][10][11]. Как все белки семейства рецепторов липопротеинов низкой плотности LRP1 содержит цистеин-богатые повторы комплементного типа, EGF-повторы, бета-пропеллерный домен и цитоплазматический домен[9]. Большой внеклеточный домен LRP1α, или альфа-цепь, содержит лиганд-связывающие домены, пронумерованные от I до IV, которые включают 2, 8, 10 и 11 цистеиновых повторов, соответственно[8][9][10][11]. Эти повторы связывают белки внеклеточного матрикса, факторы роста, протеазы, комплексы протеазных ингибиторов и другие белки липопротеинового метаболизма[8][9]. Из 4 лиганд-связывающих доменов домены II и IV отвечают за связывание большинства лигандов LRP1.[11] EGF-повторы и β-пропеллерные домены обеспечивают высвобождение лигандов при понижении pH, происходящем в эндосомах, при этом β-пропеллер сдвигает освободившийся лиганд[9]. Трансмембранный домен (LRP1β), или β-цепь белка, содержит 100 аминокислот цитоплазматического C-конца. Цитоплазменный мотив NPxY играет роль в эндоцитозе и передаче сигнала.[8]
Функции
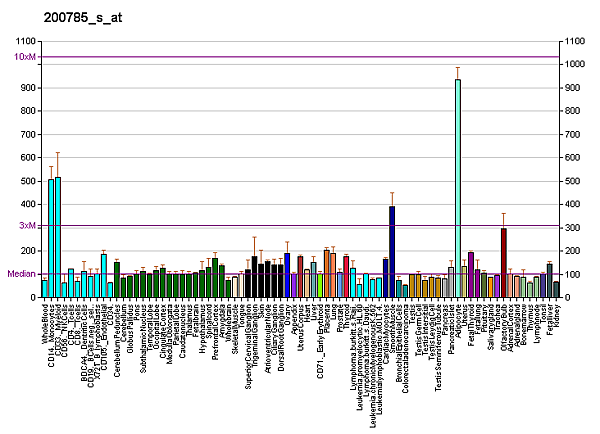
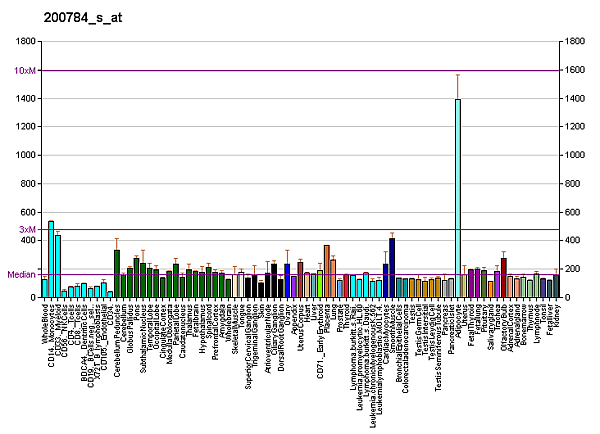
Белок LRP1 экспрессирован практически во всех тканях. Наиболее высокий уровень рецептора находится в гладкомышечных клетках, гепатоцитах и нейронах[8][9]. LRP1 играет роль во внутриклеточной передаче сигнала и эндоцитозе, которые вовлечены во множество биологических процессов: липидный и липопротеиновый метаболизм, деградация протеаз, регулирование рецептора тромбоцитарного фактора роста, созревание и рециркулирование интегринов, регулирование сосудистого тонуса, регулирование проницаемости гемато-энцефалического барьера, клеточная пролиферация, клеточная миграция, воспаление и апоптоз. Он также играет роль в развитии нейродегенеративных заболеваний, атеросклероза и рака[7][8][9][10][11].
В основном LRP1 участвует в регулировании активности белков за счёт связывания лиганда как ко-рецептор вместе с трансмембранными или адаптерными белками, такими как плазмин, с последующей деградацией лиганда в лизосомах[9][10][11]. В липопротеиновом метаболизме LRP1 связывает аполипопротеин E, что стимулирует сигнальный путь, который вызывает повышение уровня внутриклеточного cAMP, увеличивает активность протеинкиназы A и ингибирует миграцию гладкомышечных клеток. В целом это приводит к протекции против сосудистых заболеваний[9]. В то время как мембрано-связанный LRP1 обеспечивает очистку от протеаз и ингибиторов, протеолитическое отщепление эктодомена высвобождает LRP1, который, наоборот, конкурирует с мембранным LRP1, что приводит к задержке нормальной функции белка[8]. В процесс отщепления внеклеточного домена LRP1 вовлечены несколько шеддаз, включая ADAM10,[12] ADAM12,[13] ADAM17[14] и MT1-MMP.[13]. LRP1 постоянно эндоцитируется с мембраны и вновь рециркулирует на клеточную мембрану[9].
Хотя роль LRP1 в апоптозе менее изучена, известно, что это требует связывания LRP1 с tPA, что приводит к сигнальному каскаду ERK1/2 и приводит к повышенной клеточной выживаемости[15].
Роль в патологии
Нормальное функционирование нейронов требует холестерина. Холестерин доставляется к нейронам апоЕ-содержащими липопротеинами, которые связываются с рецепторами LRP1, экспрессированными на нейронах. Предполагается, что одной из причин болезни Альцгеймера может быть снижение LRP1, опосредованное метаболизмом APP, что в конечном итоге приводит к снижению нейронального холестерина и увеличению бета-амилоида (Aβ)[16].
LRP1 также играет роль в эффективном клиренсе Aβ из мозга через гемато-энцефалический барьер[17][18]. Известно, что экспрессия LRP1 снижается в эндотелиальных клетках в процессе старения как у человека, так и у животных[19][20]. Механизм клиренса модулируется полиморфизмом апоE, причём наличие изоформы апоE4 приводит к пониженному трансцитозу Aβ в моделях гемато-энцефалического барьера[21]. Кроме этого, сниженный клиренс Aβ может возникать из-за усиленного отщепления эктодомена LRP1 шеддазами, что также замедляет клиренс Aβ[22].
LRP1 играет роль в нескольких процессах, связанных с развитием сердечно-сосудистых заболеваний. Атеросклероз — основная причина таких сердечно-сосудистых заболеваний, как инсульт и инфаркт миокарда. В печени LRP1 играет важную роль в удалении из кровотока атерогенных липопротеинов, таких как ремнанты хиломикрон и ЛПОНП, и других проатерогенных компонентов[23][24]. LRP1 играет также холестерин-независимую роль в атеросклерозе путём модулирования активности и клеточной локализации PDGFR-β в гладко-мышечных клетках[25][26]. Наконец, LRP1 в макрофагах модулирует внеклеточный матрикс и воспалительный ответ, что имеет важное значение в прогрессировании атеросклероза[27][28].
Взаимодействия
Литература
- Li Z., Dai J., Zheng H., Liu B., Caudill M. An integrated view of the roles and mechanisms of heat shock protein gp96-peptide complex in eliciting immune response (англ.) // Frontiers in Bioscience : journal. — Frontiers in Bioscience, 2002. — March (vol. 7). — P. d731—51. — doi:10.2741/A808. — PMID 11861214.
- van der Geer P. Phosphorylation of LRP1: regulation of transport and signal transduction (англ.) // Trends in Cardiovascular Medicine : journal. — 2002. — May (vol. 12, no. 4). — P. 160—165. — doi:10.1016/S1050-1738(02)00154-8. — PMID 12069755.
- May P., Herz J. LDL receptor-related proteins in neurodevelopment (неопр.) // Traffic. — 2003. — May (т. 4, № 5). — С. 291—301. — doi:10.1034/j.1600-0854.2003.00086_4_5.x. — PMID 12713657.
- Llorente-Cortés V., Badimon L. LDL receptor-related protein and the vascular wall: implications for atherothrombosis (англ.) // Arteriosclerosis, Thrombosis, and Vascular Biology : journal. — 2005. — March (vol. 25, no. 3). — P. 497—504. — doi:10.1161/01.ATV.0000154280.62072.fd. — PMID 15705932.
- Huang S.S., Huang J.S. TGF-beta control of cell proliferation (англ.) // Journal of Cellular Biochemistry : journal. — 2005. — October (vol. 96, no. 3). — P. 447—462. — doi:10.1002/jcb.20558. — PMID 16088940.
- Lillis A.P., Mikhailenko I., Strickland D.K. Beyond endocytosis: LRP function in cell migration, proliferation and vascular permeability (англ.) // Journal of Thrombosis and Haemostasis : journal. — 2005. — August (vol. 3, no. 8). — P. 1884—1893. — doi:10.1111/j.1538-7836.2005.01371.x. — PMID 16102056.