Fas-рецептор
Fas-рецептор (англ. Fas receptor, сокр. FasR), также известный как апоптозный антиген 1 (APO-1 или APT), кластер дифференцировки 95 (CD95) или член суперсемейства рецепторов фактора некроза опухолей 6 (TNFRSF6) — белок, который у людей кодируется геном FAS[5][6]. Впервые Fas был идентифицирован с использованием моноклональных антител, полученных путём иммунизации мышей клеточной линией FS-7. Таким образом, название Fas происходит от FS-7-ассоциированного поверхностного антигена[7].
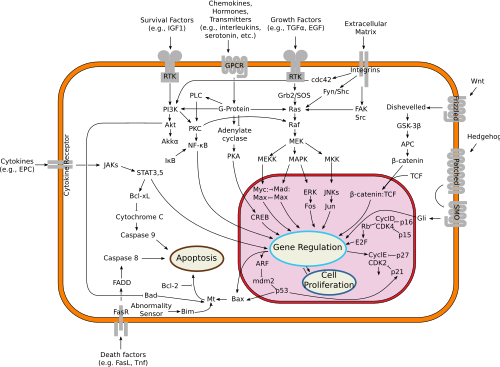
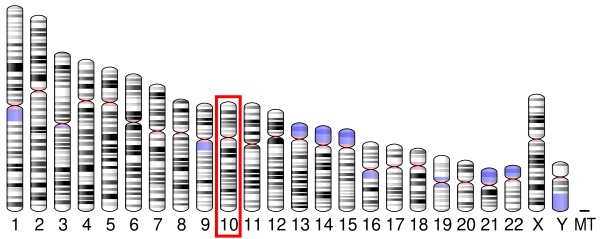
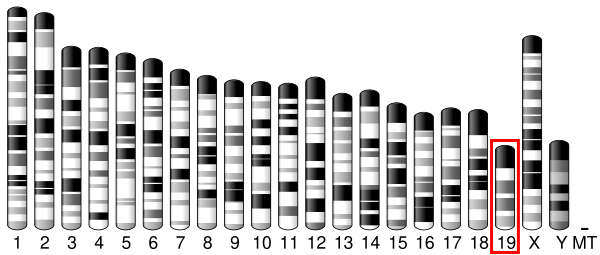
Рецептор Fas представляет собой так называемый рецептор смерти, расположенный на поверхности клеток, активация которого приводит к запрограммированной гибели клеток (апоптозу). Активация FasR является началом одного из двух путей апоптоза — рецептор-опосредованного (он является внешним), второй путь — митохондриальный (внутренний)[8]. Ген, кодирующий FasR у людей локализован на 10-ой хромосоме и на 19-ой у мышей. Подобные последовательности, являющиеся эволюционно связанными (ортологи), обнаружены у большинства млекопитающих.
Общие сведения
Ген
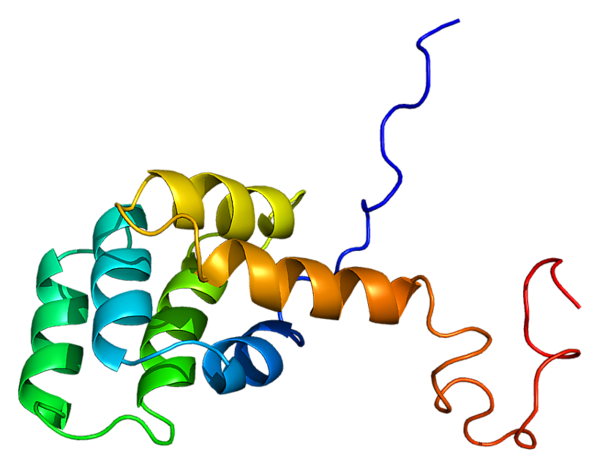
Белок
В предыдущих отчётах было идентифицировано до восьми вариантов сплайсинга, которые транслируются в семь изоформ белка. Индуцирующий апоптоз рецептор Fas называют изоформой 1 и представляет собой трансмембранный белок 1 типа. Многие из других изоформ являются редкими гаплотипами, которые обычно связаны с состоянием заболевания. Однако две изоформы, апоптоз-индуцирующая мембраносвязанная форма и растворимая форма, являются нормальными продуктами, синтез которых посредством альтернативного сплайсинга регулируется цитотоксическим РНК-связывающим белком TIA1[9].
Зрелый белок Fas содержит 319 аминокислот, имеет предсказанную молекулярную массу 48 кДа и разделён на 3 домена: внеклеточный домен, трансмембранный домен и цитоплазматический домен. Внеклеточный домен содержит 157 аминокислот и богат остатками цистеина. Трансмембранный и цитоплазматический домены содержат 17 и 145 аминокислот соответственно. Экзоны с 1 по 5 кодируют внеклеточную область. Экзон 6 кодирует трансмембранную область. Экзоны 7-9 кодируют внутриклеточную область.
Функции
Fas образует инициирующий смерть сигнальный комплекс (DISC) при связывании лиганда. Тример Fas-лиганд (FasL), закреплённый на мембране на поверхности соседней клетки, вызывает олигомеризацию Fas. Имеются недавние исследования, в которых предполагалось, что тримеризация Fas не может быть подтверждена. Другие модели предполагают олигомеризацию до 5-7 молекул Fas в DISC[10]. Данное событие также имитируется связыванием агонистического антитела Fas, хотя некоторые данные свидетельствуют о том, что индуцируемый антителом апоптотический сигнал ненадёжен при изучении передачи сигналов Fas. С этой целью было использовано несколько хитроумных способов тримеризации антител в исследованиях in vitro.
При последующей агрегации домена смерти (DD) рецепторный комплекс интернализуется с помощью клеточного эндосомального механизма. Это позволяет адаптивной молекуле FADD связывать домен смерти Fas со своим собственным доменом смерти[11].
FADD также содержит эффекторный домен смерти (DED) вблизи его аминокислотного конца[12], который облегчает связывание с DED FADD-подобного бета-превращающего фермента интерлейкина-1 (FLICE), более часто называемого каспазой 8. Затем FLICE может самостоятельно активироваться посредством протеолитического расщепления на субъединицы p10 и p18, две из которых образуют активный фермент гетеротетрамера. Активная каспаза 8 затем высвобождается из DISC в цитозоль, где она расщепляет другие эффекторные каспазы, что в конечном итоге приводит к деградации ДНК, мембранному блеббингу и другим признакам апоптоза.
Недавно было также показано, что Fas способствует росту опухоли, поскольку во время прогрессирования опухоли он часто подавляется или клетки становятся устойчивыми к апоптозу. Раковые клетки в целом, независимо от их чувствительности к апоптозу Fas, зависят от конститутивной активности Fas. Это стимулируется продуцируемыми опухолевыми клетками Fas-лигандов, необходимых для оптимального роста[13].
Хотя было показано, что Fas стимулирует рост опухоли в вышеупомянутых моделях мышей, анализ базы данных геномики рака человека показал, что FAS значительно не амплифицируется очагово в наборе данных из 3131 опухолей (FAS не является онкогеном), но значительно фокально удаляется во всех наборах данных из этих 3131 опухолей[14], предполагая, что FAS функционирует как супрессор опухолей у людей.
В культивируемых клетках FasL индуцирует различные типы апоптоза раковых клеток через рецептор Fas. На моделях AOM-DSS-индуцированной карциномы толстой кишки и MCA-индуцированной саркомы мышей было показано, что Fas действует как супрессор опухолей[15]. Кроме того, рецептор Fas также опосредует опухоль-специфическую цитотоксичность Т-лимфоцитов (CTL)[16].
Роль в апоптозе
В некоторых статьях предполагается, что внешний путь Fas является достаточным для индукции полного апоптоза, происходящего в определённых типах клеток посредством сборки DISC и последующей активации каспазы 8. Эти клетки называются клетками 1 типа и характеризуются неспособностью антиапоптотических членов семейства Bcl-2 (а именно Bcl-2 и Bcl-xL) защищать от опосредованного Fas апоптоза. Характерные клетки 1 типа включают H9, CH1, SKW6.4 и SW480, все из которых представляют собой линии лимфоцитов, кроме последней, которая представляет собой линию клеток аденокарциномы толстой кишки. Тем не менее, в каскаде сигналов Fas существуют доказательства перекрёстных помех между внешним и внутренним путями.
В большинстве типов клеток каспаза 8 катализирует расщепление проапоптотического белка BH3-only Bid в его усеченную форму, tBid. Только BH-3 члены семейства Bcl-2 взаимодействуют исключительно с антиапоптотическими членами семейства (Bcl-2, Bcl-xL), позволяя Bak и Bax транслоцироваться на наружную митохондриальную мембрану, таким образом проникая в неё и облегчая высвобождение проапоптотические белки, таких как цитохром C и Smac/DIABLO, антагониста ингибиторов белков апоптоза (IAPs).