ADAM10
ADAM10 (CD156c; англ. A Disintegrin And Metalloproteinase domain 10; КФ: 3.4.24.81) — фермент металлопротеаза, относящийся к семейству металлопротеаз ADAM. Играет важную роль в развитии, воспалении, нейропротекции и онкологических заболеваниях. По ферментативной специфичности близка к другой металлопротеазе ADAM17.
Общие сведения
Структура
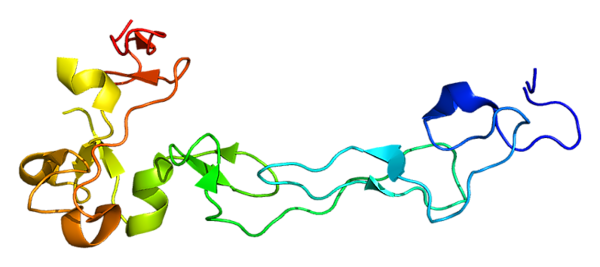
С помощью метода кристаллографического анализа дифракции рентгеновских лучей была изучена структура одного домена ADAM10. Богатый цистеином домен играет важную роль в регуляции активности протеаз in vivo. Недавние экспериментальные данные свидетельствуют о том, что эта область, отличная от активного центра, может быть ответственна за субстратную специфичность фермента. Предполагается, что этот домен связывается с определенными областями субстрата и фермента, позволяя происходить гидролизу пептидных связей в четко определенных участках субстрата[5].
Предлагаемый активный центр ADAM10 идентичен ферментам в семействе металлопротеиновых белков змеиного яда. Структурный анализ ADAM17 показал, что он имеет ту же последовательность аминокислот активного центра, что и ADAM10, и это позволяет предположить, что три гистидина в этой последовательности связывают атом Zn2+, а глутамат является каталитически активным участком[6].
Функции
ADAM10 представляет собой металлопротеазу с относительно низкой специфичностью, локализованную на поверхности клеток и способную расщеплять широкий спектр белков. В нейронах ADAM10 является наиболее важным ферментом для протеолитического процессинга белка-предшественника амилоида. ADAM10 вместе с ADAM17 расщепляет эктодомен триггерного рецептора, экспрессируемого на миелоидных клетках — TREM2, с образованием растворимого sTREM2, который был предложен в качестве биомаркера при нейродегенеративных заболеваниях. ADAM10 принадлежит к подсемейству металлопротеаз A, самому древнему подсемейству белков ADAM, которое является общим для всех основных групп животных, хоанофлагеллят, грибов и зелёных водорослей из класса Mamiellophyceae.
Субстраты
К субстратам ADAM10 относятся ряд молекул адгезии, находящиеся на клеточной мембране, включая L1-CAM, E-кадгерин, N-кадгерин и CD44.[7][8]
Клиническое значение
ADAM10 играет ключевую роль в регуляции молекулярных механизмов, ответственных за формирование, созревание и стабилизацию дендритных шипов, а также в молекулярной организации глутаматергических синапсов. Следовательно, изменение активности ADAM10 строго коррелирует с возникновением различных типов синаптопатий, начиная от нарушений развития нервной системы, то есть расстройств типа аутизма, и заканчивая нейродегенеративными заболеваниями, типа болезни Альцгеймера[9].
В сочетании с низкими дозами герцептина — противоопухолевыми антителами — селективные ингибиторы ADAM10 снижают пролиферацию в клеточных линиях со повышенной экспрессией HER2, в то время как ингибиторы, которые не ингибируют ADAM10, не действуют. Эти результаты согласуются с тем, что ADAM10 является основным фактором контроля HER2, ингибирование которого может обеспечить новый терапевтический подход к лечению рака молочной железы и других видов рака с активной передачей сигналов HER2. Повышенное количество продукта гена ADAM10 в нейронных синапсах в сочетании с белком AP2 было отмечено в нейронах гиппокампа у пациентов с болезнью Альцгеймера[10].
Примечания
Ссылки
- Pruessmeyer J., Ludwig A. The good, the bad and the ugly substrates for ADAM10 and ADAM17 in brain pathology, inflammation and cancer (англ.) // Seminars in Cell and Developmental Biology : journal. — 2009. — April (vol. 20, no. 2). — P. 164—174. — doi:10.1016/j.semcdb.2008.09.005. — PMID 18951988.
- Crawford H.C., Dempsey P.J., Brown G., Adam L., Moss M.L. ADAM10 as a therapeutic target for cancer and inflammation (англ.) // Current Pharmaceutical Design : journal. — 2009. — Vol. 15, no. 20. — P. 2288—2299. — PMID 19601831.
- Deuss M., Reiss K., Hartmann D. Part-time alpha-secretases: the functional biology of ADAM 9, 10 and 17 (англ.) // Current Alzheimer Research : journal. — 2008. — April (vol. 5, no. 2). — P. 187—201. — PMID 18393804.