CD97
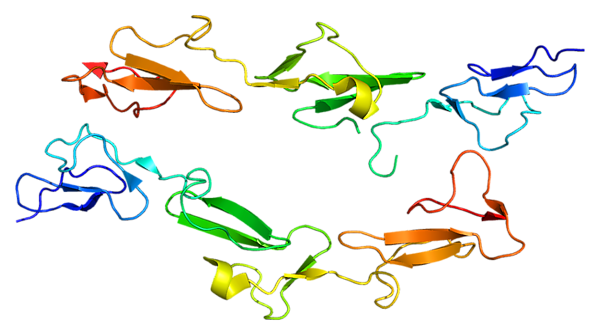
ADGRE5 (Adhesion G protein-coupled receptor E5) или CD97 — белок класса адгезивных рецепторов, сопряжённых с G-белком (GPCR)[5][6], продукт гена ADGRE5[7][8][9][10]. Белки класса адгезивных GPCR характеризуются крупным внеклеточным регионом, который часто содержат N-конечные белковые функциональные фрагменты, связанные с семиспиральным мембранным регионом TM7 через домен, известный как GAIN (индуцирующий аутопротеолиз GPCR)[11].
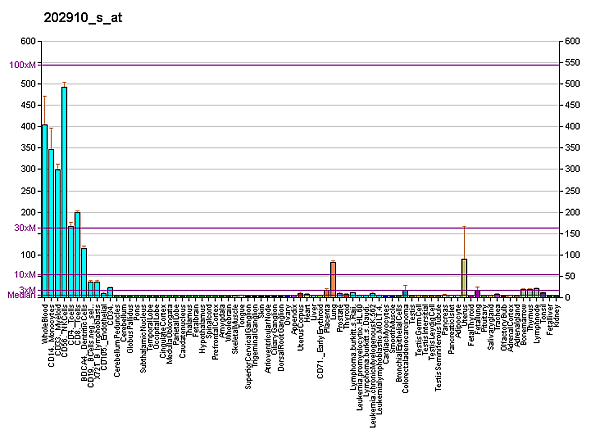
CD97 широко экспрессирован на многих клетках, включая гемопоэтические стволовые клетки и клетки-предшественники, иммунные клетки, эпителиальные клетки, мышечные клетки, а также опухолевые клетки упомянутого происхождения[12][13][14][15][16][17]. N-Конечный домен CD97 содержит EGF-подобные домены, которые в результате альтернативного сплайсинга образуют три арианта белка[9]. N-Конечный фрагмент CD97 имеет 3-5 EGF-подобных доменов у человека и 3-4 — у мыши[18].
Общие сведения
| CD97 | |||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||||||||||||||||||||||||||||||||||||||||||
| Псевдонимы | ADGRE5, TM7LN1, CD97, adhesion G protein-coupled receptor E5 | ||||||||||||||||||||||||||||||||||||||||||||||
| Внешние ID | OMIM: 601211 MGI: 1347095 HomoloGene: 8050 GeneCards: ADGRE5 | ||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
Лиганды
Фактор ускорения распада комплемента (DAF/CD55), регуляторный белок каскада комплемента, взаимодействует с первым и вторым EGF-подобными доменами CD97[19], хондроитинсульфат B — с четвёртым[20]. Интегрины α5β1 и αvβ3 связываются с доменом RGD, расположенным после EGF-подобных доменов[21], а CD90 (Thy-1) взаимодействует с доменом GAIN[22]. Связывание с CD55 требует N-гликозилирования EGF-подобных доменов CD97[23].
Роль в передаче сигнала
Трансгенная экспрессия CD97 у мышей приводит к увеличению нефосфорилированного мембраносвязанного β-катенина и фосфорилированной протеинкиназы B (AKT)[24]. Более того, эктопическая экспрессия CD97 облегчает активацию RhoA посредством связывания с Gα12/13, а также индуцирует экспрессию Ki67 и фосфорилирует киназы ERK и Akt за счёт усиления передачи сигнала рецептора лизофосфатидной кислоты LPAR1[25][26]. Лизофосфатидилэтаноламин и лизофосфатидная кислота используют димер LPAR1–CD97 для переноса сигнала комплекса Gi/o-белок-фосфолипаза C-инозитол-1,4,5-трифосфат и индуцирует уровень внутриклеточного кальция в клетках пака молочной железы[27].
Функции
CD97 играет критическую роль медиатора иммунной системы. При активации лимфоидных и миелоидных клеток и нейтрофилов экспрессия CD97 увеличивается, что обеспечивает адгезию и миграцию этих клеток к участкам воспаления[28]. Более этого, показано, что CD97 регулирует гомеостаз гранулоцитов. Обнаружено, что у мышей, у которых отсутствует CD97 или его лиганд CD55, уровень гранулоцитов повышен в два раза в результате усиленного гранулопоэза[29]. Антитела против CD97 снижают различные воспалительные заболевания за счёт понижения гранулоцитов[30]. При этом анти-CD97 антитела вызывают гранулоцитопению только при воспалении посредством механизма, связанного с Fc-рецептором[31]. Наконец, взаимодействие между CD97 и его лигандом CD55 регулирует активацию T-лимфоцитов и усиливает пролиферацию и синтез цитокинов[32][33].
Нарушения в экспрессии CD97 описаны при аутоиммунных заболеваниях, таких как ревматоидный артрит и рассеянный склероз. Экспрессия CD97 на макрофагах и наличие высокого уровня CD55 на фибробласто-подобных синовиальных клетках предполагает, что взаимодействие CD97 с CD55 участвует в рекрутировании и задерживании макрофагов в синовиальной оболочке при ревматоидном артрите[34]. Антитела против CD97, как и отсутствие CD97 и CD55, у мышей снижают синовиальное воспаление и повреждение суставов при индуцированном экспериментальном артрите[35][36]. В мозге CD97 отсутствует в белом веществе, экспрессия белка ограничена исключительно эндотелием сосудов. В ранних предактивных бляшках повышенная экспрессия CD97 на эндотелиальных клетках и стабильная экспрессия на мигрировавших лейкоцитах предполагает роль обоих белков в миграции иммунных клеток через гематоэнцефалический барьер[37]. Кроме этого, свободные N-терминальные фрагменты CD97 обнаружены в сыворотке больных ревматоидным артром и рассеянным склерозом[34].
Кроме важных функций в иммунной системе CD97, вероятно, участвует в межклеточных взаимодействиях. CD97 в энтероцитах толстого кишечника усиливает E-кадгериновые адгезивные контакты, что обеспечивает латеральное межклеточное соединение и регулирует локализацию и деградацию β-катенина, опосредованные киназой гликогенсинтазы 3β и протеинкиназой B[24]. Эктопическая экспрессия CD97 повышает уровень N-кадгерина и β-катенина в клетках фибросаркомы, что усиливает межклеточную агрегацию[38]. CD97 присутствует на саркоплазматическом ретикулуме и периферической сарколемме мышечных клеток скелетных мышц. Однако, хотя отсутствие CD97 влияет на структуру сарколеммы, оно не изменяет функционирование мышцы[17]. Наконец, CD97 способен активировать ангиогенез эндотелия, опосредованный через интегрины α5β1 и αvβ3, которые обеспечивают прикрепление клеток[21].
Клиническое значение
Экспрессия CD97 на опухолевых клетках впервые была обнаружена на клетках дедифференциированной фибросаркомы и в метастазах этих клеток в лимфатических узлах[39]. В настоящее время известно, что CD97 присутствует на многих типах опухолей, включая тироидные, желудочные, поджелудочные, пищеводные, колоректальные и оральные сквамозные саркомы, а также глиобластомы[39][40][41][42][43][44][45]. Кроме этого, повышенная экспрессия CD97 характерна для клеток инвазивной зоны опухолей[46], что предполагает возможную роль белка в миграции и метастазировании опухолевых клеток[43][46] и коррелирует с неблагоприятным прогнозом[44][41][42][47][48]. В некоторых опухолях роль CD97 зависит от изоформы белка. Так, короткая изоформа EGF(1,2,5) усиливает миграцию и метастазирование клеток карциномы желудка[49]; короткая изоформа EGF(1,2,5) индуцирует, а полная изоформа EGF(1-5), наоборот, подавляет проникновение клеток карциномы желудка в ткани[50].
Повышенная экспрессия CD97 индуцирует клеточную миграцию, активирует матриксные металлопротеиназы (MMP) и повышает секрецию интерлийкина 8[51]. Супрессор опухоли микроРНК-126, который часто понижен в опухолевых клетках, влияет на CD97, что может модулировать прогрессирование опухоли[52]. CD97 может образовывать гетеродимер с рецептором LPAR1, играющий роль в росте опухоли, который синэргически модулирует функции и перенос сигнала Rho ГТФазы, опосредованного лизофосфатидной кислотой[26][25]. CD97 регулирует локализацию и деградацию β-катенина[24]. Киназа гликогенсинтазы 3β, заингибированная в некоторых опухолевых клетках, регулирует стабильность β-катенина в цитоплазме и его последующий перенос в ядро, который облегчает экспрессию протоонкогенов[53][54]. Благодаря своей роли в инвазии опухолей и ангиогенезе CD97 является потенциальной терапевтической мишенью. Обнаружено, что несколько агентов способны снизить экспрессию CD97, такие как TGF-β, бутират натрия, ретиноевая кислота и троглитазон[41][42][55].
Примечания
Литература
- Hamann J, Veninga H, de Groot DM, Visser L, Hofstra CL, Tak PP; et al. (2010). “CD97 in leukocyte trafficking”. Adv Exp Med Biol. 706: 128—37. DOI:10.1007/978-1-4419-7913-1_11. PMID 21618832.
- Safaee M, Clark AJ, Ivan ME, Oh MC, Bloch O, Sun MZ; et al. (2013). “CD97 is a multifunctional leukocyte receptor with distinct roles in human cancers (Review)”. Int J Oncol. 43 (5): 1343—50. DOI:10.3892/ijo.2013.2075. PMID 23969601.