Аланинаминопептидаза
Аланинаминопептидаза (ААП, КФ 3.4.11.2; аминопептидаза N) — мембранный белок, фермент, относящийся к классу пептидаз, или протеаз. Используется как маркёр почечных повреждений и играет роль в диагностике определённых болезней почек. Другие названия фермента: аминопептидаза M, микросомальная аминопептидаза, миелоидный гликопротеин плазматической мембраны CD13, gp150.
Общие сведения
| Аланинаминопептидаза | |||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||||||||||||||||||||||||||||||
| Идентификаторы | |||||||||||||||||||||||||||||||||||||||||||||||
| Псевдонимы | ANPEP, APN, CD13, GP150, LAP1, P150, PEPN, alanyl aminopeptidase, membrane, AP-M, hAPN, AP-N | ||||||||||||||||||||||||||||||||||||||||||||||
| Внешние ID | OMIM: 151530 MGI: 5000466 HomoloGene: 68163 GeneCards: ANPEP | ||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
Тканевая специфичность и функции
Аланинаминопептидаза (ААП) локализована в тонком кишечнике и на мембране почечных микроворсинок, а также на других плазматических мембранах. В тонком кишечнике аланинаминопептидаза участвует в конечном разложении пептидов, образованных при гидролизе белков пищи под действием желудочных и панкреатических протеаз.
Кроме этого, ААП имеет множество физиологических функций, включая ферментативную регуляцию пептидов, и функции, связанные с клетками злокачественных опухолей, такие как их инвазивность, дифференцировка и апоптоз, подвижность и ангиогенез. Было показано, что ААП может служить вирусным рецептором и участвовать в метаболизме холестерина[5].
Каталитическая специфичность
ААП является экзопептидазой и высвобождает N-концевую аминокислоту из пептида, амида или ариламида. Предпочтительнее ААП гидролизует связь у N-концевого аланина и других нейтральных аминокислот, но может гидролизовать пептидную связь практически всех остальных аминокислот, включая пролин, хотя с замедленной скоростью. В случае, когда за гидрофобной аминокислотой X следует пролин, ААП высвобождает дипептид X-Pro[6].
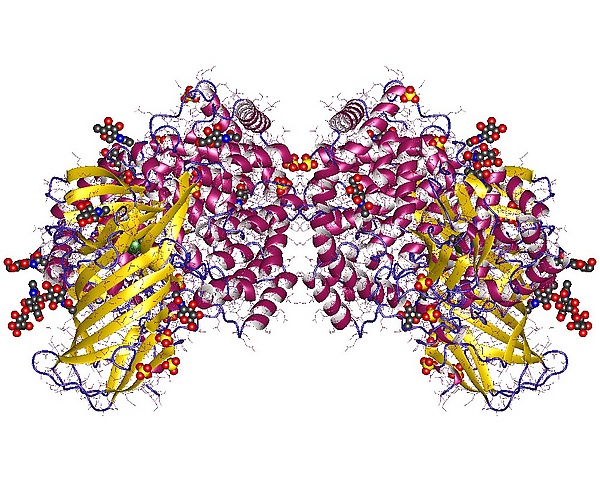
Структура
ААП состоит из 966 аминокислот, молекулярная масса — 109,5 кДа. Включает короткий N-концевой цитоплазматический участок, трансмембранный фрагмент и внеклеточный металлопротеазный фрагмент. Внеклеточный участок включает 4 сульфотирозинов, 1 фосфотреонин и 10 участков N-гликозилирования. Активный центр фермента состоит из акцептора протона (остаток глутаминовой кислоты), трёх аминокислот, связывающих активный цинк и тирозина-стабилизатора промежуточного состояния.
Примечания
Библиография
- Yeager C.L., Ashmun R.A., Williams R.K., et al. Human aminopeptidase N is a receptor for human coronavirus 229E (англ.) // Nature : journal. — 1992. — Vol. 357, no. 6377. — P. 420—422. — doi:10.1038/357420a0. — PMID 1350662.
- Wickström M., Larsson R., Nygren P., Gullbo J. Aminopeptidase N (CD13) as a target for cancer chemotherapy (англ.) // Cancer Science : journal. — 2011. — March (vol. 102, no. 3). — P. 501—508. — doi:10.1111/j.1349-7006.2010.01826.x. — PMID 21205077.