Лимфатическая мальформация
Лимфати́ческая мальформа́ция (ЛМ; лимфангио́ма) — доброкачественное врождённое сосудистое новообразование, обусловленное нарушением лимфангиогенеза в эмбриональном периоде. Оно обычно проявляется в виде кистозного образования, заполненного жидкостью. Хотя ЛМ может поражать любую часть тела, крайне редко - головной мозг. Преимущественно возникает в области головы, шеи или подмышечной впадины у детей. Клиническое проявление ЛМ значительно варьируется у разных пациентов: от локального отёка, проявляющегося поверхностным образованием, до обширной диффузной аномалии лимфатических протоков, приводящей к слоновости. ЛМ обычно растёт медленно и постепенно, но при определённых условиях, таких как инфекция, гормональные изменения или травма, может увеличиваться стремительно, становясь угрожающим для жизни состоянием, требующим немедленного лечения[1][2].
Классификация
Выделяют врождённую ЛМ и приобретённую ЛМ[1].
Клинически выделяют следующие формы ЛМ[2]:
- кистозная ЛМ;
- генерализованная;
- капошиформный лимфангиоматоз;
- болезнь Горхема — Стоута (массивный остеолиз);
- канальцевая ЛМ.
Гистологически кистозная ЛМ делится на[1][2]:
- макрокистозные ЛМ — обычно выглядят как солитарные образования различных размеров, состоящие из множественных крупных кист, заполненных жидкостью. Чаще всего они локализуются в области шеи;
- микрокистозные ЛМ — представляют собой более мелкие кистозные образования, заполненные жидкостью, и локальные диффузные инфильтративные поражения. Они могут возникать на любом участке кожи или слизистых оболочек, при этом чаще всего локализуются в полости рта, глотке и на языке;
- смешанные ЛМ — характеризуются наличием одновременно макрокистозных и микрокистозных компонентов;
- лимфангиоматоз (также называемый генерализованной лимфатической аномалией или диффузной ЛМ) — включает в себя диффузные и мультицентрические пролиферативные поражения, затрагивающие множество органов.
Этиология
Точная этиология ЛМ неизвестна, но ключевым механизмом признаны нарушения лимфангиогенеза из-за дисфункции сигнальных путей PI3K/AKT и mTOR. Врождённые формы заболевания возникают вследствие внутриутробной блокады лимфотока, причины которой не установлены. Кистозные ЛМ нередко ассоциированы с хромосомными аномалиями, такими как трисомии 13, 18 и 21, а также с синдромами Нунан, Тёрнера и Дауна[1][3].
Приобретённые ЛМ могут развиваться после травм, операций или на фоне хронического лимфостаза, повреждающих лимфодренажную систему. Инфекция или кровоизлияние в мальформацию, как описано в литературе, способны вызывать её быстрый рост[1].
Патогенез
В основе развития ЛМ лежат молекулярно-генетические нарушения, возникающие на разных этапах формирования лимфатической системы[2][4]:
- наиболее часто обнаруживаются мутации в гене PIK3CA, который кодирует один из важнейших регуляторных белков внутриклеточной передачи сигнала. Эти мутации приводят к стойкой активации сигнального пути PI3K/AKT/mTOR, что вызывает неконтролируемое деление, повышенную способность к разрастанию и выживанию лимфатических эндотелиальных клеток. Из-за этого формируются аномальные лимфатические сосуды, которые не способны функционировать должным образом;
- помимо этого, в формировании ЛМ участвует и сигнальный путь RAS/RAF/MEK/ERK. Мутации в гене NRAS обнаруживаются в эндотелиальных клетках при некоторых формах заболевания, особенно при генерализованной ЛМ и кистозной ЛМ костей. Такие мутации также вызывают избыточную пролиферацию клеток и делают возможным развитие обширных и множественных очагов поражения;
- важную роль играет нарушение регуляции факторов роста сосудов, в первую очередь фактора роста эндотелия сосудов типа C (VEGF-C) и его рецепторов. В норме VEGF-C необходим для правильного формирования лимфатической сети во время эмбрионального развития, однако его избыточная экспрессия в лимфатических эндотелиальных клетках приводит к хаотичному разрастанию лимфатических сосудов;
- согласно современным представлениям, в патогенезе ЛМ также задействованы сигнальный путь Wnt/β-катенин, который контролирует дифференцировку лимфатических сосудов, и воспалительные механизмы. В очагах поражения нередко формируются лимфоидные скопления, напоминающие структуру лимфатических узлов, а также обнаруживаются макрофаги определённого типа (М2), которые выделяют факторы роста и поддерживают воспаление. Это позволяет рассматривать ЛМ не только как порок развития, но и как заболевание, в котором важную роль играет хроническое воспаление;
- некоторые исследования показывают, что в основе заболевания могут лежать нарушения на уровне клеток-предшественников. При микрокистозных формах, которые особенно трудно поддаются лечению, обнаружена особая популяция клеток — лимфатических стволовых клеток-предшественников. Они разбросаны среди аномальных сосудов и, вероятно, служат источником постоянного образования новых очагов, что объясняет высокую частоту рецидивов при таких формах заболевания.
Микроскопически ЛМ характеризуется наличием расширенных лимфатических каналов, расположенных в дерме и нередко распространяющихся в подкожную клетчатку. Более глубокие сосуды имеют крупный калибр и толстые стенки, содержащие гладкомышечные клетки. Просвет каналов заполнен лимфатической жидкостью, в которой часто встречаются эритроциты, лимфоциты, макрофаги и нейтрофилы. Стенки образований выстланы уплощёнными эндотелиальными клетками, а окружающая строма представлена соединительной тканью с наличием множества лимфоидных и других воспалительных клеток. В некоторых случаях отмечаются акантоз и гиперкератоз прилегающего эпидермиса[5].
Эпидемиология
ЛМ относятся к редким сосудистым образованиям: они составляют 4 % всех сосудистых опухолей и около 25 % всех доброкачественных сосудистых опухолей у детей, а общая распространённость оценивается в 1 случай на 2000-4000 новорождённых. Хотя ЛМ может проявиться в любом возрасте, чаще всего заболевание выявляется в перинатальном периоде или в раннем детстве. Данные о гендерных различиях противоречивы: большинство исследований указывают на равную распространённость у лиц мужского и женского пола, однако некоторые авторы сообщают о преобладании заболевания у женщин, в то время как другие приводят соотношение 3:1 в пользу мужчин[2][5].
Диагностика
Клинически ЛМ проявляется множественными сгруппированными или рассеянными везикулярными папулами с лимфатическим или геморрагическим содержимым. В области гениталий поверхность может быть бородавчатой. Приобретённая форма чаще всего локализуется в подмышечных, паховых областях и на гениталиях, нередко в сочетании с лимфедемой. Сопутствующие симптомы могут включать зуд, боль, жжение, лимфорею, инфицирование, а также косметические дефекты[3][5].
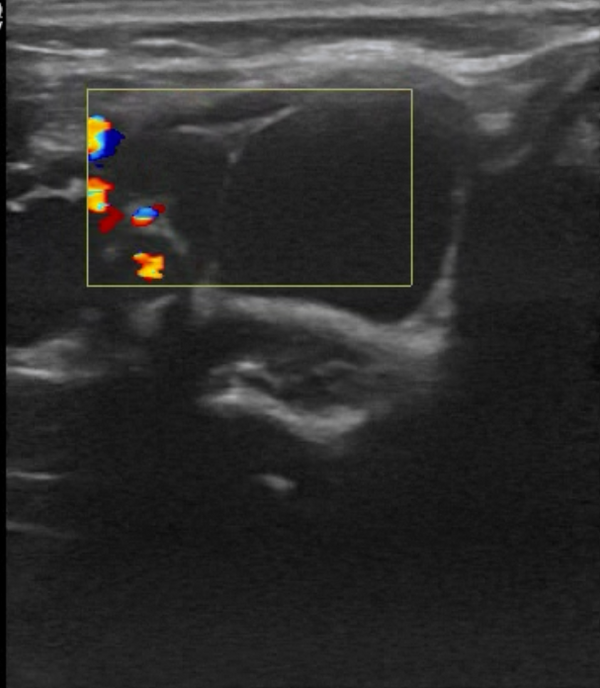
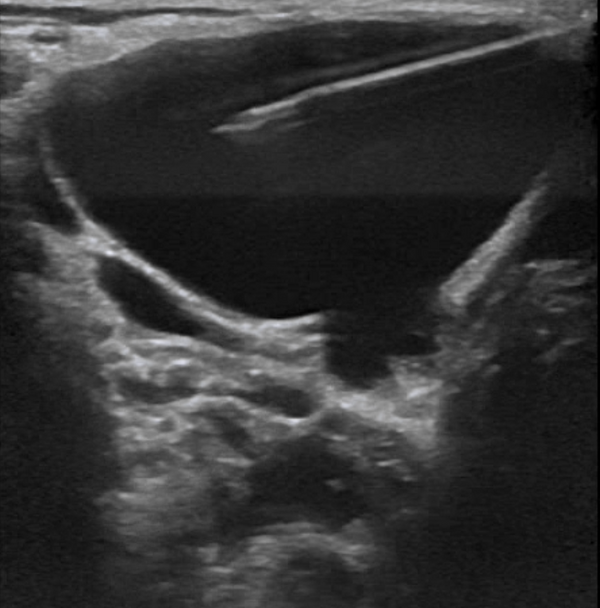
Ультразвуковое исследование: ЛМ классифицируются по данным исследования как макрокистозные, когда отдельные аномальные каналы превышают 10 мм в диаметре, и как микрокистозные, когда отдельные каналы имеют размер менее 10 мм; возможно также сочетание обоих типов. Макрокистозные формы визуализируются как многодольчатые кистозные образования, тогда как микрокистозные очаги выглядят нечёткими и гиперэхогенными из-за множества перегородок между мелкими стенками кист. Микрокистозные формы обычно характеризуются большей инфильтрацией и склонностью к внутренним кровоизлияниям. Смешанные очаги включают как кистозные, так и солидные компоненты, что связано с размером кист и их формой при ультразвуковом исследовании. Цветовое допплеровское картирование позволяет выявлять сосудистые каналы внутри перегородок. В случаях геморрагических или воспалительных осложнений в кистах могут наблюдаться уровни жидкости[6].
При компьютерной томографии большинство ЛМ визуализируются как однородные кистозные образования, однако некоторые могут выглядеть неоднородными из-за наличия в очагах белковых, жидких, кровяных или жировых включений. Кистозные ЛМ обычно имеют чёткие контуры, мультикистозное строение и могут демонстрировать слабое усиление перегородок или стенки после внутривенного введения контрастного препарата[6].
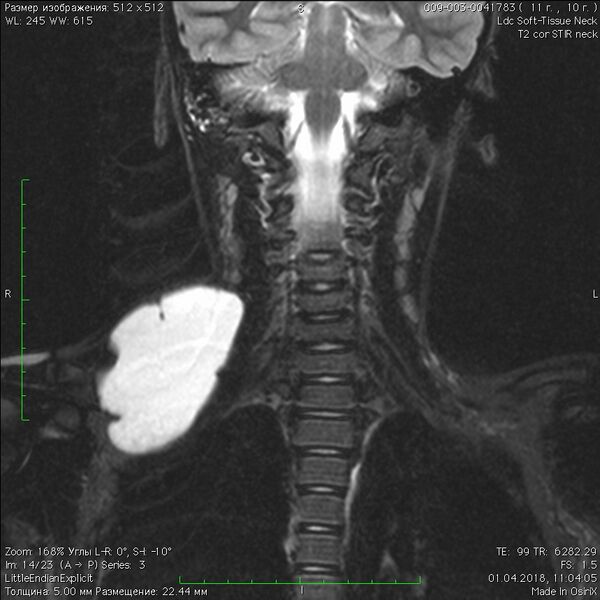
При магнитно-резонансной томографии очаги имеют многодольчатое перегородчатое строение. Они характеризуются изо- или гипоинтенсивным сигналом на Т1-взвешенных изображениях и гиперинтенсивным сигналом на Т2-взвешенных изображениях, а также в режиме подавления сигнала от жира, поскольку эти кистозные образования могут быть различных размеров и часто заполнены жидкостью. Внутри очагов могут наблюдаться уровни жидкости. Чистые ЛМ не накапливают контрастный препарат внутри, так как полностью состоят из полостей, заполненных жидкостью и не сообщающихся с венозной системой. Контрастные препараты усиливают сигнал от периферических стенок и перегородок очага, причём усиление капсул и стенок особенно выражено при макрокистозных формах. Микрокистозные ЛМ не демонстрируют значимого усиления. Также может наблюдаться окружающий отёк (лимфедема)[6].
Дерматоскопия: описываются два различных дерматоскопических паттерна: жёлтые лакуны, окружённые бледными перегородками без включения крови, а также жёлто-розовые лакуны, чередующиеся с тёмно-красными или синеватыми лакунами, что соответствует наличию кровяных включений. Также важным дерматоскопическим признаком является феномен «гипопиона» — переход цвета от тёмного к светлому в некоторых лакунах[3].
Дифференциальная диагностика
Дифференциальная диагностика ЛМ проводится со следующими заболеваниями[3][5]:
- меланома кожи;
- опухоль Дабска;
- герпетиформный дерматит;
- кожные проявления простого герпеса;
- липомы;
- кожные проявления метастатических опухолей;
- кожные проявления нейрофиброматоза 1-го типа;
- опоясывающий лишай;
- лимфангиэктазия;
- синдром Стюарта — Тривса.
Осложнения
ЛМ в зависимости от локализации могут приводить к различным осложнениям. При расположении в области головы и шеи они способны вызывать дисфагию, сдавление дыхательных путей, проблемы с кормлением, ограничение подвижности шеи, а также синдром верхней полой вены. При локализации в брюшной полости или забрюшинном пространстве ЛМ могут становиться причиной кишечной непроходимости, заворота кишки, ишемии кишки, портальной гипертензии, обструкции мочевыводящих путей, болей в животе или его вздутия[1].
Лечение
Медикаментозная терапия ЛМ включает использование различных групп препаратов[2]:
- ингибиторы фосфодиэстеразы-5: вызывают расслабление гладкой мускулатуры, улучшают лимфатический дренаж. Микрокистозные формы могут быть резистентны к данному лечению;
- неселективные бета-адреноблокаторы: снижают экспрессию факторов VEGF, угнетая ангиогенез. В экспериментах подавляют пролиферацию, миграцию и дифференцировку эндотелиальных клеток;
- ингибиторы mTOR: блокируют сигнальный путь PI3K/AKT/mTOR, подавляют экспрессию PROX1 и VEGFR-3, избирательно угнетают рост аномальных лимфатических сосудов. Эффективны при микрокистозных формах;
- таргетные препараты: ингибиторы PI3K, AKT, MAPK, тирозинкиназ, VEGF-A, а также модуляторы BMP, Wnt, ингибиторы JAK, блокаторы кальциевых каналов и активаторы калиевых каналов находятся на разных стадиях исследований.
К возможным методам хирургического лечения ЛМ относятся[2]:
- иссечения ЛМ остаётся методом выбора. Однако ввиду инфильтративного роста и близости к важным структурам полное удаление часто невозможно;
- склеротерапия: применяется при невозможности полного хирургического удаления или высокой сложности операции. Методика эффективна преимущественно при макрокистозных формах, при микрокистозных — значительно менее эффективна;
- радиочастотная абляция: разрушает ткань очага с минимальным повреждением окружающих структур. Применяется как метод выбора при микрокистозных формах в полости рта и глотки, особенно на языке. Позволяет выполнить субмукозную резекцию крупных образований, обтурирующих глотку, с остановкой кровотечения и сохранением важных анатомических структур.
Прогноз
ЛМ представляют собой доброкачественные новообразования и характеризуются благоприятным прогнозом. Риск злокачественной трансформации крайне низок (единичные случаи).
Кожные формы заболевания крайне редко влияют на общее самочувствие пациентов. Пациенты, как правило, ведут полноценную здоровую жизнь и обращаются за медицинской помощью преимущественно по косметическим соображениям. ЛМ имеют высокую склонность к местному рецидивированию, если не удалены полностью[5].
Диспансерное наблюдение
Пациентам с ЛМ показано диспансерное наблюдение с привлечением педиатра или терапевта и профильного хирурга, в зависимости от зоны поражения с проведением контрольных обследования, частота и объём которых определяются индивидуально[5][7].
Профилактика
Специфической профилактики возникновения ЛМ не существует. При подозрении на патологию при пренатальном ультразвуковом скрининге, антенатальная тактика заключается в плановом рациональном ведении беременности[7].
Примечания
Литература
- Hoang V. T., Nguyen M. D., Van H. A. T., et al. Review of diagnosis, differential diagnosis, and management of retroperitoneal lymphangioma (англ.) // Japanese Journal of Radiology. — 2023. — Vol. 41. — P. 283—301. — doi:10.1007/s11604-022-01356-0.
- Bochor N., Gera P. Exploring Lymphangioma: A Synthesis of the Literature and Clinical Perspectives (англ.) // Lymphatics. — 2025. — Vol. 3, no. 1. — P. 4. — doi:10.3390/lymphatics3010004.
- Liu X., Cheng C., Chen K., et al. Recent Progress in Lymphangioma (англ.) // Frontiers in Pediatrics. — 2021. — Vol. 9. — P. 735832. — doi:10.3389/fped.2021.735832.
- Кручинин К. С., Омарова Ж. Р., Соколов Ю. Ю., и др. Лимфатические мальформации (обзор литературы) // Волгоградский научно-медицинский журнал. — 2022. — № 3.