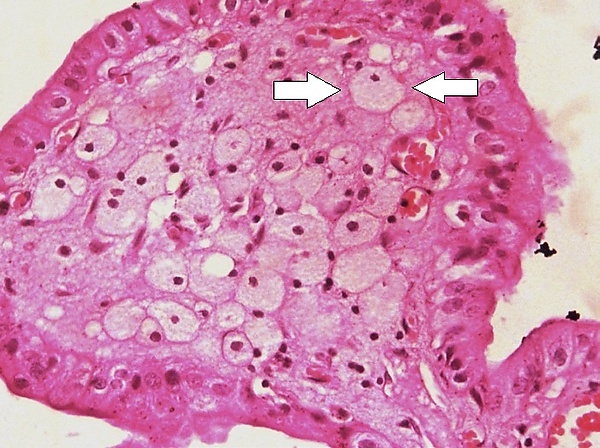
Пенистые клетки
Пе́нистые клетки (син. пе́нистые макрофа́ги, ксанто́мные кле́тки; англ. foam cells, foamy macrophages, lipid-laden macrophages[1]) — макрофаги, способные накапливать липиды в цитоплазме. Участвуют в механизмах развития воспалений, атеросклероза[2], ксантом[3], рака предстательной железы[4] и рака яичника[5].
История
Пенистые клетки впервые были обнаружены в атеросклеротических бляшках и получили своё название из-за внешнего вида — под микроскопом они напоминали пену. В XIX веке появилась гипотеза о том, что пенистые клетки образуются из макрофагов субэндотелиального пространства сосудов в результате захвата окислённых липопротеинов низкой плотности. Позже стало известно, что макрофаги превращаются в пенистые клетки при воспалительных болезнях: в синовиальной жидкости — при ревматоидном артрите, в жировой ткани — при сахарном диабете, в почках — при острой и хронической почечной недостаточности, в головном мозге — при энцефалитах (например, при инфицировании Chlamydia pneumoniae и Mycobacterium tuberculosis, вирусом иммунодефицита человека, цитомегаловирусом[6][2].
Развитие
Макрофаги трансформируются в пенистые клетки в острую фазу воспаления. В эту фазу повреждённые ткани выделяют макрофаг-колониестимулирующий фактор, который запускает дифференцировку моноцитов в макрофаги. Макрофаги отвечают снижением экспрессии АТФ-связанных кассетных транспортёров холестерина А1 и G1 и аполипопротеина Е, усилением экспрессии ферментов синтеза холестерина[6]. Активация провоспалительных сигнальных путей инактивирует липидные сенсоры макрофагов, контролирующие липидный обмен, и макрофаги начинают накапливать липиды. Липидные включения усиливают воспалительные сигнальные каскады, усиливающие защитную функцию макрофагов[2].
Считается, что M. tuberculosis запускает нарушение липидного обмена через толл-подобные рецепторы 2. В исследованиях показано, что инфицирование макрофагов M. tuberculosis и трансфекция экзогенной 15-липооксигеназы в пенистые клетки запускает образование и накопление эфиров простагландина Е2 и 15-гидроксиэйкосатетраеновой кислоты в липидных включениях пенистых клеток. В эксперименте на мышах Ch. pneumoniae вызывали «инфекционный» атеросклероз. Бактерии активировали макрофаги через толл-подобные рецепторы 2 и 4, адаптер белка раннего ответа миелоидной дифференцировки, сигнальные белки IRF3 и TRIF и активацию фермента JNK, что приводит к снижению экспрессии рецепторов активаторов пролиферации пероксисом-γ1[6].
Некоторые вирусы перепрограммируют липидный обмен в макрофагах. Вирусы иммунодефицита человека, Эбола, Марбурга, гриппа используют рафты, обогащённые холестерином и сфингомиелином для проникновения в клетку, сборки и выхода из клетки. Вирусы иммунодефицита человека нуждаются в переносе холестерина в специализированные рафты на стадии сборки вирусных частиц[6].
Высокая концентрация холестерина при атеросклерозе подавляет в макрофагах экспрессию классических рецепторов липопротеинов низкой плотности, поэтому макрофаги преимущественно поглощают модифицированные липопротеины. Этот процесс не контролируется по механизму отрицательной обратной связи. В результате макрофаги пересыщаются холестерином и превращаются пенистые клетки. Пенистые клетки вначале удаляют избыток холестерина из крови, но теряют способность к миграции и начинают откладываться в стенке сосудов, образуя жировые полоски[7][8].
Клиническое значение
Пенистые клетки не просто накапливают липиды — они участвуют в развитии и завершении острого воспаления. В начале воспаления макрофаги М1 и пенистые клетки активно поглощают патогены, продуцируют провоспалительные факторы и кислородные метаболиты. На 1—3-е сутки пенистые клетки начинают секретировать противовоспалительные факторы, которые привлекают моноциты из кровеносных сосудов (макрофаги М2). Повышенная концентрация холестерина и жирных кислот в пенистых клетках активирует апоптоз: на поверхности клеток появляется фосфолипид фосфатидилсерин — сигнал макрофагам М2 к поглощению пенистых клеток. После поглощения пенистых клеток макрофаги М2 секретируют медиаторы восстановительной стадии воспаления[2][6]. Однако в некоторых случаях пенистые клетки могут провоцировать обострение хронического воспаления — при несостоятельном апоптозе, нарушении баланса секреции про- и противовоспалительных медиаторов в макрофагах, дефекте клиренса апоптозных клеток[6].
При атеросклерозе тромбоциты и эндотелиоциты активируют пенистые клетки жировых полосок. В ответ пенистые клетки вырабатывают тромбоцитарный фактор роста, интерлейкин 1, окись азота, простациклин, трансформирующий фактор роста β и фактор некроза опухолей α. Эти вещества привлекают гладкомышечные клетки и лейкоциты. Гладкомышечные клетки мигрируют из медии артерий в интиму, разрастаются и производят макромолекулы внеклеточного матрикса, а лейкоциты поддерживают воспаление. Кроме того, пенистые клетки продуцируют металлопротеиназы и катепсины матрикса. Эти ферменты разрушают коллаген и эластин, что снижает прочность фиброзной бляшки и повышает вероятность её разрыва[7][9].
На ранних стадиях ксантомы представляют собой скопление пенистых клеток. В старых очагах преобладают фибробласты и новообразованные коллагеновые волокна, окружающие группы пенистых клеток. В дальнейшем фиброзная ткань замещает пенистые клетки[3].
В протоках предстательной железы за пределами опухолевой ткани выявлены участки с крупными пенистыми клетками. Учёные считают эти клетки негативным прогностическим фактором и возможной мишенью для разработки лечения[4].
Гигантские CD68-позитивные макрофаги с пенистой цитоплазмой характерны для IIIC и IV стадии рака яичника. Эти клетки статистически значимо ассоциировались с прогрессированием и рецидивированием рака яичника[5].
Примечания
Литература
- Душкин М. И. Макрофаг/пенистая клетка как атрибут воспаления: механизмы образования и функциональная роль // Биохимия. — 2012. — Т. 77, № 4. — С. 419–432.
- Мельдеханов Т. Т., Есиргепова С. Р., Пиржанов Б. Т., и др. К патогенезу и морфогенезу атеросклероза // Актуальные проблемы теоретической и клинической медицины. — 2021. — № 4. — С. 29—37. — doi:10.24412/2790-1289-2021-42937.