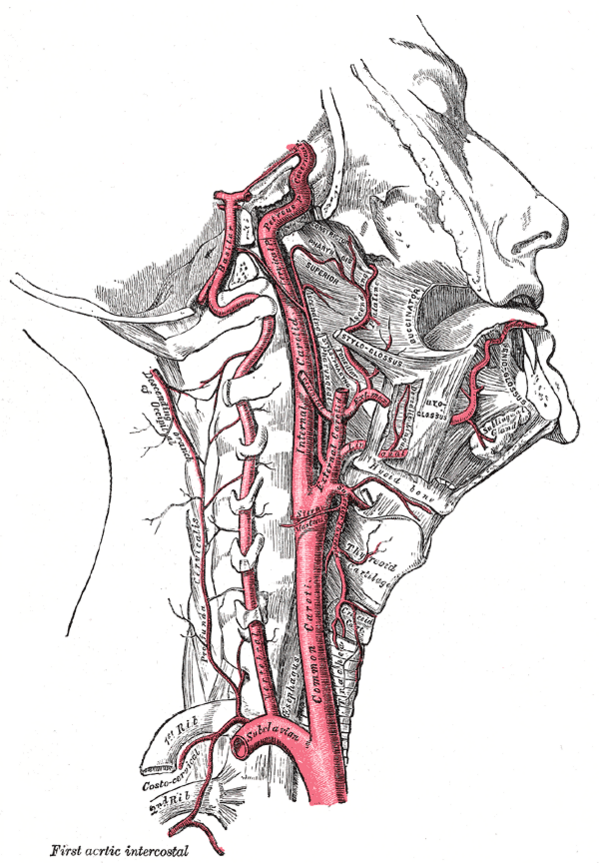
Стеноз сонных артерий
Стено́з со́нных арте́рий (ССА) — состояние, характеризующееся сужением просвета сонных артерий вследствие формирования атеросклеротических бляшек, которые являются проявлением системного атеросклеротического процесса. Клинически ССА проявляется транзиторными ишемическими атаками либо ишемическими инсультами[1].
Что важно знать
История
В 1658 году швейцарский патолог Вефер впервые предположил связь между симптомами недостаточности мозгового кровообращения и патологией сонных артерий, постулировав, что причиной инсульта является нарушение кровоснабжения мозга. В 1664 году Уиллис подтвердил клиническое значение артериального круга мозга, описав случаи бессимптомной окклюзии внутренней сонной артерии благодаря коллатеральному кровотоку. В XVIII—XIX веках ван Свитен выдвинул гипотезу об эмболах, отходящих от артерии, а позже Вирхов ввёл понятия тромбоза, ишемии и эмболии, а также описал связь эмбола в сонной артерии с односторонней слепотой. В начале XX века Хиари разработал тромбоэмболическую теорию, показав, что атеросклероз бифуркации сонных артерий является важнейшим источником церебральных эмболий, а Хант доказал, что как окклюзия, так и ССА могут вызывать острое нарушение мозгового кровообращения. С развитием ангиографии в 1937 году Монниц и коллеги визуализировали окклюзии шейного отдела внутренней сонной артерии, а в 1951 году Фишер опубликовал знаковую работу, детально описав связь атероматозных поражений сонных артерий с транзиторными и стойкими церебральными симптомами, что привлекло внимание к этим сосудам как к основному субстрату инсульта и дало толчок развитию хирургической реконструкции сонных артерий[3].
Классификация
По клиническому течению выделяют[4]:
- симптомный ССА;
- асимптомный ССА.
Этиология
ССА является следствием системного атеросклероза, поэтому любой фактор риска, предрасполагающий пациента к развитию и прогрессированию заболевания, может способствовать развитию ССА. К таким факторам риска относятся курение, гиперлипидемия, мужской пол, сахарный диабет, злоупотребление алкоголем, артериальная гипертензия и пожилой возраст. У некоторых пациентов, особенно у молодых женщин со ССА, значительно более важную роль играет фибромускулярная дисплазия[5].
Патогенез
Патогенез ССА обусловлен развитием атеросклероза. Эндотелий сонной артерии при атеросклерозе повреждается в течение длительного времени, при этом факторами риска выступают гиперлипидемия, повышенное артериальное давление, курение и иммунный ответ. В результате повышается проницаемость сосудистого эндотелия и усиливается адгезия лейкоцитов и моноцитов. Активируются макрофаги и формируется фиброзная капсула, содержащая гладкомышечные клетки, коллаген и эластин. Макрофаги и гладкомышечные клетки захватывают липиды, гладкомышечные клетки быстро пролиферируют, происходит отложение внеклеточного матрикса. В ходе этой серии воспалительных реакций секретируются различные деструктивные ферменты, которые вызывают разрыв атеросклеротической бляшки, в результате чего в кровоток выбрасываются различные тромбогенные вещества, что приводит к образованию тромбов и стенозу или окклюзии сонной артерии[6].
Эпидемиология
Распространённость симптомного ССА составляет 6 случаев на 100 000 населения, а мировая распространённость бессимптомного хронического стеноза неизвестна и может быть выше. Расчётная распространённость тяжёлого бессимптомного каротидного стеноза (70 % и более) варьируется от 0,1 % до 3,1 %, увеличивается с возрастом и обусловливает 0,7 % риска инсульта в популяции. Несмотря на то, что пациенты чёрной расы имеют более высокий риск инсульта по сравнению с белыми пациентами, у них отмечается более низкая частота тяжёлого стеноза. Мужчины имеют более высокую распространённость ССА по сравнению с женщинами.[5][7].
Распространённость симптомного ССА в России достоверно не определена, однако, известно, что ССА является основной причиной развития острого нарушения мозгового кровообращения. Общая распространённость бессимптомного ССА (закупорка и стеноз прецеребральных и церебральных артерий, не приводящих к инфаркту мозга) в среднем по России в 2022 г. составила 23,3 на 100 тыс. взрослого населения[8][9].
Диагностика
Клиническая картина ССА определяется преимущественно наличием или отсутствием эпизодов церебральной ишемии в анамнезе. При объективном осмотре пациентов с подозрением на данную патологию ключевое значение имеет оценка неврологического статуса, которая может выявить признаки ранее перенесённого нарушения мозгового кровообращения. К таким признакам относятся гемипарез, гемигипестезия, транзиторные нарушения памяти, дезориентация во времени и пространстве, речевые расстройства, изменение походки, а также другие очаговые неврологические симптомы, указывающие на состоявшийся ишемический эпизод в каротидном бассейне[1].
Важным компонентом физикального обследования остаётся аускультация артерий шеи с целью выявления систолического шума. Данный метод является стандартным при осмотре пациентов, однако его диагностическая ценность в отношении гемодинамически значимого стеноза сонных артерий ограничена. Обнаружение систолического шума над бифуркацией общей сонной артерии в большей степени коррелирует с наличием системного атеросклеротического поражения, нежели с локальным стенозом[1].
Биохимический анализ крови: характерны явления дислипидемии, гипергликемии и повышения концентрации креатинина и мочевины[1].
При компьютерной томографии характерными изменениями при ССА являются визуализация зон сниженной плотности в головном мозге, соответствующих инфаркту в бассейне средней мозговой артерии, а также непосредственное выявление окклюзии или стеноза внутренней сонной артерии. Метод позволяет оценить плотные кальцификаты в области бифуркации сонной артерии, изъязвления атеросклеротической бляшки, которые могут быть источником эмболии, а также визуализировать тромбоз сонной артерии[10].
Магнитно-резонансная томография: позволяет оценить степень сужения сосуда в соответствии с установленными критериями, а также выявить признаки нестабильности атеросклеротической бляшки. Применение диффузионно-взвешенных последовательностей даёт возможность верифицировать очаговую ишемию головного мозга и дифференцировать её механизмы: у пациентов с нестабильными бляшками чаще наблюдается картина диссеминированных мелкоочаговых инфарктов, тогда как при гемодинамически значимом стенозе характерно формирование инфарктов в пограничных зонах кровоснабжения между сосудистыми бассейнами. Комплексная оценка данных магнитно-резонансной ангиографии и перфузионных методик позволяет не только подтвердить наличие стеноза, но и уточнить его патофизиологическую значимость, что имеет важное значение для определения тактики ведения пациента[10].
Ультразвуковое исследование: в В-режиме симптомные атеросклеротические бляшки чаще имеют гипоэхогенную структуру и высокую степень стеноза, тогда как асимптомные — гиперэхогенны и умеренно сужают просвет. Допплерография позволяет количественно оценить степень стеноза по пиковой систолической и конечной диастолической скоростям, а также их отношению в общей и внутренней сонных артериях. Транскраниальная допплерография выявляет интракраниальные стенозы, оценивая их гемодинамическую значимость[10].
Радионуклидные методы, такие как однофотонная эмиссионная компьютерная томография и позитронно-эмиссионная томография, позволяют дифференцировать участки ишемии и завершённого инфаркта головного мозга. С помощью динамической оценки церебрального кровотока с использованием радиофармпрепаратов в сочетании с фармакологической нагрузкой ацетазоламидом возможно выявление гемодинамически значимых стенозов и оценка цереброваскулярного резерва[10].
Ангиография: метод даёт возможность оценить характер поражения стенки сонной артерии — гладкий, неровный, фокальный или протяжённый, а также визуализировать коллатеральное кровообращение и постстенотическое расширение[10].
Дифференциальная диагностика
Дифференциальная диагностика ССА проводится со следующими заболеваниями[5][7]:
- расслоение сонной артерии;
- фибромускулярная дисплазия;
- клапанные пороки сердца;
- аритмии (особенно фибрилляция предсердий);
- пристеночный тромбоз;
- болезнь Такаясу;
- гигантоклеточный артериит;
- васкулиты и артерииты;
- врождённые аномалии сосудов головного мозга;
- заболевания соединительной ткани;
- гиперкоагуляционные состояния.
Осложнения
Лечение
Лечение ССА направлено на снижение риска инсульта и включает медикаментозную терапию и хирургическую реваскуляризацию. Медикаментозная коррекция заключается в высокоинтенсивной терапии статинами. Выбор антитромботической терапии зависит от генеза ишемического события: при кардиоэмболическом варианте показаны антикоагулянты, при атеротромботическом — антиагреганты. Также пациентам с ССА показана антигипертензивная терапия в случае развития артериальной гипертензии[1].
Хирургическое лечение показано пациентам с асимптомным стенозом более 60 % и симптомным стенозом 50-99 %. Предпочтительным методом является каротидная эндартерэктомия, техника которой (классическая с пластикой заплатой или эверсионная) выбирается с учётом анатомических особенностей и характера поражения. Альтернативой выступает стентирование сонных артерий, которое рекомендуется в анатомически сложных условиях (высокое расположение бифуркации, распространение поражения на интракраниальные отделы), рестенозах после предшествующей эндартерэктомии, а также у пациентов с трахеостомой, лучевым поражением шеи или высоким хирургическим риском. У пациентов с острым инсультом и выраженным неврологическим дефицитом оперативное вмешательство откладывают до стабилизации состояния[1].
Прогноз
Прогноз у пациентов со ССА определяется характером исходного ишемического события и эффективностью проводимой терапии. Риск повторного инсульта после успешно выполненной каротидной эндартерэктомии зависит от того, имела ли место транзиторная ишемическая атака или инсульт: у пациентов, перенёсших транзиторную ишемическую атаку, частота ипсилатерального инсульта составляет 1-2 % в год, тогда как у пациентов с инсультом в анамнезе этот показатель достигает 2-3 % в год. У бессимптомных пациентов с каротидным стенозом годовой риск ипсилатерального ишемического инсульта оценивается в 0,9 %. Важно отметить, что на фоне оптимальной медикаментозной терапии частота инсультов у бессимптомных пациентов с каротидным стенозом имеет устойчивую тенденцию к снижению[5][7].
Диспансерное наблюдение
Диспансерное наблюдение после выявления ССА или выполненных реконструктивных операций носит пожизненный характер. В раннем послеоперационном периоде рекомендовано ограничение интенсивных физических нагрузок в течение 2-3 недель. Частота наблюдения составляет не реже 2 раз в год, при этом пациенты с сочетанной сердечно-сосудистой патологией наблюдаются кардиологом, а в остальных случаях — терапевтом. Контролируемые показатели включают антропометрические данные (индекс массы тела, окружность талии), уровень артериального давления, липидный профиль (холестерин липопротеинов низкой плотности не реже 2 раз в год), а также результаты инструментальных исследований. Ультразвуковое дуплексное сканирование брахиоцефальных артерий выполняется не реже 1 раза в год. Пациентам, перенёсшим ишемический инсульт или транзиторную ишемическую атаку, показано диспансерное наблюдение невролога в течение 2 лет[1].
Профилактика
Профилактика ССА заключается в профилактике развития атеросклероза и направлена на коррекцию модифицируемых факторов риска и включает немедикаментозные и медикаментозные мероприятия. К немедикаментозным относятся отказ от курения, соблюдение диеты с ограничением насыщенных жиров и простых углеводов, нормализация массы тела, регулярная физическая активность. Медикаментозная профилактика заключается в достижении целевых уровней артериального давления, липидного профиля (преимущественно с использованием статинов) и гликемического контроля при наличии сахарного диабета, а также в назначении антитромбоцитарных препаратов у пациентов с высоким сердечно-сосудистым риском[9].
Примечания
Литература
- Lee Y., Park J. H. Carotid artery stenosis: diagnosis and guidelines for management (англ.) // Journal of Korean Society of Geriatric Neurosurgery. — 2024. — Vol. 20, no. 2. — P. 37—45. — doi:10.51638/jksgn.2024.00080.
- Хорев Н. Г. Изменение подходов к лечению стеноза внутренней сонной артерии // Амбулаторная хирургия. — 2025. — № 1. — doi:10.21518/akh2025-007.
- Чернявский М. А., Иртюга О. Б., Янишевский С. Н., и др. Российский консенсус по диагностике и лечению пациентов со стенозом сонных артерий // Российский кардиологический журнал. — 2022. — Т. 27, № 11. — С. 5284. — doi:10.15829/1560-4071-2022-5284.