Пролин
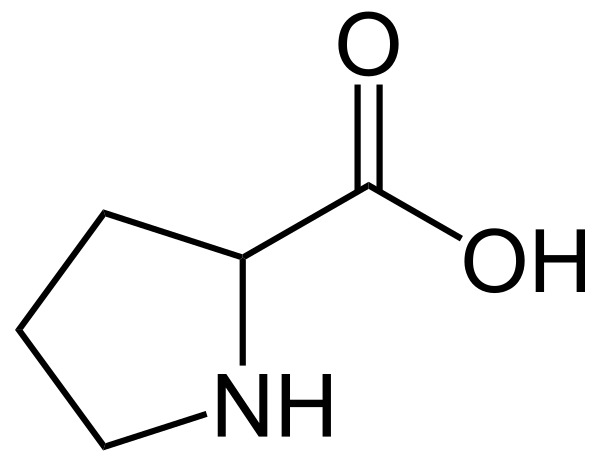
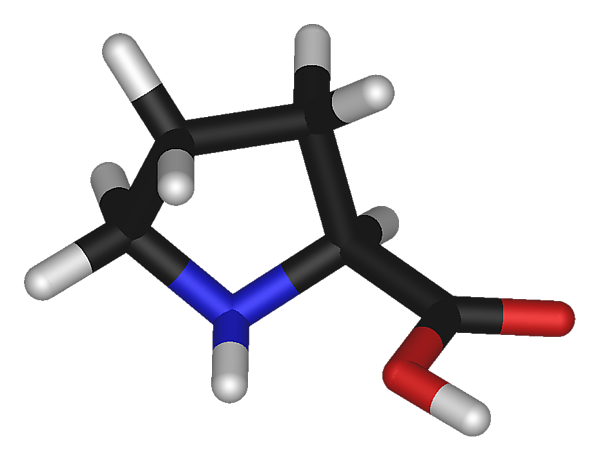
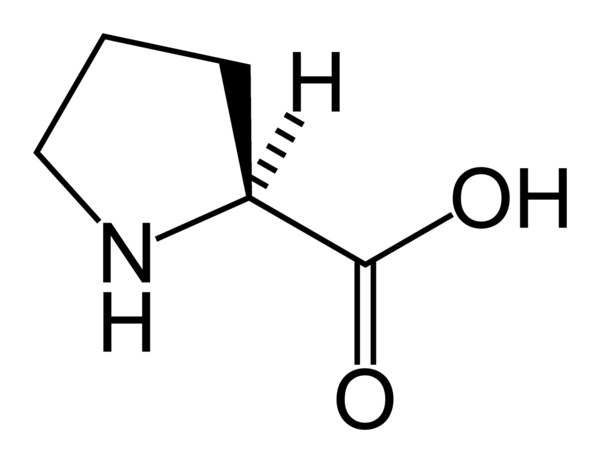
Проли́н (пирролидин-α-карбоновая кислота) — гетероциклическая аминокислота, в которую атом азота входит в составе вторичного, а не первичного, амина. Существует в двух оптически изомерных формах — L и D, а также в виде рацемата.
L-пролин — одна из двадцати протеиногенных аминокислот. Считается, что пролин входит в состав белков всех организмов. Особенно богат пролином основной белок соединительной ткани — коллаген. В составе белков атом азота в молекуле пролина не связан с атомом водорода, таким образом, пептидная группировка X-Pro не может быть донором водорода при формировании водородной связи. Обладая конформационно жёсткой структурой, пролин сильно изгибает пептидную цепь. Участки белков с высоким содержанием пролина часто формируют вторичную структуру полипролиновой спирали II типа.
Из-за своей структуры пролин иногда называют иминокислотой[1], однако это не соответствует номенклатуре ИЮПАК для иминов[2] и считается устаревшим[3].
Общие сведения
| Пролин | |
|---|---|
| Общие | |
| Систематическое наименование |
L-пирролидин-2- карбоновая кислота |
| Сокращения |
Про, Pro, P CCU,CCC,CCA,CCG |
| Хим. формула | C5H9NO2 |
| Рац. формула | C5H9NO2 |
| Физические свойства | |
| Молярная масса | 115,13 г/моль |
| Плотность | 1,35—1,38 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 221 °C |
| Химические свойства | |
| Константа диссоциации кислоты |
1,99 10,60 |
| Изоэлектрическая точка | 6,3 |
| Классификация | |
| Рег. номер CAS | [147-85-3] |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 614 |
| UNII | DCS9E77JPQ |
| CompTox Dashboard EPA | DTXSID9041104 |
| Рег. номер EINECS | 205—702-2 |
| SMILES | |
| InChI | |
| RTECS | TW3584000 |
| ChEBI | 26271 |
| ChemSpider | 594 |
| ECHA InfoCard | 100.009.264 |
История
В чистом виде пролин впервые получил в 1900 г. немецкий химик-органик Рихард Вильштеттер получивший эту аминокислоту при изучении н-метилпролина. Через год другой немецкий химик — Франц Фишер опубликовал схему синтеза пролина из фталимида пропилмалонового эфира и он же дал название веществу от слова «пирролидин», ядро которого входит в молекулу пролина[4][5].
Физические и химические свойства.
Представляет собой бесцветные, легко растворимые в воде кристаллы, плавящиеся при температуре около 220 °C. Также хорошо растворим в этаноле, хуже — в ацетоне и бензоле, нерастворим в диэтиловом эфире.
В организме пролин синтезируется из глутаминовой кислоты.
Пролин, как и гидроксипролин, в отличие от других аминокислот, не образует с нингидрином пурпура Руэмана[6][7][8], а даёт жёлтое окрашивание.
В составе коллагена пролин при участии аскорбиновой кислоты окисляется в гидроксипролин. Чередующиеся остатки молекулы пролина и гидроксипролина способствуют созданию стабильной трёхспиральной структуры коллагена, придающей молекуле прочность.
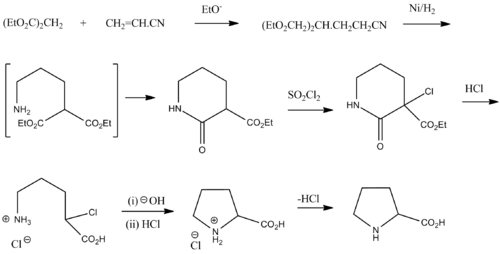
Лабораторный синтез пролина
Рацемическая смесь L- и D-пролина может быть получена из диэтилового эфира малоновой кислоты и акрилонитрила[9]:
Примечания