Синдром Бёрта — Хогг — Дьюбе
Синдро́м Бёрта ― Хогг ― Дьюбе́ (СБХД) — редкое наследственное аутосомно-доминантное заболевание, обусловленное мутациями в зародышевой линии гена-супрессора опухолевого роста FLCN, который кодирует белок фолликулин. Для синдрома характерно образование доброкачественных кожных фиброфолликулом, преимущественно локализующихся на голове и шее, множественных кист в лёгких, а также повышенный риск спонтанного пневмоторакса. Кроме того, у пациентов с этим синдромом часто развиваются опухоли почек различных гистологических типов[2].
Что важно знать
История
Самый ранний возможный случай этого заболевания в медицинской литературе был зафиксирован ещё в 1925 году Бурнье и Рейсеком, которые описали перифолликулярные фибромы на лице 56-летней женщины. Триходискомы впервые были выделены как отдельное явление в 1974 году Закхеймом и Пинкусом, но их связь с синдромом Бёрта — Хогг — Дьюбе (СБХД) была установлена только позднее. Первый случай СБХД с системными проявлениями описали Хорнштейн и Кникенберг: они обнаружили характерные фиброфолликуломы у двух сиблингов и их отца, у которых также были выявлены полипы толстой кишки. Синдром был впервые детально описан в 1977 году тремя канадскими врачами — Артуром Бёртом, Джорджиной Хогг и Уильямом Дьюбе. Они изучали семью с наследственным раком щитовидной железы и обнаружили, что у многих её членов присутствовали фиброфолликуломы, триходискомы и акрохордоны, которые впоследствии стали классическими симптомами этого заболевания. Первый случай спонтанного пневмоторакса, ассоциированного с СБХД, был описан в 1986 году, а первый случай рака почки — в 1993-м. Наличие лёгочных кист у пациентов с СБХД подтвердили в 1999 году[2][3][4].
Этиология
Генетический локус, связанный с СБХД, был картирован на 17-й хромосоме в 2001 году. Год спустя было установлено, что причиной заболевания являются мутации в гене FLCN, кодирующем белок фолликулин. На 2025 год это единственный известный ген, ассоциированный с данным синдромом. В семьях с СБХД выявлено более 200 патогенных вариантов мутаций (сдвиг рамки считывания, нонсенс-мутации, нарушения сплайсинга). Большинство из них приводят к укорочению белка, что предположительно вызывает потерю функции фолликулина. Хотя мутации часто наследуются от поражённого родителя, возможны и de novo случаи у пациентов без семейного анамнеза[5].
На сегодняшний день чёткой корреляции между типом или локализацией мутаций в FLCN и фенотипическими проявлениями не установлено. Пенетрантность БХД считается высокой, но экспрессивность заболевания значительно варьирует как между членами одной семьи, так и между разными семьями. У некоторых носителей мутаций FLCN единственным клиническим проявлением являются лёгочные кисты или рецидивирующие пневмотораксы[5].
Патогенез
Ген FLCN классифицируется как ген-супрессор опухолевого роста. Точная функция фолликулина, который экспрессируется в большинстве тканей, до конца не изучена. Считается, что он участвует в регуляции роста и пролиферации клеток через взаимодействие с сигнальным путём mTOR (мишень рапамицина у млекопитающих)[5].
Механизмы образования лёгочных кист при нарушении функции фолликулина остаются не до конца ясными. Предполагается, что в этом процессе задействованы несколько нарушенных сигнальных путей, включая mTOR и AMP-активируемую протеинкиназу, а также нарушения клеточной адгезии и дисбаланс в гомеостазе внеклеточного матрикса. Также имеется гипотеза о том, что кисты могут формироваться вследствие дефицита межклеточной адгезии, который со временем приводит к расширению альвеолярных пространств — особенно в тех участках лёгких, где объём альвеол изменяется во время дыхательного цикла. Эта «гипотеза растяжения» объясняет преимущественно субплевральное и базальное расположение кист при СБХД[5].
Новые данные свидетельствуют о сниженной активности Wnt-сигнального пути в мезенхимальных клетках с дефицитом FLCN, что связано с ингибирующим эффектом транскрипционного фактора TFE3. Эти находки позволяют предположить, что нарушение Wnt-зависимой межклеточной коммуникации в процессе развития лёгких может способствовать формированию кист при СБХД[5].
Патогенез рака почки при СБХД связан с нарушением функции гена FLCN. Рак почки у пациентов с СБХД существенно отличается от других форм. Помимо характерного гистологического строения (преимущественно хромофобные и смешанные онкоцитарные/хромофобные опухоли), эти новообразования демонстрируют аномалии числа копий ДНК в дополнение к соматическим мутациям FLCN. В отличие от спорадических случаев рака почки, которые обычно происходят из клеток проксимальных канальцев, опухоли при СБХД берут начало из дистальных отделов нефрона[5].
Эпидемиология
СБХД представляет собой редкое генетическое заболевание с распространённостью в общей популяции около 1,86 случая на 1 миллион человек, без существенных гендерных различий — 1,86 на миллион у мужчин и 1,88 на миллион у женщин[6].
Диагностика
СБХД характеризуется значительной фенотипической гетерогенностью. Носители мутаций гена FLCN могут быть полностью бессимптомными или демонстрировать различные комбинации кожных, лёгочных и почечных проявлений. Классическая клиническая картина включает кожные поражения (фиброфолликуломы) и рецидивирующие спонтанные пневмотораксы, развивающиеся на фоне множественных лёгочных кист. Однако в некоторых случаях заболевание может проявляться исключительно лёгочными кистами или повторяющимися пневмотораксами без каких-либо кожных или почечных симптомов[5].
- Лёгочные проявления: более чем у 80 % пациентов с СБХД выявляются множественные двусторонние лёгочные кисты. Хотя эти изменения могут обнаруживаться уже у молодых взрослых, в большинстве случаев они проявляются в возрасте 40—50 лет. Характерной особенностью кист при БХД является их склонность к разрывам, что приводит к развитию спонтанного пневмоторакса с высоким риском рецидивов. За исключением эпизодов пневмоторакса, лёгочные кисты при БХД обычно протекают бессимптомно или сопровождаются лишь незначительными проявлениями в виде лёгкого кашля или одышки при физической нагрузке. Это характерно даже для пациентов с обширным поражением лёгких. В литературе описаны отдельные случаи сочетания СБХД с лёгочной аденокарциномой, атипичной аденоматозной гиперплазией и микронодулярными гиперплазиями пневмоцитов. Однако на 2025 год чёткая связь между БХД и развитием лёгочных опухолей не установлена[5].
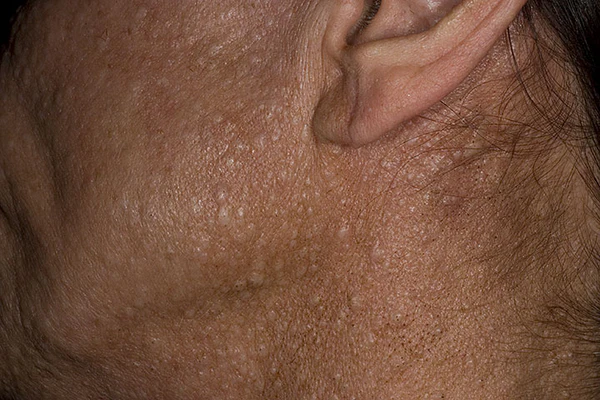
- Кожные проявления: характерны фиброфолликуломы и триходискомы, которые представляют собой гамартомы эпителия волосяного фолликула и перифолликулярной ткани. Фиброфолликуломы и триходискомы выглядят как белесоватые или телесного цвета куполообразные папулы диаметром 2—3 мм с гладкой поверхностью. Типичная локализация — лицо, заушная и шейная области, верхняя часть груди. Третьим по частоте кожным проявлением являются акрохордоны — небольшие мягкие доброкачественные образования телесного цвета на тонкой ножке, расположенные преимущественно на веках, шее и в подмышечных областях. Кожные поражения обычно выявляются в возрасте 30—40 лет, крайне редко до 25 лет. Количество элементов может варьироваться: от единичных до нескольких сотен. Описаны и другие кожные проявления СБХД: комедоноподобный и кистозный варианты фиброфолликулом, перифолликулярные фибромы, соединительнотканные невусы, множественные ангиоматозные узелки, липомы, ангиолипомы и ангиофибромы[5].
- Опухоли почки представляют наиболее серьёзное проявление СБХД. Они развиваются примерно у 30 % пациентов с этим синдромом, причём риск развития рака почки у больных СБХД в семь раз выше по сравнению с общей популяцией. Характерной особенностью СБХД-ассоциированных почечных опухолей является их мультифокальный и двусторонний характер (более чем в половине случаев), а также разнообразное гистологическое строение. Злокачественный потенциал этих опухолей варьирует от доброкачественных онкоцитом (около 5 % случаев) до злокачественных почечно-клеточных карцином (примерно 70—80 % случаев)[5].
- Иные проявления: у пациентов с СБХД в литературе описаны различные доброкачественные и злокачественные опухоли (онкоцитома околоушной железы, рабдомиома, аденома паращитовидной железы, рак молочной железы, колоректальный рак). Однако на 2025 год убедительных доказательств причинной связи этих опухолей с мутациями гена FLCN не установлено[5].
Компьютерная томография является ключевым методом диагностики. В лёгких характерно наличие множественных тонкостенных двусторонних кист на фоне нормальной лёгочной ткани. Кисты демонстрируют значительное разнообразие по размеру (от нескольких миллиметров до 2 см и более, хотя большинство не превышает 1 см), форме (круглые, овальные или неправильные) и количеству (от единичных до более 400 образований). Типичными особенностями являются тонкие равномерные стенки кист и преимущественное расположение в базальных, субплевральных и парамедиастинальных отделах лёгких. Крупные кисты часто имеют сложное дольчатое строение с множественными перегородками. У большинства пациентов обнаруживается около 20 кист, занимающих не более 30 % объёма лёгких[5].
При спирометрии выявляются сохранные значения ОФВ1, ФЖЕЛ, их соотношения и общей ёмкости лёгких. Средний остаточный объём часто умеренно увеличен[5].
При подозрении на опухолевые образования почек проводится гистологическое исследование ткани почки, полученного путём биопсии[5].
Диагноз подтверждается выявлением мутации в гене FLCN методом секвенирования[5].
Основные критерии[7]:
- Наличие ≥ 5 фиброфолликулом или триходиском, из которых хотя бы одна:
- подтверждена гистологически;
- появилась во взрослом возрасте.
- Выявление патогенной мутации в гене FLCN.
Второстепенные критерии:
- Множественные лёгочные кисты, характеризующиеся:
- двусторонним расположением;
- преимущественно базальной локализацией.
- Рак почки, если:
- диагностирован в возрасте < 50 лет;
- имеет мультифокальный или двусторонний характер;
- обладает смешанной хромофобной и онкоцитарной гистологией.
- Наличие СБХД у родственника первой степени родства.
Для диагностики СБХД требуется соответствие либо одному основному критерию, либо двум второстепенным критериям. При этом отрицательный результат генетического теста не исключает диагноза, поскольку до 40 % клинически подтверждённых случаев могут не иметь обнаруживаемых мутаций[7].
Дифференциальная диагностика
Дифференциальная диагностика проводится со следующими состояниями[5][7]:
- синдром Каудена;
- туберозный склероз;
- синдром Брука — Шпиглера;
- лимфангиолейомиоматоз;
- эмфизема лёгких;
- лангергансоклеточный гистиоцитоз лёгких;
- болезнь фон Гиппеля — Линдау.
Осложнения
Основным осложнением у пациентов с СБХД является развитие спонтанного пневмоторакса. Риск пневмоторакса у пациентов с БХД в 50 раз выше по сравнению с общей популяцией[5].
Лечение
На 2025 год не существует специфического лечения кистозного поражения лёгких при СБХД. Лечение лёгочных проявлений сосредоточено на профилактике и лечении пневмотораксов. Учитывая высокую частоту рецидивов (более 60 % при консервативном лечении), процедура плевродеза проводится уже после первого эпизода спонтанного пневмоторакса — эта процедура позволяет снизить риск повторного пневмоторакса до 30 %. Наиболее эффективной методикой признано тотальное покрытие висцеральной плевры целлюлозной сеткой, которое демонстрирует нулевой процент рецидивов[5].
При возникновении опухолей почки выполняется их хирургическое лечение[5].
Кожные проявления при СБХД не требуют обязательного лечения, поскольку не несут риска злокачественного перерождения. Однако при наличии эстетических жалоб пациентам может быть проведено хирургическое иссечение образований[5].
Прогноз
Прогноз для пациентов с СБХД в первую очередь зависит от раннего выявления и лечения опухолей почки. Рецидивирующие пневмотораксы могут значительно ухудшать качество жизни, а множественные фиброфолликуломы часто воспринимаются пациентами как серьёзный косметический дефект, однако не имеют влияния на прогноз[8].
Диспансерное наблюдение
В связи с риском развития злокачественных новообразований в течение жизни, а также высоким риском развития спонтанного пневмоторакса диспансерное наблюдение пациентов с СБХД требует междисциплинарного подхода с участием пульмонолога, торакального хирурга, дерматолога и уролога[7].
Профилактика
Профилактика направлена на снижение риска прогрессирования лёгочных проявлений и возможного развития инфекционных осложнений. Рекомендован отказ от курения, вакцинация пневмококковой вакциной и ежегодная вакцинация против гриппа[5].
Примечания
- ↑ Monarch Disease Ontology release 2018-06-29sonu — 2018-06-29 — 2018.
- ↑ 1 2 Авдеев С. Н., Трушенко Н. В., Авдеев И. С., Николенко А. М., Неклюдова Г. В. Болезнь Берта — Хогга — Дюбе: клинические наблюдения (рус.) // Пульмонология : журнальная статья. — 2023. — Т. 33, № 2. — С. 266—272. — ISSN 0869-0189. — doi:10.18093/0869-0189-2023-33-2-266-272.
- ↑ Schmidt L. S. Birt — Hogg — Dubé syndrome: from gene discovery to molecularly targeted therapies (англ.) // Familial Cancer : журнальная статья. — 2013. — Сентябрь (т. 12, № 3). — С. 357—364. — ISSN 1389-9600. — doi:10.1007/s10689-012-9574-y. — PMID 23108783.
- ↑ I Kluijt, D De Jong, HJ Teertstra, PH Axwijk, JJP Gille, K Bell, A Van Rens, AWG Van Der Velden, L Middelton, S Horenblas. Early onset of renal cancer in a family with Birt–Hogg–Dubé syndrome // Clinical Genetics. — 2009-06. — Т. 75, вып. 6. — С. 537–543. — ISSN 1399-0004 0009-9163, 1399-0004. — doi:10.1111/j.1399-0004.2009.01159.x.
- ↑ 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 Cécile Daccord, Jean-Marc Good, Marie-Anne Morren, Olivier Bonny, Daniel Hohl, Romain Lazor. Birt — Hogg — Dubé syndrome // European Respiratory Review. — 2020-09-17. — Т. 29, вып. 157. — С. 200042. — ISSN 1600-0617 0905-9180, 1600-0617. — doi:10.1183/16000617.0042-2020.
- ↑ Muller M. E., Daccord C., Taffé P., Lazor R. Prevalence of Birt — Hogg — Dubé Syndrome Determined Through Epidemiological Data on Spontaneous Pneumothorax and Bayes Theorem (англ.) // Frontiers in Medicine : журнальная статья. — 2021. — 27 апреля (т. 8). — С. 631168. — ISSN 2296-858X. — doi:10.3389/fmed.2021.631168. — PMID 33987191.
- ↑ 1 2 3 4 Jonathan S. Crane, Veronica Rutt, Amanda M. Oakley. Birt — Hogg — Dube Syndrome (англ.). — 2023-07-04.
- ↑ Elke Sattler. Birt — Hogg — Dubé syndrome (англ.). Orphanet (ноябрь 2023).
Литература
- Баранова Александра Николаевна, Абраменко Анастасия Владимировна, Георгинова Ольга Анатольевна, Французевич Лайне Яновна, Краснова Татьяна Николаевна. Экстрапульмональные поражения у пациентов с орфанными заболеваниями лёгких // Практическая пульмонология. — 2023. — № 2. — doi:10.24412/2409-6636-2023-12878.
- Бродская О. Н., Поливанов Г. Э. Буллёзная эмфизема и буллёзная болезнь лёгких // Практическая пульмонология. — 2019. — № 1.