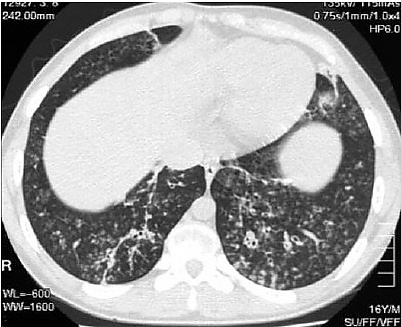
Диффузный панбронхиолит
Диффу́зный панбронхиоли́т (ДП) — идиопатическое воспалительное заболевание, которое преимущественно поражает респираторные бронхиолы, вызывая прогрессирующее гнойное воспаление и тяжёлое обструктивное поражение дыхательных путей. Без лечения заболевание прогрессирует до бронхоэктатической болезни и дыхательной недостаточности с летальный исходом[2].
Общие сведения
История
В начале 1960-х годов врачи в Японии начали наблюдать и описывать новое хроническое заболевание лёгких. В 1969 году для его обозначения было введено название «диффузный панбронхиолит», чтобы отличать его от хронического бронхита, эмфиземы лёгких, альвеолита и других обструктивных заболеваний лёгких, сопровождающихся воспалением. В период с 1978 по 1980 год результаты общенационального исследования, проведённого по инициативе Министерства здравоохранения и социального обеспечения Японии, выявили более 1000 вероятных случаев диффузного панбронхиолита (ДП), из которых 82 были подтверждены гистологически. К 1980-м годам это заболевание получило международное признание как отдельная патология лёгких[2][3].
Классификация
ДП относится к категории первичных бронхиолитов, то есть воспалительный процесс изначально возникает в бронхиолах или ограничивается ими. В отличие от них, вторичные бронхиолиты являются вторичным проявлением иного заболевания[4].
Этиология
Развитие ДП у восточноазиатского населения свидетельствует о том, что предрасположенность к заболеванию обусловлена генетическими факторами, характерными именно для азиатов. Антиген HLA-B54, известный как этнический маркер восточноазиатских популяций, демонстрирует сильную ассоциацию с ДП в Японии. В то же время у корейских пациентов с ДП выявлена связь с HLA-A11. Исследование генетических маркеров, проведённое группой Кудо и Кейчо, позволило предположить, что основной ген предрасположенности к ДП расположен на 6-й хромосоме. Впоследствии в этом регионе были обнаружены два новых гена — PBMUCL1 и PBMUCL2, которые могут играть роль в патогенезе заболевания[5].
Патогенез
Ключевым аспектом патогенеза ДП является скопление лимфоцитов и макрофагов вокруг респираторных бронхиол. Исследования показывают, что у пациентов с ДП часто наблюдается гиперплазия лимфоидной ткани, ассоциированной с бронхами. В фолликулярных зонах преобладают B-лимфоциты, экспрессирующие поверхностный иммуноглобулин M, тогда как в парафолликулярных областях локализуются T-лимфоциты, преимущественно CD4+. Ещё одной важной особенностью ДП является скопление нейтрофилов в проксимальных отделах дыхательных путей. В бронхиальной жидкости пациентов значительно повышено количество нейтрофилов и их эластазная активность. Хемотаксическая активность в бронхиальном секрете также усилена за счёт высоких уровней интерлейкина-8, лейкотриена B4 и других хемоаттрактантов. Избыточная выработка хемоаттрактантов и активация молекул адгезии приводят к массивной миграции нейтрофилов в дыхательные пути, что вызывает воспалительный процесс[5].
При патологоанатомическом исследовании ткани лёгких при ДП на срезах обнаруживаются мелкие желтоватые узелки в паренхиме. Эти узелки представляют собой утолщённые стенки респираторных бронхиол, инфильтрированные лимфоцитами, плазматическими клетками и гистиоцитами. Воспалительный процесс распространяется на перибронхиолярные ткани, тогда как альвеолярные стенки остаются интактными, хотя в стенках бронхиол, прилегающих к альвеолярным ходам, отмечается скопление пенистых гистиоцитов. На поздних стадиях ДП может быть трудно отличить от бронхоэктатической болезни из-за вторичного расширения проксимальных бронхиол[5].
Эпидемиология
ДП на 2025 год признан во всем мире как отдельное клиническое заболевание, которое обычно развивается в возрасте от 20 до 50 лет (средний возраст начала — 40 лет, возможный диапазон — от 10 до 70 лет). Согласно популяционному исследованию, проведённому в Японии в 1982 году, распространённость ДП составляла 11 случаев на 100 000 человек. В Японии соотношение мужчин и женщин среди пациентов составляет примерно 1,4—2:1, что не указывает на выраженное преобладание какого-либо пола[2].
После первоначального описания ДПБ в Японии случаи заболевания были зарегистрированы и в других странах Азии, включая Тайвань, Корею, Китай, Малайзию, Таиланд и Сингапур. В последние годы ДП также выявляли у представителей европейской, латиноамериканской и афроамериканской популяций в Италии, Франции, Великобритании, Германии, Норвегии и США. Описан один случай заболевания у ребёнка[2].
Диагностика
Более чем у 80 % пациентов с ДП в анамнезе или на момент диагностики выявляется хронический синусит. В возрасте от 20 до 50 лет у больных обычно наблюдаются хронический кашель и обильное выделение гнойной мокроты, к которым позже присоединяется одышка при физической нагрузке. При аускультации лёгких выслушиваются грубые хрипы[5].
При стандартной рентгенографии органов грудной клетки выявляются двусторонние диффузные мелкоочаговые затемнения на фоне признаков гипервоздушности лёгочной ткани. В запущенных случаях визуализируются кольцевидные или параллельные линейные тени, свидетельствующие о развитии бронхоэктазов[2].
Наибольшую диагностическую ценность имеет компьютерная томография, позволяющая дифференцировать ДП от других бронхиолитов. Характерные находки включают:
- центрилобулярно расположенные узелковые затемнения, часто с линейными ветвящимися участками пониженной плотности («симптом дерева в почках»);
- признаки воздушной ловушки на экспираторных снимках;
- расширение просвета бронхов и утолщение их стенок;
- отсутствие мозаичной олигемии[2].
Выделяют 4 стадии изменений по данным компьютерной томографии:
- 1-я стадия — мелкие узелки (<5 мм);
- 2-я стадия — центрилобулярные узелки, соединённые с дистальными ветвящимися структурами (Y-образная конфигурация, «дерево в почках»);
- 3-я стадия — кистозные расширения узелков (ранние бронхоэктазы);
- 4-я стадия — крупные кисты, соединённые с расширенными проксимальными бронхами[2].
Исследование функции внешнего дыхания посредством спирометрии выявляет выраженные обструктивные нарушения, слабо поддающиеся действию бронходилататоров. Для диагностики используются следующие критерии:
- снижение соотношения ОФВ1/ФЖЕЛ менее 70 %;
- жизненная ёмкость лёгких менее 80 % от должных значений;
- увеличение остаточного объёма свыше 150 % от нормы[2].
- Иммунотурбидиметрия: характерно повышение концентрации сывороточного иммуноглобулина A.
- Иммуноферментный анализ крови: характерно обнаружение ревматоидного фактора.
- Общий анализ крови: умеренный нейтрофилёз, увеличенная скорость оседания эритроцитов.
- Микробиологический анализ мокроты: при первичном обследовании у 44 % больных высевается Haemophilus influenzae, у 22 % — Pseudomonas aeruginosa. Также в мокроте могут обнаруживаться Streptococcus pneumoniae и Moraxella catarrhalis. При этом частота выявления Pseudomonas aeruginosa прогрессивно увеличивается по мере прогрессирования заболевания, достигая в среднем 60 % через 4 года от начала симптомов[5].
Диагностические критерии диффузного панбронхиолита (согласно рекомендациям Министерства здравоохранения и социального обеспечения Японии)
Обязательные критерии (требуется наличие всех трёх):
- Стойкий кашель с выделением мокроты и одышка при физической нагрузке.
- Наличие хронического синусита в анамнезе или на момент обследования.
- Двусторонние диффузные мелкоочаговые затемнения на рентгенограмме грудной клетки или центрилобулярные микронодулярные изменения при компьютерной томографии.
Дополнительные критерии (требуется минимум два из следующих):
- Наличие грубых хрипов при аускультации.
- Снижение показателя ОФВ1/ФЖЕЛ менее 70 % и гипоксемия (парциальной давление кислорода в артериальной крови менее 80 мм рт. ст.).
- Повышенный титр холодовых агглютининов (≥64).
Для постановки достоверного диагноза необходимо соответствие всем трём основным критериям плюс минимум двум дополнительным[5].
Дифференциальная диагностика
Дифференциальная диагностика проводится со следующими состояниями[2]:
- гипогаммаглобулинемия;
- муковисцидоз;
- первичная цилиарная дискинезия;
- бронхолёгочный аспергиллёз;
- гранулёматоз Вегенера;
- туберкулёз;
- саркоидоз;
- аспирационная пневмония;
- облитерирующий бронхиолит;
- коллагеноз-ассоциированный бронхиолит;
- бронхиолит при язвенном колите.
Осложнения
Осложнения диффузного панбронхиолита (ДПБ) включают[6]:
- бронхлэктатическая болезнь;
- дыхательная недостаточность;
- лёгочная гипертензия;
- хроническое лёгочное сердце с развитием сердечной недостаточности;
- рецидивирующие пневмонии.
Лечение
Основным звеном консервативной терапии являются макролидные антибиотики. Макролидные антибиотики известны своей эффективностью в лечении острых инфекций дыхательных путей, но не менее важны их противовоспалительные и иммунорегуляторные свойства. Макролиды подавляют выработку провоспалительных цитокинов. Макролиды также блокируют образование молекул адгезии, необходимых для миграции нейтрофилов. Доказано, что лечение эритромицином снижает абсолютное количество и процентное содержание нейтрофилов в бронхоальвеолярной жидкости у пациентов с ДП, а также уменьшает количество нейтрофилов после воздействия грамотрицательных бактерий. В совокупности эти противовоспалительные эффекты приводят к улучшению функции лёгких и снижению частоты инфекций дыхательных путей[2].
Примечания
Литература
- Голуб А. В., Козлов Р. С. Макролиды для терапии внебольничных инфекций нижних отделов дыхательных путей // Медицинский совет. — 2013. — № 5.
- Котляров Пётр Михайлович, Георгиади С. Г. София Георгиевна. Бронхиолиты: возможности рентгенологической диагностики // Практическая пульмонология. — 2003. — № 1.