Глутаровая ацидемия 2-го типа
Глута́ровая ацидеми́я 2-го ти́па (ГА 2-го ти́па; мно́жественная недоста́точность ацил-КоА-дегидрогена́зы) — редкое наследственное заболевание, связанное с нарушением метаболизма аминокислот и жирных кислот. Клиническая картина варьируется от тяжёлых метаболических расстройств у новорождённых до более лёгких проявлений (мышечная слабость и дыхательная недостаточность) у детей и взрослых. Заболевание возникает из-за дефицита ключевых митохондриальных ферментов — электрон-переносящего флавопротеина и ETF-дегидрогеназы. Недостаточность этих ферментов приводит к накоплению токсичных метаболитов в тканях и биологических жидкостях, что вызывает повреждение внутренних органов. В основе заболевания лежат мутации в генах ETFA, ETFB и ETFDH. Лечение включает патогенетическую терапию, направленную на коррекцию метаболических нарушений, а также симптоматическую терапию[1].
Что важно знать
История
ГА 2-го типа была впервые описана в 1976 году врачом Х. Пширембелем и его коллегами. Они описали клиническое наблюдение младенца с гипогликемией и метаболическим ацидозом, у которого отмечался необычный запах кожи. Лабораторные анализы выявили повышение концентрации глутаровой и молочной кислот в моче пациента. Исследователи предположили, что данное заболевание связано с нарушением метаболизма нескольких ацил-КоА соединений. Чтобы дифференцировать его от глутаровой ацидемии 1-го типа, описанной годом ранее, было введено название «глутаровая ацидемия 2-го типа». Позднее, в 1991—1994 годах, учёные установили генетическую природу болезни, обнаружив её связь с мутациями в генах ETFA, ETFDH и ETFB, кодирующих ключевые ферменты митохондриального бета-окисления[1].
Классификация
Классификация ГА 2-го типа[1]
- По клиническим формам:
- неонатальная форма с врождёнными аномалиями (тяжёлое течение, сочетается с пороками развития);
- неонатальная форма без врождённых аномалий (характерны метаболические кризы в раннем возрасте);
- поздняя (мягкая) форма (проявляется в детском или взрослом возрасте мышечной слабостью, гипогликемией).
- По ответу на терапию рибофлавином:
- рибофлавин-чувствительная форма;
- рибофлавин-резистентная форма.
Этиология
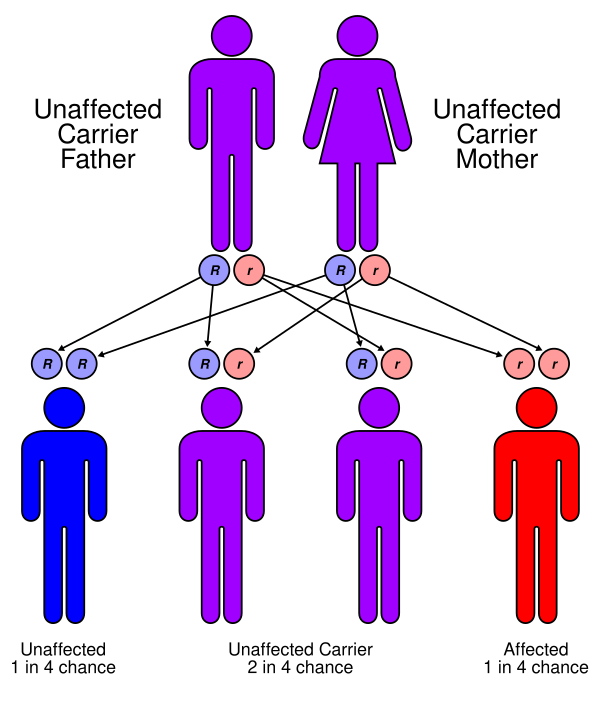
ГА 2-го типа представляет собой наследственное заболевание с аутосомно-рецессивным типом наследования, обусловленное мутациями в генах ETFA, ETFB и ETFDH. Эти гены кодируют ключевые ферменты митохондриального энергетического обмена: ETFA и ETFB отвечают за синтез α- и β-субъединиц электронпереносящего флавопротеина, а ген ETFDH кодирует ETF-дегидрогеназу. Данные ферменты играют критическую роль в процессах β-окисления жирных кислот и катаболизма аминокислот, обеспечивая перенос электронов в дыхательной цепи митохондрий[2].
Патогенез
ГА 2-го типа представляет собой наследственное метаболическое заболевание, в основе которого лежит дефект системы переноса электронов в митохондриях. Ключевыми участниками этого процесса являются электрон-переносящий флавопротеин и ETF-дегидрогеназа. Эти ферменты выполняют критически важную функцию в энергетическом обмене — обеспечивают окисление жирных кислот и катаболизм аминокислот, что особенно важно в периоды, когда организм не может получить достаточное количество энергии из глюкозы. Нарушение работы любого из компонентов дыхательной цепи переноса электронов приводит к серьёзным последствиям: во-первых, блокируется нормальный процесс β-окисления жирных кислот, во-вторых, нарушается метаболизм некоторых аминокислот[1][2].
В результате этих нарушений в организме накапливаются токсичные промежуточные продукты обмена веществ (глутаровая, изовалериановая и различные дикарбоновые кислоты). Эти соединения оказывают повреждающее действие на клетки и ткани, особенно чувствительны к их воздействию нервная система, поперечно-полосатая мышечная ткань и миокард. Параллельно развивается выраженный энергетический дефицит, так как нарушается основной путь получения энергии в условиях голодания или повышенной нагрузки[1][2].
Эпидемиология
Распространённость ГА 2-го типа в мире составляет один случай на 200—300 тысяч живых новорождённых. Эпидемиологических данных по России нет[2].
Диагностика
Неонатальная форма ГА 2-го типа с врождёнными аномалиями представляет собой тяжёлое мультисистемное заболевание, сопровождающееся характерными дисморфическими признаками. У новорождённых отмечаются специфические черты лица: высокий лоб, низко посаженные уши, гипертелоризм, недоразвитие средней зоны лица. Заболевание сочетается с множественными врождёнными аномалиями развития: пороки центральной нервной системы (нарушения формирования мозговых извилин, аномальная миграция нейронов, дегенеративные изменения с глиозом полосатого тела), аномалии желчевыводящих путей, пороки желудочно-кишечного тракта, почечные дисплазии и кисты, врождённые пороки сердца и краниофациальные дисплазии. Также встречаются такие признаки, как стопы-качалки, дефекты мышц передней брюшной стенки и аномалии наружных половых органов. В наиболее тяжёлых случаях возможна внутриутробная гибель плода. У выживших новорождённых наблюдается выраженная мышечная гипотония, гепатомегалия и повышенная склонность к инфекционным заболеваниям[3].
Неонатальная форма ГА 2-го типа без сопутствующих врождённых аномалий проявляется в течение первых двух-трёх суток после рождения. Для этой формы заболевания характерны те же клинические проявления, что и при варианте с пороками развития, однако у таких пациентов отсутствуют какие-либо пороки развития внутренних органов и специфические лицевые дисморфии[2].
Поздняя форма ГА 2-го типа может проявиться в любом возрасте — от раннего детства до зрелых лет, демонстрируя при этом волнообразное течение с чередованием острых метаболических кризов и периодов относительной стабилизации состояния. Во время обострений у пациентов развивается характерный симптомокомплекс, включающий неукротимую рвоту, опасные гипогликемические состояния, выраженный метаболический ацидоз и признаки токсического поражения печени. В межприступные периоды доминируют симптомы хронического поражения мышечной системы: прогрессирующая мышечная слабость, быстрая утомляемость, болезненные мышечные спазмы и выраженное снижение толерантности к физическим нагрузкам. Особенностью данной формы является постепенное нарастание неврологического дефицита и мышечных нарушений по мере прогрессирования заболевания, при этом тяжесть симптоматики может варьировать от умеренных проявлений до глубокой инвалидизации[2].
При проведении магнитно-резонансной томографии и компьютерной томографии головного мозга выявляются атрофия мозгового вещества, поражение белого вещества, а в отдельных случаях — образование заполненных жидкостью полостей в перивентрикулярной зоне и области скорлупы. Эти находки объясняются уменьшением количества извилин, нарушениями миграции нейронов, потерей нервных клеток, а также очаговыми диспластическими изменениями и формированием множественных кист[3].
Позитронно-эмиссионная томография с фтордезоксиглюкозой выявляет умеренное снижение метаболической активности — в коре головного мозга пациента и в хвостатых ядрах. У пациентов с неонатальной формой без врождённых аномалий отклонения не выявляются[3].
Биохимический анализ крови: характерны метаболический ацидоз, гипогликемия, гипераммониемия, повышение активности печёночных ферментов[1].
Биохимический анализ мочи: характерно выявление кетоновых тел[1].
Характерно повышение концентрации глутаровой, этилмалоновой кислот в моче и ацилкарнитина в крови, выявляемое с помощью тандемной масс-спектрометрии или хромато-масс-спектрометрии[1].
Молекулярно-генетический анализ: характерно выявление мутаций в генах ETFA, ETFB и ETFDH методом секвенирования[1].
Дифференциальная диагностика
Дифференциальная диагностика ГА 2-го типа проводится со следующими состояниями[4]:
- глутаровая ацидурия 1-го типа;
- глутаровая ацидурия 3-го типа;
- дефицит среднецепочечной ацил-КоА-дегидрогеназы.
Лечение
Основу терапии ГА 2-го типа составляют препараты, направленные на коррекцию метаболических нарушений. Рибофлавин применяется для улучшения функции ферментов дыхательной цепи. Коэнзим Q10 включают в схему лечения для поддержания энергетического обмена в митохондриях, а L-карнитин используют для связывания и выведения токсичных органических кислот. При развитии острых состояний проводят купирование гипогликемии с помощью перорального или внутривенного введения растворов глюкозы. Для борьбы с гипераммониемией назначают бензоат натрия. В тяжёлых случаях показана госпитализация и проведение гемодиализа для экстренного выведения накопившихся токсичных метаболитов[1][2].
Перспективными направлениями терапии считаются применение безафибрата, способствующего усилению экспрессии ферментов β-окисления жирных кислот, и использование кетоновых тел. Кетоновые тела выполняют двойную функцию — служат альтернативным источником энергии и поддерживают процессы миелинизации в нервной ткани[1].
Прогноз
Прогноз заболевания зависит от тяжести симптомов. Как правило, при неонатальных формах он неблагоприятный. Поздняя форма при соблюдении врачебных рекомендаций и диетотерапии протекает более благоприятно[2].
Диспансерное наблюдение
Пациентов с ГА 2-го типа наблюдают невролог, гастроэнтеролог, диетолог, офтальмолог, эндокринолог, кардиолог. Периодичность наблюдения определяется индивидуально[1].
Профилактика
Семьям с больными ГА 2-го типа детьми при планировании новой беременности рекомендуется медико-генетическое консультирование врача-генетика, а также пренатальная диагностика[2].
Примечание
Литература
- Баранова П. В., Байдакова Г. В., Лендоева Д. В. и др. Клинико-генетическая характеристика пациентов с глутаровой ацидурией типа 2, выявленных по программе расширенного неонатального скрининга в Российской Федерации. — 2024. — Т. 23, № 9. — С. 18—31. — doi:10.25557/2073-7998.2024.09.18-31.