Изолейцин
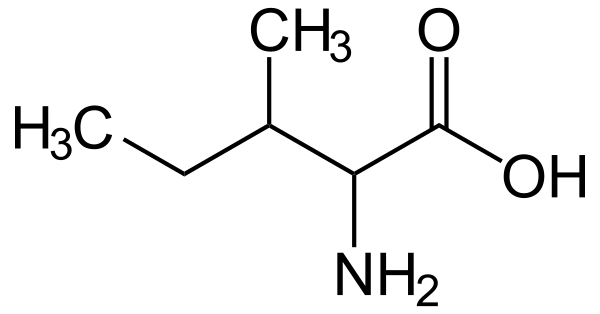
Изолейцин (сокращённо Ile или I; 2-амино-3-метилпентановая кислота)[2] — алифатическая α-аминокислота, имеющая химическую формулу HO2CCH(NH2)CH(CH3)CH2CH3 и входящая в состав всех природных белков. Является незаменимой аминокислотой, что означает, что изолейцин не может синтезироваться в организме человека и должен поступать в него с пищей. Участвует в энергетическом обмене. При недостаточности ферментов, катализирующих декарбоксилирование изолейцина, возникает кетоацидоз.
Кодоны изолейцина: AUU, AUC и AUA.
Вместе с валином и лейцином входит в число аминокислот с разветвлёнными боковыми цепями.
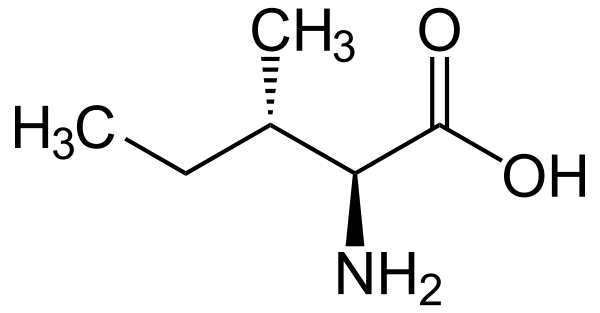
Обладая углеводородной боковой цепью, изолейцин относится к числу гидрофобных аминокислот. Характерной особенностью боковой цепи изолейцина является её хиральность (второй такой аминокислотой является треонин). Для изолейцина возможно четыре стереоизомера, включая два возможных диастереоизомера L-изолейцина. В природе, однако, изолейцин присутствует лишь в одной энантиомерной форме — (2S,3S)-2-амино-3-метилпентановая кислота.
Аминокислота была открыта немецким химиком и биохимиком Феликсом Эрлихом в 1906 году.
Общие сведения
| Изолейцин | |
|---|---|
| Общие | |
| Сокращения |
Иле, Ile, I AUU,AUC,AUA |
| Хим. формула | HO2CCH(NH2)CH(CH3)CH2CH3 |
| Рац. формула | C6H13NO2 |
| Физические свойства | |
| Молярная масса | 131,17 г/моль |
| Химические свойства | |
| Константа диссоциации кислоты | 9,758[1] |
| Классификация | |
| Рег. номер CAS | 73-32-5 |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 6306 |
| UNII | 04Y7590D77 |
| CompTox Dashboard EPA | DTXSID1047441 |
| Рег. номер EINECS | 200-798-2 |
| SMILES | |
| InChI | |
| ChEBI | 17191 |
| ChemSpider | 6067 |
| ECHA InfoCard | 100.000.726 |
Биосинтез
Как и другие незаменимые аминокислоты, изолейцин не синтезируется в организмах животных, и должен поступать извне, обычно в составе белков. В растениях и микроорганизмах изолейцин синтезируется посредством нескольких стадий, начиная от пировиноградной кислоты и α-кетобутирата; процесс катализируется рядом ферментов[3], среди которых треониндезаминаза.
Синтез
Изолейцин может быть синтезирован по многостадийной схеме, начиная с 2-бромбутана и диэтилмалоната. О получении изолейцина синтетическим путём впервые было сообщено в 1905[4].
Применение
Изолейцин активирует синтез мышечного белка по механизму mTOR. В свете этого фактора используется в косметологии для регенерации старой кожи.
Повышенная потребность в изолейцине наблюдается у грудных детей. Также потребность увеличивается после потери крови, ожогов, растяжении и прочих процессов, сопровождаемых регенерацией тканей[5].
Изолейцин – основной строительный материал для кетоновых тел и глюкозы. Таким образом, аминокислота регулирует уровень сахара в крови.
Также изолейцин участвует в процессе синтеза гемоглобина.
Вместе с тем изолейцин защищает организм от чрезмерной выработки серотонина.