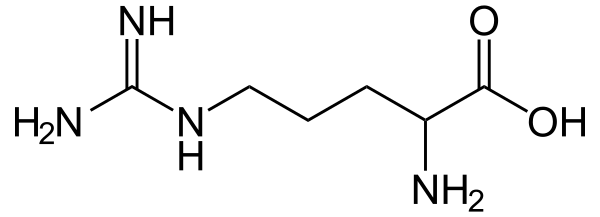
Аргининемия
Аргининеми́я (аргина́зная недоста́точность, дефици́т аргина́зы 1, недоста́точность аргина́зы, гипераргининеми́я) — редкое наследственное заболевание из группы нарушений цикла мочевины, вызванное дефицитом фермента аргиназы. Аргининемия обусловлена мутациями в гене ARG1. Передаётся по аутосомно-рецессивному типу. Заболевание характеризуется накоплением аргинина и аммиака в организме, что приводит к гипераммониемии различной степени выраженности. Основные клинические проявления включают задержку психомоторного развития, спастичность, судороги и когнитивные нарушения. Манифестация заболевания обычно происходит в детском возрасте, в среднем от 1 до 3 лет. Уровень гипераммониемии при аргининемии, как правило, ниже, чем при других нарушениях цикла мочевины, однако в отсутствие лечения возможны прогрессирующие неврологические осложнения. Диагноз устанавливается на основании характерной клинической картины, результатов нейровизуализации, ультразвукового исследования печения, а также биохимического анализа крови и мочи. Лечение носит поддерживающий и симптоматический характер и направлено на снижение уровня аммиака и аргинина. При ранней диагностике и адекватном лечении прогноз благоприятный[1][2][3].
Что важно знать
История
Аргининемия была впервые описана в 1969 году немецким врачом Терхеггеном Х. Г. на примере двух сестёр в возрасте полутора и пяти лет. У пациенток наблюдались эпилептические припадки, выраженная умственная отсталость и спастичность конечностей. Биохимическое исследование выявило повышенную концентрацию аргинина в крови и спинномозговой жидкости, а также сниженную активность фермента аргиназы[1].
В 1986 году был идентифицирован ген ARG1, мутации в котором лежат в основе развития аргининемии[1].
Этиология
Аргининемия обусловлена мутациями в гене ARG1, расположенном на длинном плече 6-й хромосомы (6q23.2), который кодирует фермент аргиназу 1. Этот фермент катализирует последнюю стадию цикла мочевины — гидролиз L-аргинина до орнитина и мочевины[1]. Данное заболевание наследуется по аутосомно-рецессивному типу: для его проявления необходимы две патологические аллели гена ARG1. Оба родителя больного обычно являются носителями одной мутантной копии гена, но не имеют клинических проявлений болезни[4].
Дефицит аргиназы 1 нарушает функционирование цикла мочевины — ключевого метаболического пути, с помощью которого организм обезвреживает избыточный аммиак, образующийся при расщеплении белков. Нарушение приводит к гипераргининемии, а также к гипераммониемии, особенно в катаболических состояниях (например, при инфекции или голодании)[2][5][6].
В организме существует также фермент аргиназа 2, кодируемый геном ARG2 и локализованный преимущественно в митохондриях внепечёночных тканей (почках, поджелудочной железе и др.). Однако активность аргиназы 2 недостаточна для компенсации дефицита аргиназы 1 в печени[3].
Провоцирующие факторы, способствующие более быстрому накоплению аммиаку в крови[6]:
- употребление продуктов с высоким содержанием белка,
- стресс, вызванный болезнью или голоданием.
Патогенез
Аргиназа 1 преимущественно экспрессируется в гепатоцитах, а также в эритроцитах и слюнных железах. Она катализирует пятый и заключительный этап цикла мочевины — гидролиз аргинина до орнитина и мочевины. При её дефиците наблюдается накопление аргинина и его производных, в том числе гуанидиноацетата, обладающего нейротоксическим действием. Это приводит к нейродегенеративным изменениям, включая прогрессирующую задержку развития, спастичность и умственную отсталость[1][2][3].
У людей с дефицитом аргиназы этот фермент повреждён или отсутствует, и аргинин не расщепляется должным образом. В результате мочевина не может образовываться в нормальном режиме, и в крови накапливается избыток азота в виде аммиака[6].
Также можно выявить накопление оротовой кислоты, поскольку снижение уровня орнитина приводит к нарушению активности орнитинтранскарбамилазы, что приводит к накоплению или избытку карбамилфосфата, который впоследствии направляется на путь синтеза пиримидина, что проявляется оротурией[3].
Эпидемиология
Распространённость аргининемии оценивается в пределах от 1 случая на 300000 до 1000000 новорождённых[6]. Точные эпидемиологические данные по Российской Федерации не установлены. Заболевание встречается с одинаковой частотой у мужчин и женщин и передаётся по аутосомно-рецессивному типу наследования[1][2].
Если оба родителя являются носителями мутации, риск рождения ребёнка с заболеванием составляет 25 %[2].
Диагностика
Диагноз устанавливается на основании характерной клинической картины, результатов нейровизуализации, ультразвукового исследования печения, а также биохимического анализа крови и мочи[1].
Первые симптомы заболевания, как правило, проявляются в возрасте от 1 до 3 лет. Аргининемия редко манифестирует в неонатальном периоде, а случаи тяжёлой гипераммониемии у новорождённых практически не наблюдаются. Заболевание характеризуется триадой симптомов, типичных для нарушений цикла мочевины: гипераммониемией, энцефалопатией и респираторным алкалозом. Клинические проявления развиваются постепенно и включают[1][2][4]:
- спастичность, преимущественно нижних конечностей, нередко с последующим развитием спастической диплегии или тетрапареза;
- задержку моторного и когнитивного развития, умственную отсталость, утрату ранее приобретённых навыков;
- эпилептические припадки, судороги, тремор;
- атаксию, нарушения равновесия и координации;
- головные боли;
- микроцефалию;
- агрессивное поведение, синдром дефицита внимания и гиперактивности, общее расстройство развития;
- нарушения памяти и мелкой моторики, особенно у взрослых пациентов;
- снижение линейного роста;
- контрактуры суставов;
- полную утрату контроля над функциями кишечника и мочевого пузыря.
Также могут наблюдаться[1][7][8]:
- лёгкая или выраженная дисфункция печени, гепатомегалия;
- нарушения минерализации костей;
- обезвоживание;
- гипотония;
- летаргия.
Некоторые пациенты могут оставаться бессимптомными до раннего детства, а у части признаки заболевания могут быть слабо выражены и манифестировать в более позднем возрасте[2][4].
- Биохимический анализ крови — выявляется выраженное повышение концентрации аргинина (в 3—4 раза выше нормы), которое считается патогномоничным признаком заболевания. Также может наблюдаться умеренная гипераммониемия (уровень аммиака в плазме крови чаще менее 200 мкг/дл, но может быть выше). В ряде случаев повышается концентрация печёночных трансаминаз[1][2][3].
- Биохимический анализ мочи — выявляется повышения экскреция аргинина, а также других аминокислот, включая лизин, орнитин, цистин, глицин. Также наблюдается повышенная концентрация оротовой кислоты, что дополнительно указывает на нарушение цикла мочевины[1][3].
- Масс-спектрометрический анализ аминокислот — выявляется значительное повышение концентрации аргинина в плазме[2].
- Молекулярно-генетическое исследование — выявление мутаций в гене ARG1[1].
- Магнитно-резонансная томография головного мозга — может выявляться атрофия коры головного мозга различной степени, микроцефалия, участки ишемии и отёка[3][8].
- Компьютерная томография головного мозга — применяется при недоступности магнитно-резонансной томографии. Позволяет обнаружить признаки церебральной атрофии и подтвердить наличие структурных изменений[1].
- Ультразвуковое исследование печени — позволяет выявить гепатомегалию, структурные изменения печени, признаки фиброза или цирроза[1][3].
Дифференциальная диагностика
Включает:
- первичная гипераммониемия[2],
- органические ацидурии[2],
- дефицит карбоангидразы VA[2],
- митохондриопатии[2],
- печёночная недостаточность[2],
- спастическая параплегия[2],
- дефицит аргининосукцинатлиазы[8],
- дефицит карбамоилфосфатсинтетазы[8],
- цитруллинемия[8],
- синдром гиперорнитинемии-гипераммониемии-гомоцитруллинемии[8],
- метилмалоновая ацидемия[8],
- пропионовая ацидемия[8],
- гиперинсулинизм[8],
- дефицит N-ацетилглутаматсинтетазы[8],
- дефицит орнитинтранскарбамилазы[8].
Лечение
Лечение носит поддерживающий и симптоматический характер. Терапия аргининемии направлена на снижение уровня аргинина и аммиака в крови, предупреждение неврологических осложнений и стабилизацию метаболического состояния пациента. Ведущую роль играют диетотерапия и препараты, способствующие удалению избытка азота. При тяжёлых формах рассматриваются инвазивные методы[1][8].
Основу терапии составляет диета с ограниченным содержанием белка и добавлением незаменимых аминокислот. Применяются азотсвязывающие препараты: бензоат натрия, фенилбутират натрия, глицерил фенилбутират и фенилацетат натрия. Эти средства обеспечивают альтернативные пути удаления азота из организма и снижают риск гипераммониемии[8].
При необходимости назначают карглуминовую кислоту, а также симптоматические средства, включая противосудорожные препараты (исключая вальпроевую кислоту) и противорвотные (ондансетрон, палоносетрон). В периоды катаболического стресса (инфекции, голодание, хирургия) требуется усиленная метаболическая поддержка[1][8].
С 2023 года в Европейском союзе одобрена заместительная ферментная терапия пегзиларгиназой, позволяющая эффективно снижать уровень аргинина. Проводятся исследования по использованию генной терапии, редактирования гена ARG1 и терапии мРНК[1][8][9].
При тяжёлом течении и недостаточном эффекте консервативной терапии может проводиться трансплантация печени. Эта операция позволяет стабилизировать метаболические показатели, устранить гипераммониемию и остановить прогрессирование неврологических нарушений. Однако уже развившиеся неврологические симптомы, как правило, необратимы[1][8].
Дополнительно применяются реабилитационные мероприятия, включая физиотерапию, лечебную физкультуру и ортопедическую коррекцию для снижения выраженности спастичности[1][8].
Прогноз
В большинстве случаев прогноз при аргининемии считается относительно благоприятным, особенно при ранней диагностике и своевременно начатом лечении. Заболевание совместимо с высокой продолжительностью жизни, однако выраженность неврологических нарушений, степень поражения печени и наличие осложнений существенно влияют на качество жизни пациента. У большинства пациентов со временем развиваются стойкие неврологические нарушения, которые не всегда удаётся предотвратить классическими методами терапии. Тем не менее проведение неонатального скрининга и начало лечения с рождения позволяют существенно улучшить прогноз, предотвращая тяжёлые нарушения развития[1][2][8].
У пациентов, которым диагноз был поставлен на поздней стадии, сохраняется риск необратимых повреждений центральной нервной системы. Однако даже в таких случаях лечение может замедлить прогрессирование заболевания[8].
Диспансерное наблюдение
Профилактика
Пренатальная диагностика аргининемии возможна в семьях, где ранее был выявлен случай заболевания, а также при наличии известных факторов риска. Диагностика проводится с использованием анализа ДНК для выявления патогенных вариантов в гене ARG1. Генетическое консультирование рекомендуется при планировании беременности, особенно в случае отягощённого семейного анамнеза[2][8].
С 2023 года аргининемия включена в программу расширенного неонатального скрининга в Российской Федерации. Диагностика проводится с помощью тандемной масс-спектрометрии, что позволяет выявлять заболевание на доклинической стадии[1].
Профилактика осложнений, в частности гипераммониемии, включает соблюдение диеты с ограничением белка. При этом белковая нагрузка должна быть достаточной для нормального роста и развития ребёнка[1].