Бета-окисление
Бе́та-окисле́ние (β-окисление), также цикл Кноопа — Линена, — метаболический процесс деградации жирных кислот[1]. Своё название процесс получил по 2-му углеродному атому (С-3 или β-положение) от карбоксильной группы (-СООН) жирной кислоты, который подвергается окислению и последовательному отделению от молекулы. Продуктами каждого цикла β-окисления являются ФАДH2, НАДH и ацетил-КоА. Реакции β-окисления и последующего окисления ацетил-КоА в цикле Кребса служат одним из основных источников энергии для синтеза АТФ по механизму окислительного фосфорилирования[2][3].
В эукариотических клетках β-окисление происходит исключительно в аэробных условиях в матриксе митохондрий или пероксисомах, у растений этот процесс осуществляется в глиоксисомах.
Процесс β-окисления представляет собой специфический путь деградации жирных кислот. Он является одним из главных источников энергии, служащей для синтеза АТФ[2].
Все реакции многостадийного окисления ускоряются специфическими ферментами. β-Окисление высших жирных кислот является универсальным биохимическим процессом, протекающим во всех живых организмах. У млекопитающих этот процесс происходит во многих тканях, в первую очередь в печени, почках и сердце. Ненасыщенные высшие жирные кислоты (олеиновая, линолевая, линоленовая и др.) предварительно восстанавливаются до предельных кислот.
Помимо β-окисления, которое является основным процессом деградации жирных кислот у животных и человека, существуют ещё α-окисление и ω-окисление. α-Окисление встречается как у растений, так и у животных, однако, весь процесс происходит в пероксисомах[4]. ω-Окисление менее распространено среди животных (позвоночные), встречается главным образом у растений[4]. Процесс ω-окисления происходит в эндоплазматическом ретикулуме (ЭР).
История
β-Окисление было открыто в 1904 году немецким химиком Францем Кноопом (Franz Knoop) в опытах с кормлением собак различными жирными кислотами, в которых один атом водорода на концевом атоме ω-С углерода метильной группы -CH3 был замещён на фенильный радикал -С6H5[1][3].
Францем Кноопом было выдвинуто предположение, что окисление молекулы жирной кислоты в тканях организма происходит в β-положении. В результате от молекулы жирной кислоты последовательно отщепляются двууглеродные фрагменты со стороны карбоксильной группы[3].
Жирные кислоты, входящие в состав естественных жиров животных и растений, имеют чётное число углеродных атомов. Любая такая кислота, от которой отщепляется по паре углеродных атомов, в конце концов проходит через стадию масляной кислоты. После очередного β-окисления масляная кислота становится ацетоуксусной. Последняя затем гидролизуется до двух молекул уксусной кислоты[3]. Однако в то время механизмы окисления жирных кислот, происходящие при β-С атоме были ещё неизвестны[5][6]. В 1948—1949 гг. Кеннеди и Ленинджер установили, что процесс окисления жирных кислот происходит в митохондриях. Ф. Линен с сотрудниками (1954—1958 гг.) описал основные ферментативные процессы окисления жирных кислот[1].
Теория β-окисления жирных кислот, предложенная Ф. Кноопом, в значительной мере послужила основой современных представлений о механизме окисления жирных кислот[1][3].
Метаболические процессы
β-Окисление представляет собой последовательность процессов:
- Активацию жирных кислот, происходящую в цитоплазме клетки с образованием ацил-КоА
- Транспортировку ацил-КоА через двойную мембрану митохондрии посредством карнитина (трансмембранный перенос)
- Внутримитохондриальное β-окисление (происходит в матриксе)[7].
Жирные кислоты, которые образовались в клетке путём гидролиза триацилглицеридов или поступившие в неё из крови должны быть активированы, так как сами по себе они являются метаболическими инертными веществами, и вследствие этого не могут быть подвержены биохимическим реакциям, включая и окисление. Процесс их активирования происходит в цитоплазме при участии АТФ, кофермента A (HS-СoA) и ионов Mg2+. Реакция катализируется ферментом ацил-КоА-синтетазой жирных кислот с длинной цепью (Long-chain-fatty-acid—CоА ligase, КФ 6.2.1.3), процесс является эндергоническим, то есть протекает за счёт использования энергии гидролиза молекулы АТФ:
ацил-КоА-синтетазы находятся как в цитоплазме, так и в матриксе митохондрий. Эти ферменты отличаются по специфичности к жирным кислотам с различной длиной углеводородной цепи. Жирные кислоты с короткой и средней длиной цепи (от 4 до 12 атомов углерода) могут проникать в матрикс митохондрий путём диффузии. Активация этих жирных кислот происходит в матриксе митохондрий[2].
Жирные кислоты с длинной цепью, которые преобладают в организме человека (от 12 до 20 атомов углерода), активируются ацил-КоА-синтетазами, расположенными на внешней стороне внешней мембраны митохондрий.
Выделившийся в ходе реакции пирофосфат гидролизуется ферментом пирофосфатазой (КФ 3.6.1.1):
При этом происходит сдвиг равновесия реакции в сторону образования ацил-КоА[2].
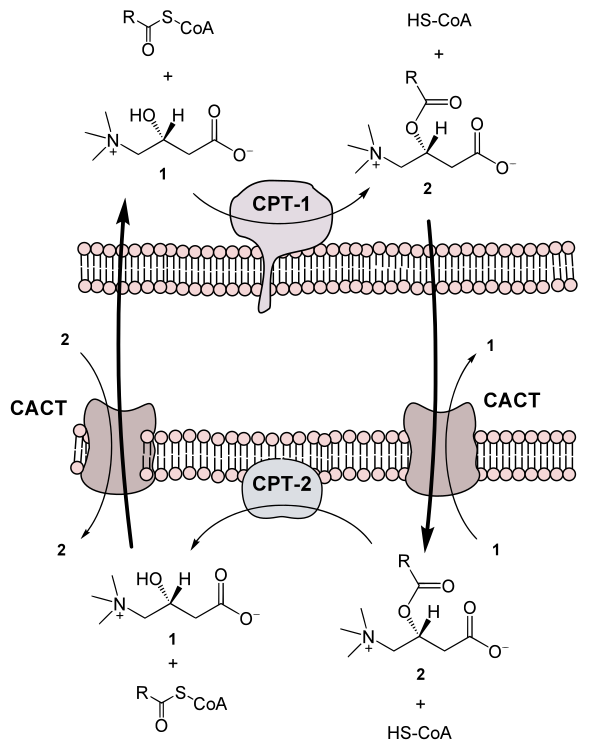
Поскольку процесс активации жирных кислот происходит в цитоплазме, то далее необходим транспорт ацил-КоА через мембрану внутрь митохондрии.
Транспортировка жирных кислот с длинной цепью через плотную митохондриальную мембрану осуществляется посредством карнитина. В наружной мембране митохондрий находится фермент карнитинацилтрансфераза I (карнитин-пальмитоилтрансфераза I, CPT1, КФ 2.3.1.21), катализирующий реакцию с образованием ацилкарнитина (ацильная группа переносится с атома серы КоА на гидроксильную группу карнитина с образованием ацилкарнитина (карнитин-СOR)), который диффундирует через наружную митохондриальную мембрану[2][3]:
R-CO~SКоА + карнитин ↔ карнитин-COR + КоА-SH
Образовавшийся ацилкарнитин проходит через межмембранное пространство к наружной стороне внутренней мембраны и транспортируется с помощью фермента карнитин-ацилкарнитин-транслоказы (CACT)[2].
После прохождения ацилкарнитина (карнитин-СOR) через мембрану митохондрии происходит обратная реакция — расщепление ацилкарнитина при участии КоА-SH и фермента митохондриальной карнитинацил-КоА-трансферазы или карнитинацилтрансферазы II (карнитин-пальмитоилтрансфераза II, CPT2, КФ 2.3.1.21):
КоА-SH + карнитин-COR ↔ R-CO~SКоА + карнитин
Таким образом, ацил-КоА становится доступным для ферментов β-окисления. Свободный карнитин возвращается на цитоплазматическую сторону внутренней мембраны митохондрии той же транслоказой[2][3][8].
После этого ацил-КоА включается в реакции β-окисления.
Процесс трансмембранного переноса жирных кислот может ингибироваться малонил-КоА[9].
В матриксе митохондрии происходит окисление жирных кислот в цикле Кнооппа — Линена. В нём участвуют четыре фермента, которые последовательно действуют на ацил-КоА. Конечным метаболитом данного цикла является ацетил-КоА. Сам процесс состоит из четырёх реакций.
| Наименование реакции | Схема реакции | Фермент | образовавшийся продукт |
|---|---|---|---|
| Дегидрирование активированной жирной кислоты (ацил-КоА). β-Окисление начинается с дегидрирования ацил-КоА ФАД-зависимой ацил-КоА дегидрогеназой жирных кислот с длинной цепью (LCAD) с образованием двойной связи между α- и β-атомами углерода (С-2 и С-3) в продукте реакции — еноил-КоА. Восстановленный в этой реакции кофермент ФАДH2 передаёт атомы водорода в ЭТЦ на кофермент Q. В результате синтезируются 2 молекулы ATФ. | ацил-КоА-дегидрогеназа (КФ 1.3.99.3) | Транс-Δ2-еноил-КоА | |
| Реакция гидратации. Ненасыщенный ацил-КоА (еноил-CоА) при участии фермента еноил-CоА-гидратазы присоединяет молекулу воды. В результате образуется β-гидроксиацил-КоА. Реакция обратима и стереоспецифична, образовавшийся продукт имеет L-форму. | Еноил-CоА-гидратаза (КФ 4.2.1.17) | L-β-гидроксиацил-КоА | |
| НАД+ — зависимое окисление или вторая реакция дегидрирования. Образовавшийся L-β-гидроксиацил-КоА затем окисляется. Реакция катализируется НАД+-зависимой дегидрогеназой. | L-β-гидроксиацетилдегидрогеназа (КФ 1.1.1.35) | L-β-кетоацил-КоА | |
| Тиолазная реакция. В этой реакции β-кетоацил-КоА взаимодействует с коферментом А. В результате происходит расщепление β-кетоацил-КоА и образуется укороченный на два углеродных атома ацил-КоА и двууглеродный фрагмент в виде ацетил-КоА. Данная реакция катализируется ацетил-КоА-ацилтрансферазой (или β-кетотиолазой). | β-Кетотиолаза (КФ 2.3.1.9) | Ацил-КоА и ацетил-КоА |
Образовавшийся ацетил-КоА подвергается окислению в цикле Кребса, а ацил-КоА, укоротившийся на два углеродных атома, снова многократно проходит весь путь β-окисления вплоть до образования бутирил-КоА (4-углеродное соединение), который в свою очередь окисляется до 2 молекул ацетил-КоА. ФАДH2 и НАДH·H поступают прямо в дыхательную цепь[1].
Для полной деградации длинноцепочечной жирной кислоты цикл должен многократно повторяться, так, например, для стеарил-CоА (С17Н35СО~SКоА) необходимы восемь циклов[10].
Особенности окисления жирных кислот с нечётным числом углеродных атомов
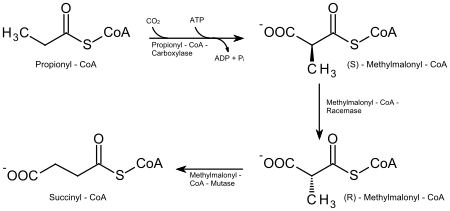
В результате окисления жирных кислот с нечётным числом углеродных атомов образуются не только ацетил-КоА, ФАДH2 и НАДH, но и одна молекула пропионил-КоА (C2H5-CO~SКоА).
Пропионил-КоА превращается в сукцинил-КоА последовательно. Карбоксилирование пропионил-КоА осуществляется под действием пропионил-КоA-карбоксилазы (КФ 6.4.1.3) (коферментом этого фермента служит биотин (витамин B7) — переносчик карбоксигрупп; реакция требует также АТФ). Реакция стереоспецифична. Продуктом реакции является S-изомер метилмалонил-КоА, который катализируется метилмалонил-КоА-рацемазой (КФ 5.1.99.1) в R-изомер. Образовавшийся R-изомер метилмалонил-КоА под действием фермента метилмалонил-КоА-мутазы (КФ 5.4.99.2) (кофермент которой дезоксиаденозилцианокобаламин является производным витамина B12) превращается в сукцинил-КоА, который далее вступает в цикл Кребса[1].
Окисление ненасыщенных жирных кислот
Ненасыщенные жирные кислоты (НЖК) составляют почти половину от общего количества жирных кислот в организме человека. Особенности β-окисления таких кислот определяются положением и числом двойных связей. Двойные связи (-C=C-) природных ненасыщенных жирных кислот (олеиновой, линолевой и т. д.) имеют цис-конфигурацию, а в КоА-эфирах ненасыщенных кислот, являющихся промежуточными продуктами при β-окислении насыщенных жирных кислот, двойные связи имеют транс-конфигурацию. β-Окисление этих кислот идёт обычным путём до тех пор, пока двойная связь не окажется между третьим и четвёртым атомами углерода. Затем фермент еноил-КоА-изомераза (КФ 5.3.3.8) перемещает двойную связь из положения Δ3-4 в положение Δ2-3 и изменяет цис-конформацию двойной связи на транс-, которая требуется для β-окисления. Далее процесс протекает также, как и для насыщенных кислот[1][2][3].
При окислении жирных кислот, имеющих две (-С=C-C-C=C-) и более ненасыщенные связи, требуется ещё один дополнительный фермент β-гидроксиацил-КоА-эпимераза (КФ 5.1.2.3).
Скорость окисления ненасыщенных жирных кислот много выше, чем насыщенных, что обусловлено наличием двойных связей. Например, если взять за эталон скорость окисления насыщенной стеариновой кислоты, то скорость окисления олеиновой в 11, линолевой в 114, линоленовой в 170, а арахидоновой почти в 200 раз выше, чем стеариновой[1].
Бета-окисление у растений
Энергетический баланс процесса
В результате переноса электронов по ЭТЦ от ФАДH2 и НАДH синтезируется по 4 молекулы АТФ (1,5 от ФАДH2, и 2,5 от НАДH[11]). В случае окисления пальмитиновой кислоты проходит 7 циклов β-окисления (16/2-1 = 7), что ведёт к образованию 4×7 = 28 молекул АТФ. В процессе β-окисления пальмитиновой кислоты образуется 8 молекул ацетил-КоА, каждая из которых при полном сгорании в цикле трикарбоновых кислот даёт 10 молекул АТФ, а 8 молекул дадут 10×8 = 80 молекул АТФ.
Таким образом, всего при полном окислении пальмитиновой кислоты образуется 28+80 = 108 молекул АТФ. Однако с учётом одной молекулы АТФ, которая гидролизуется до АМФ, то есть тратятся 2 макроэргические связи или две АТФ, в самом начале на процесс активирования (образования пальмитоил-CоА), общий энергетический выход при полном окислении одной молекулы пальмитиновой кислоты в условиях животного организма составит 108-2=106 молекул[3].
Суммарное уравнение окисления пальмитиновой кислоты выглядит следующим образом:
Формула для расчёта общего количества АТФ, которые генерируются в результате процесса β-окисления жирных кислот с чётным числом углеродных атомов:
где n — количество атомов углерода в молекуле жирной кислоты; 10 и 4 — соответственно, количество молекул АТФ, синтезируемых при окислении 1 моль ацетил-КоА в цикле Кребса и в одном цикле бета-окисления жирной кислоты (1,5 АТФ от ФАДН2 и 2,5 АТФ от НАДН); -2 — количество АТФ, затраченные на активацию жирной кислоты.
Формула для расчёта общего количества АТФ, которые генерируются в результате процесса β-окисления жирных кислот с нечётным числом углеродных атомов:
где n — количество атомов углерода в молекуле жирной кислоты; 25 — количество АТФ, которое синтезируется при окислении образовавшейся 1 молекулы сукцинил-КоА в цикле Кребса до оксалоацетата С4 (5 моль) и его последующего полного окисления в ЦТК (2×10 = 20 моль); -3 — количество АТФ, затраченные на активацию жирной кислоты (2 моль), а также на синтез метилмалонил-КоА (1 моль). Рассчитаем количество синтезируемых молекул АТФ при окислении 1 моль нонадекановой кислоты (С19). Воспользуемся формулой: (19-3/2 × 10) + (19/2-1,5 × 4) + 25 - 3 = 134 моль АТФ.
Энергетический расчёт β-окисления для некоторых жирных кислот представлен в виде таблицы.
| Жирная кислота | Кол-во молекул АТФ генерируемых на 1 молекулу жирной кислоты | Кол-во затраченных молекул АТФ | Общий энергетический выход молекул АТФ |
|---|---|---|---|
| Каприловая кислота C7H15COOH | 44 | 2 | 44-2=42 |
| Лауриновая кислота С11Н23COOH | 80 | 2 | 80-2=78 |
| Миристиновая кислота С13Н27СООН | 94 | 2 | 94-2=92 |
| Пентадециловая кислота С14Н29СООН | 101 | 2 | 101-2=99 |
| Пальмитиновая кислота С15Н31СООН | 108 | 2 | 108-2=106 |
| Маргариновая кислота С16Н33СООН | 115 | 2 | 115-2=113 |
| Стеариновая кислота С17Н35СООН | 122 | 2 | 122-2=120 |
| Арахиновая кислота С19Н39СООН | 136 | 2 | 136-2=134 |
Во многих тканях окисление жирных кислот — важный источник энергии. Это ткани с высокой активностью ферментов цикла Кребса и цепи переноса электронов — клетки красных скелетных мышц, сердечная мышца (миокард), почки. Например, эритроциты, в которых отсутствуют митохондрии, не могут окислять жирные кислоты. В то же время жирные кислоты не могут служить источником энергии для мозга и других нервных тканей, так как они не проходят через гематоэнцефалический барьер, вследствие их гидрофобных свойств. Скорость обмена жирных кислот в нервных тканях на порядок ниже чем, например, в скелетных мышцах. Поэтому в таких ситуациях, особенно при длительном голодании, печень перерабатывает около 50 % поступающих в неё жирных кислот в другие источники энергии — кетоновые тела, которые может утилизировать нервная ткань[2].
Внемитохондриальное окисление жирных кислот
Помимо β-окисления жирных кислот, происходящего в митохондриях существует и внемитохондриальное окисление. Жирные кислоты, имеющие бóльшую длину цепи (от С20), не могут быть окислены в митохондриях из-за наличия плотной двойной мембраны, которая воспрепятствует процессу переноса их через межмембранное пространство. Поэтому окисление длиноцепочечных жирных кислот (С20-С22 и более) происходит в пероксисомах[12] . В пероксисомах процесс β-окисления жирных кислот протекает в модифицированном виде. Продуктами окисления в данном случае являются ацетил-КоА, октаноил-КоА и пероксид водорода Н2О2. Ацетил-КоА образуется на стадии, катализируемой ФАД-зависимой дегидрогеназой. Ферменты пероксисом не атакуют жирные кислоты с короткими цепями, и процесс β-окисления останавливается при образовании октаноил-КоА.
Данный процесс не сопряжён с окислительным фосфорилированием и генерацией АТФ и поэтому октаноил-КоА и ацетил-КоА переходят с КоА на карнитин и направляются в митохондрии, где окисляются с образованием АТФ[8].
Активация пероксисомального β-окисления происходит при избыточном содержании в потребляемой пищи жирных кислот начиная с С20, а также при приёме гиполипидемических лекарственных препаратов.
Регуляция
Скорость регуляции процесса β-окисления включает несколько факторов:
- Соотношений АТФ/АМФ и НАДH/НАД+, так же, как и скорость реакций ЭТЦ и общего пути катаболизма;
- состояния голодания или сытости (то есть соотношения инсулин — глюкагон);
- активности регуляторного фермента карнитин-пальмитоилтрансферазы I (CPTI);
- доступности субстрата — жирных кислот;
- потребности клетки в энергии;
- доступности кислорода[2].
Скорость β-окисления зависит также от активности фермента карнитин-пальмитоилтрансферазы I (CPTI). В печени этот фермент ингибируется малонил-КоА, веществом, образующимся при биосинтезе жирных кислот.
В мышцах карнитин-пальмитоилтрансфераза I (CPTI) также ингибируется малонил-КоА. Хотя мышечная ткань не синтезирует жирные кислоты, в ней имеется изофермент ацетил-КоА-карбоксилазы, синтезирующий малонил-КоА для регуляции β-окисления. Данный изофермент фосфорилируется протеинкиназой А, которая активируется в клетках под действием адреналина, и АМФ-зависимой протеинкиназой и таким образом происходит его ингибирование; концентрация малонил-КоА снижается. Вследствие этого, при физической работе, когда в клетке появляется АМФ, под действием адреналина активируется β-окисление, однако, его скорость зависит ещё и от доступности кислорода. Поэтому β-окисление становится источником энергии для мышц только через 10-20 минут после начала физической нагрузки (так называемые аэробные нагрузки), когда приток кислорода к тканям увеличивается[13].
Нарушения процесса
Дефекты карнитиновой транспортной системы проявляются в ферментопатиях и дефицитных состояний карнитина в организме человека.
Дефицитные состояния карнитина
Наиболее распространены дефицитные состояния, связанные с потерей карнитина во время некоторых состояний организма:
- Ацидурия; больные, страдающие органической ацидурией, теряют большое количество карнитина, который выделяется из организма в форме конъюгатов с органическими кислотами;
- при проведении длительного гемодиализа;
- при длительном лечении больных сахарным диабетом препаратами сульфонилмочевины, которые являются ингибиторами фермента карнитин-пальмитоилтрансферазы I (CPTI);
- низкая активность ферментов, катализирующих синтез карнитина;
- врожденные дефекты фермента карнитин-пальмитоилтрансферазы I (CPTI), отвечающего за транспортировку ацилированного карнитина (карнитин-СOR) через мембрану митохондрии[2].
Признаками и симптомами недостатка карнитина являются приступы гипогликемии, возникающие из-за снижения глюконеогенеза в результате нарушения процесса β-окисления жирных кислот, уменьшение образования кетоновых тел, сопровождающееся повышением содержания свободных жирных кислот (СЖК) в плазме крови, мышечная слабость (миастения), а также накопление липидов[8].
При дефекте гена карнитин-пальмитоилтрансферазы I — СРТ1 (гораздо реже гена СРТ2) развивается печёночная форма недостаточности фермента, которая приводит к гипогликемии и понижению содержания кетоновых тел в плазме крови. Дефект гена карнитин-пальмитоилтрансферазы II СРТ2 вызывает у взрослых миопатии (периодические мышечные боли, мышечная слабость, подёргивания, миоглобинурия), у новорождённых — фатальную печёночную форму (гипераммониемия, увеличенная активность сывороточных трансаминаз, гепатомегалия, некетотическая гипогликемия, кома). Для недостаточности карнитин-пальмитоилтрансферазы II также характерна кардиомегалия[8][14].
Генетические нарушения ацил-КоА-дегидрогеназ жирных кислот средней цепи
В митохондриях имеется 3 вида ацил-КоА-дегидрогеназ, окисляющих жирные кислоты с длинной, средней или короткой цепью радикала. Жирные кислоты по мере укорочения радикала в процессе β-окисления могут последовательно окисляться этими ферментами. Генетический дефект дегидрогеназы жирных кислот со средней длиной радикала (КФ 1.3.8.7) — MCADD (сокр. от Мedium-chain acyl-СоА dehydrogenase deficiency) наиболее распространён по сравнению с другими наследственными заболеваниями — 1:15 000. Частота дефектного гена ACADM, кодирующего ацил-КоА-дегидрогеназы жирных кислот со средней длиной цепи, среди европейской популяции — 1:40. Это аутосомно-рецессивное заболевание, возникающее в результате замены нуклеотида Т (тимин) на А (аденин) в 985-й позиции гена[2]. Проявляется в накоплении жирных кислот средней цепи (особенно каприловой) и их производных в крови и вторичным дефицитом карнитина. Характерными симптомами являются приступы рвоты, летаргическое состояние, сильнейшая некетотическая гипогликемия, вызванная обильной утилизацией глюкозы (особенно опасна для новорожденных), может развиться кома и возможен летальный исход. Большую опасность болезнь представляет у детей, так как среди них наблюдается самая большая летальность (до 60 %)[9].
Генетические нарушения ацил-КоА-дегидрогеназ жирных кислот с очень длинной углеродной цепью
Аутосомно-рецессивное тяжёлое генетическое заболевание встречается с частотой 1:3000-1:50000 у новорожденных стран Европы и США. Обусловлено мутацией гена ACADVL, который кодирует ацил-КоА-дегидрогеназу жирных кислот с очень длинной углеродной цепью — VLCAD (сокр. от Very long chain acyl-CоА dehydrogenase, КФ 1.3.8.9). Данный фермент участвует в митохондриальном β-окислении жирных кислот, углеродная цепь которых содержит 14—20 атомов. Болезнь характеризуется накоплением жирных кислот (С14-С20) в организме. Негативные проявления выражаются в поражениях тканей головного мозга (энцефалопатии), сердца (кардиомиопатии), печени (жировая инфильтрация). Симптомы схожи с MCADD. Существуют несколько форм дефицита ацил-КоА-дегидрогеназы жирных кислот с очень длинной углеродной цепью:
- системная;
- печёночная;
- миопатическая.
Системная форма встречается часто у новорожденных или детей раннего возраста и имеет самую высокую летальность (до 30 %). Наиболее тяжёлая и опасная форма заболевания.
Печёночная форма также часто обладает ранней манифестацией (развитием клинических проявлений), однако, имеет менее тяжёлое течении и летальность. Характеризуется приступами гипокетотической гипогликемии.
Миопатическая форма наблюдаются у детей школьного возраста и взрослых. Её основные проявления: непереносимость физической нагрузки (миастения), боли в мышцах (миалгии, рабдомиалгии), рабдомиолиз, изменение цвета мочи вследствие миоглобинурии[15].
Дикарбоновая ацидурия заболевание, связанное с повышенной экскрецией С6-С10-дикарбоновых кислот и возникающей на этом фоне гипогликемии, однако, не связанная с повышением содержания кетоновых тел. Причиной данного заболевания является MCADD. При этом нарушается β-окисление и усиливается ω-окисление длинноцепочечных жирных кислот, которые укорачиваются до среднецепочечных дикарбоновых кислот, выводимых из организма[8].
Синдром Целлвегера (Зеллвегера) или цереброгепаторенальный синдром, редкое наследственное заболевание описано американским педиатром Гансом Целлвегером (англ. H.U. Zellweger), которое проявляется в отсутствии пероксисом во всех тканях организма. Вследствие этого в организме, особенно в мозгу накапливаются полиеновые кислоты (С26—С38), представляющие собой длиноцепочечные жирные кислоты[8]. Примерная заболеваемость нарушениями биогенеза пероксисом спектра синдрома Целлвегера составляет 1:50 000 новорождённых в США и 1:500 000 новорождённых в Японии. Для синдрома характерны: пренатальная задержка роста; мышечная гипотония; затруднение сосания; арефлексия; долихоцефалия; высокий лоб; круглое плоское лицо; одутловатые веки; гипертелоризм; монголоидный разрез глаз; катаракта; пигментная ретинопатия или дисплазия зрительного нерва; колобома радужки; низко расположенные ушные раковины; микрогнатия; расщелина неба; латеральное или медиальное искривление пальцев; поражение печени (гепатомегалия (увеличение объёма печени), дисгинезия внутрипеченочных протоков, цирроз печени); поликистоз почек; нередко — тяжёлые, несовместимые с жизнью аномалии лёгких и пороки сердца; задержка психомоторного развития; судороги; стойкая желтуха. При патоморфологическом исследовании выявляют задержку миелинизации нейронов; накопление липидов в астроцитах; в печени, почках и мозге уменьшено содержание плазмогенов; в клетках печени и других тканях организма снижено количество пероксисом, большинство пероксисомных ферментов неактивны. В крови повышена активность трансаминаз и отмечается стойкая гипербилирубинемия[16]. Нарушения биогенеза пероксисом обусловлены мутациями в одном из 12 генов PEX[17], кодирующих пероксины. Мутации в этих генах ведут к аномалиям биогенеза пероксисом. Все варианты синдрома Целлвегера наследуются по аутосомно-рецессивному типу[18].
Специфическая болезнь, характеризуется сильнейшей интоксикацией, сопровождающаяся рвотой, гиповолемическим шоком, конвульсиями, гипогликемией, в тяжёлой форме может наступить кома и смертельный исход. Вызывается при употреблении:
- незрелых либо сырых плодов аки, или блигии вкусной (Blighia sapida), в состав которых входит производное α-аминопропановой кислоты, токсин — гипоглицин.
- незрелых плодов личи (Litchi chinensis), в которых также содержится гипоглицин, открытие было сделано в 2017 году в результате массовых отравлений с летальным исходом детей в Индии, которые употребляли незрелые плоды личи натощак.
В результате метаболизма гипоглицин превращается в метиленциклопропанацетил-КоА (мцпа-КоА), который инактивирует ацил-КоА-дегидрогеназу, вследствие чего ингибируется процесс β-окисления[8]. Помимо этого мцпа-КоА способен блокировать ферменты глюконеогенеза[19]. В присутствии гипоглицина происходит накопление главным образом бутирил-КоА, который гидролизуется до свободной масляной кислоты (бутирата). Масляная кислота в избытке попадает в кровь, косвенно вызывая гипогликемию[9].
См. также
Примечания
Литература
- Д.Мецлер. Биохимия. — М.: Мир, 1980. — 609 p.
- Нельсон Д., Кокс М. Основы биохимии Ленинджера. — М.: Бином, 2014. — 636 p. — 1700 экз. — ISBN 978-5-94774-366-1.
- David E. Metzler. Biochemistry: The Chemical Reactions of Living Cells. — 2nd edition. — Academic Press, 2003. — Vol. 2. — 1973 p. — ISBN 978-0-1249-2541-0.
![{\displaystyle {\mathsf {R-COOH+ATP+CoA-SH{\xrightarrow[{}]{Mg^{2+}}}R-COS-CoA+AMP+H_{4}P_{2}O_{7}}}.}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/d01bf4cc82acc0ef67831cc75f0f38637b095126)





![{\displaystyle {\left[({\frac {n}{2}}\cdot 10)+(({\frac {n}{2}}-1)\cdot 4)-2\right]}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/5333000fc28daae57d85f0234f55bef666adb885)
![{\displaystyle {\left[({\frac {n-3}{2}}\cdot 10)+(({\frac {n}{2}}-1,5)\cdot 4)+25-3\right]}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/db3e8195ca608fcefc0d5f7837e2e7dc9747fe02)