Биохимия пива
Биохимия пива включает химические изменения при производстве и выдержке пива, в которых участвуют ферменты, вырабатываемые организмами. Особое значение в этих превращениях имеет активность пивных дрожжей и ферментов солода.
В пиве содержится более 800 соединений, которые определяют его вкус и аромат[1]. Основными ингредиентами пива являются вода, этанол и углеводы. Многие вещества, сильно влияющие на органолептические характеристики пива, встречаются лишь в следовых количествах, однако они имеют ключевое значение для его общего качества из-за низких порогов обнаружения[2]. Эти соединения также проявляются в многочисленных взаимодействиях друг с другом. Можно выделить синергетический эффект, когда одно соединение усиливает восприятие другого, и антагонистический эффект, когда одно соединение снижает восприятие другого[3]. Сложность состава пива, многочисленные взаимодействия и важность даже незначительных различий в концентрации различных соединений вызывают значительные трудности в достижении предполагаемого органолептического профиля готового пива.
История
Исторически сложилось так, что пиво — это ферментированный напиток, приготовленный из зерна. В настоящее время термин «пиво» сужается до охмеленного напитка, полученного из сжиженного крахмала, ферментированного специфическими штаммами дрожжей Saccharomyces[4].
Знания о пиве, произведённом много веков назад, получены на основе археологических артефактов и письменных документов[4]. Однако, в отличие от вина, существует несколько химических археологических находок, подтверждающих присутствие пива в неолитической Месопотамии. Присутствие пива в старых ёмкостях можно обнаружить путём обнаружения оксалатов, главным образом оксалатов кальция, которые являются основным компонентом образования пивного осадка, так называемого «пивного камня»[5].
Интерпретация старых документов также затруднена. На сегодняшний день в процессе производства пива выделяют три основных этапа: соложение (проращивание и сушка зерна), затирание (ферментативное разложение природных полимеров) и ферментация (микробиологическая трансформация различных соединений). Производство пива не обязательно основывалось на этой концепции много веков назад, что может привести к недоразумениям. Другая трудность заключается в том, что старые термины, этимологически связанные с пивом (например, древнеанглийское «beor»), не всегда использовались в контексте напитков на зерновой основе; они также могли означать, например, медовуху или перебродившие фруктовые соки[4].
На протяжении тысячелетий в пиво добавляли различные травы, чтобы придать ему аромат и продлить сроки хранения[6]. Травяная смесь для производства пива в северо-западной Европе и Скандинавии называлась грюйтом gruit или грутом grut[7]. Впервые слово грюйт появляется в записях 999 года[7][8]. Император Оттон III употребляет его в двояком смысле — и как ингредиент при производстве пива, и как название права на его производство, поскольку с 811 года вместе с эдиктом Capitulare de villis Карла Великого это право было ограничено (кроме продукции для личного пользования). Скорее всего, грюйт также привнёс в пиво дрожжи и изначально оно могло напоминать хлеб[4]. Грюйт покупали у местных городских властей или епископов. Это была ранняя форма налогообложения пива[4]. Например, в городе Дордрехт пивовары должны были идти в специальное здание со своим солодом, где к нему подмешивался грюйт[7]. Церковь перестала взимать плату за него в XV веке[9].
Состав травяной смеси варьировался в зависимости от региона, но ключевым ингредиентом была восковница[9]. Кроме того, он мог содержать в том числе кориандр, тысячелистник и хмель[4], а также растения, содержащие психоактивные вещества[4][7].
Со временем возникла сильная конкуренция между пивом с добавлением восковницы и пивом с добавлением хмеля[10]. В литературе имеется много противоречивой информации о первом использовании хмеля в пиве[6]. Первое упоминание о добавлении хмеля в пиво относится к 822 году, когда аббат Адельхар из Корбей дал инструкции своему монастырю Consuetudines Corbeienses[4]. В Польше, Прибалтике и России хмель стал господствовать ещё в XIII веке[9]; в северо-западной Европе популярность восковницы постепенно снижалась с XIV века (за исключением Британских островов), пока в XVIII веке не стал преобладать хмель[8][10]. Слухи о том, что он ядовит, способствовали исчезновению восковницы, хотя современные исследования этому противоречат[8].
Когда-то роль дрожжей в производстве пива не осознавалась. До XV—XVI веков сусло после кипячения заражали переносимыми по воздуху дрожжами. Этот метод был очень ненадёжен и сопряжён с высоким риском заражения нежелательными микроорганизмами[11]. Первое упоминание о воздушных дрожжах при производстве пива относится к 1551 году в Мюнхене[8][11], хотя, скорее всего, до 1300 года пивовары использовали часть бродящей пивной пены, чтобы начать брожение другой. Затем пивовары начали выращивать дрожжи отдельно и позже добавлять их в сусло. Однако инфекции и повышенная температура были проблемой, особенно летом[11].
Иногда пивной бочонок с дрожжами сушили и смешивали с мукой, чтобы получилось тесто, которое при добавлении воды могло вызвать брожение. Вместо сушки осадок также можно было добавлять непосредственно в новое сусло, как в случае с готовым пивом или хлебом. Кроме того, из-за неаккуратной очистки посуды с шероховатой поверхностью на ней всегда оставались дрожжевые клетки. Использование чистых культур дрожжей, а значит, и определённый контроль над этим процессом, стал возможным только в конце XIX века[11]. Эмиль Кристиан Хансен был первым, кто стал работать с чистым штаммом дрожжей, который был выделен им в 1883 году и назван Saccharomyces carlsbergensis[12].
До XVI века дрожжи верхового брожения обычно использовались в производстве пива по всей Европе[11][12]. Низовое брожение, вероятно, впервые появилось в баварских монастырях и впервые упоминается в XV веке. Баварцы заметили, что качество производимого летом пива значительно ниже, потому что оно очень подвержено заражению и закислению. В 1533 году князь Максимилиан I Баварский запретил варить пиво с 23 апреля по 29 сентября без специального разрешения[12]. В связи с производством пива при более низких температурах был подобран штамм дрожжей, который лучше справлялся с брожением в таких условиях и имел тенденцию опускаться на дно сосуда[13]. Из-за летнего перерыва нужно было производить больше пива и хранить его до следующей осени, поэтому оно получило название «лагер»[12]. Пиво отличалось стойкостью, а его вкус отличался от других видов пива того времени[4].
В XIX веке появились новые технологии и возможности. Охлаждение сусла, чаны для брожения, резервуары для выдержки и наличие природного льда для охлаждения пива в подземных погребах означали, что запрет на летнее пивоварение был снят в 1850 году. Появление в 1875 году холодильника позволило производить лагер везде и вне зависимости от времени года. Пиво низового брожения становилось всё более и более популярным и начало заменять пиво верхового брожения. В моду вошли новые виды пива, особенно Pilsner, разработанный Йозефом Гроллом в 1842 году[4].
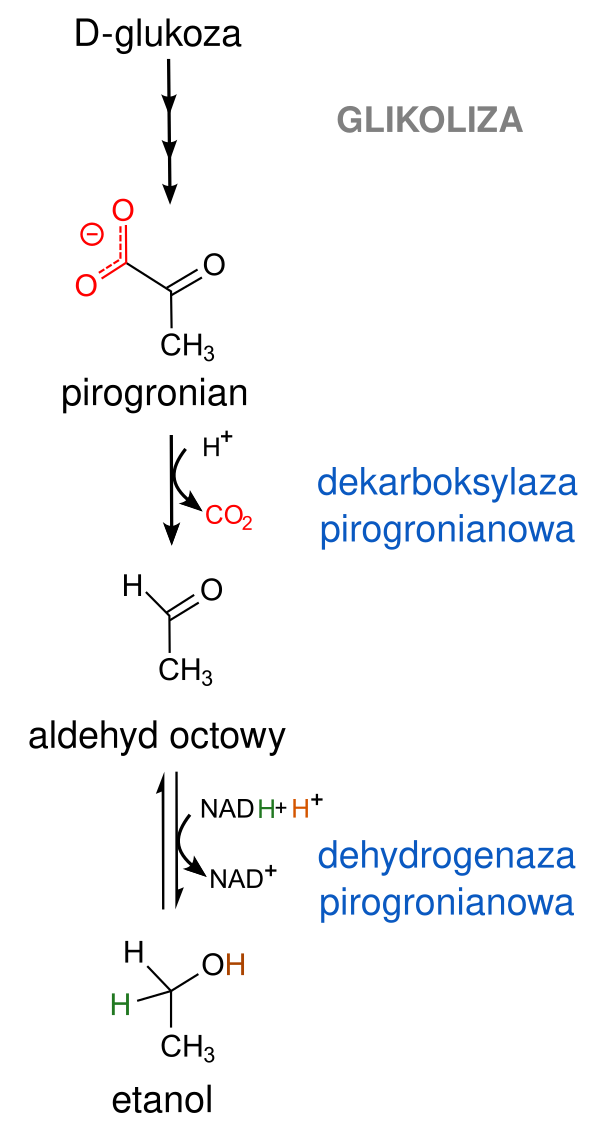
В 1762 году Майкл Комбрун опубликовал «Опыт пивоварения» (англ. Essay on Brewing), в котором подчеркивал необходимость использования термометра во время пивоварения и соложения. Антуан Лавуазье (1789) и Жозеф Гей-Люссак (1815) внесли свой вклад в открытие механизмов процесса брожения, благодаря которым было установлено химическое уравнение окисления глюкозы до CO2 и этанола[4]. В 1833 году Ансельм Пайен открыл и выделил первый фермент — диастазу[14]. В 1835 году швед Йёнс Якоб Берцелиус сформулировал принципы катализа, а Юстус фон Либих применил их к брожению сахаров, получив достаточно подробное его описание. В 1837 году трое учёных Шарль Каньяр де Ла-Тур, Фридрих Кютцинг и Теодор Шванн независимо друг от друга открыли, что дрожжи являются живыми организмами. Карл Баллинг в 1843 году разработал надёжный метод измерения и контроля превращения сахаров в сусле в этанол во время ферментации. В конечном итоге Луи Пастер в 1855—1875 годах однозначно установил роль дрожжей в спиртовом брожении, его физиологические аспекты и различия между аэробным и анаэробным метаболизмами[4].
Хотя существует много источников о пивоварении до середины XIX века, возможность других использовать эти рекомендации была ограничена, поскольку отсутствовала очень важная информация, такая как характеристики оборудования, используемого в производстве, или надёжные измерения. Научные теории, касающиеся этих процессов, могли возникнуть только после введения в пивоварение термометров, измерителей сахара, унифицированных мер и сопоставимого оборудования[4].
Вода
Современные пивоварни потребляют от около 2 л[15] до 5,7 л воды для производства 1 л пива. Вода, служащая непосредственно сырьём для производства пива (в среднем около 2 л на 1 л готового пива)[16] составляет около 90 % его состава[15] и должна не только соответствовать качеству питьевой воды, но и соответствовать дополнительным требованиям. Они связаны с технологическим процессом и желаемым качеством пива[16].
Важнейшими параметрами воды в пивоварении являются жёсткость и остаточная щёлочность. Некарбонатная (постоянная) жёсткость воды ограничивается заданной концентрацией соединений кальция. На неё не влияет приготовление пищи, так как кальций находится в виде солей сильных кислот, таких как хлорид кальция или сульфат кальция[17]. С другой стороны, карбонатная жёсткость (переходная) формируется гидрокарбонатом кальция Ca(HCO3)2 понижается во время приготовления — Ca(HCO3)2 распадается с образованием нерастворимого карбоната кальция[17]. Однако ионы бикарбоната повышают рН[18], что влияет на ферментативные процессы и коллоидные явления — создают неблагоприятное помутнение[15]. Между тем, при производстве пива желательно добиться низкого рН затора и сусла (около 5,5) для лучшей ферментативной активности и более высокого выхода[16]. Более того, более высокий рН может привести к большему выщелачиванию дубильных и горьких веществ из солодовой оболочки, что может придать пиву терпкую, неприятную горечь[15].
Параметр остаточной щёлочности используется для определения приемлемых подщелачивающих свойств воды для пивоварения. Это разница между подщелачивающими свойствами HCO-3 и свойства подкисляющих катионов[15] (главным образом кальция и магния, которые реагируют с вымываемыми из солода фосфатами с выделением протонов[17]). Остаточная щёлочность может быть выражена формулой:
- — остаточная щёлочность в °n (немецкие градусы)
- — общая щёлочность в °n
- — кальциевая жёсткость в °n
- — жёсткость по магнию в °n
и — коэффициенты, позволяющие учесть меньшие окислительные свойства катионов Ca2+ и Mg2+ по отношению к подщелачивающим свойствам HCO-3[15].
Более высокая остаточная щёлочность означает более высокий рН затора и сусла. В заторе более высокое значение рН может быть дополнительно связано с более длительным процессом фильтрации[15].
Смягчение воды для производства пива в основном включает обезуглероживание. Наиболее часто для этой цели применяют: декарбонизацию кальцием (добавление Ca(OH)2 и образование нерастворимого CaCO3), ионообменная технология, мембранная технология (обратный осмос, нанофильтрация), фильтрация (активированный уголь, фильтры для обезжелезивания)[16]. В средние века, когда методы очистки воды были неизвестны, жёсткость воды в том или ином регионе влияла на характер местного пива. Пивовары, варящие пильзнерское пиво, использовали очень мягкую воду, для мюнхенского пива использовалась жёсткая вода, а для дортмундского пива использовалась очень жёсткая вода[19].
Мягкая вода лучше всего подходит для производства светлых лагеров, а жёсткая вода — для тёмных элей, таких как стауты[20]. Более высокая щёлочность подходит такому пиву из-за того, что тёмный прожаренный солод обычно вносит кислотность, которую он уравновешивает, а кроме того, обеспечивает лучшую экстракцию красящих и ароматических соединений[17]. Рекомендуется, чтобы остаточная щёлочность заторной воды не превышала 2 °n для пильзнера, 5 °n для других светлых видов пива и 10 °n для тёмного пива[18].
Вода, содержащая ионы железа, не подходит для производства пива из-за их участия в образовании шлама, помутнения. Они способствуют потемнению сусла и пива, угнетению деятельности дрожжей и придают пиву металлический привкус. Ионы меди являются токсичными и мутагенными для дрожжей, но, поскольку чаны и системы трубопроводов изготовлены из нержавеющей стали, проблемы возникают редко. Марганец может отрицательно влиять на вкус и коллоидную стабильность пива (способствует помутнению). Однако для нормальной жизнедеятельности дрожжей необходимы следовые количества марганца, железа и меди[21].
Сульфат-ион SO2-4 способствуют приданию пиву более сухого горьковатого вкуса, который должен быть уравновешен соответствующим количеством ионов хлора. Кроме того, дрожжи могут поглощать сульфаты и создавать ароматы серы, в том числе H2S и SO2. Ионы хлора Cl- улучшают осветление пива и его коллоидную стабильность, а также принимают участие в придании пиву большего тела. Отношение их концентрации к концентрации сульфатов влияет на ощущение горечи в пиве. Концентрация Cl- не должна превышать 150 мг/л. Нитраты (NO-3) — нежелательные анионы; их количество в питьевой воде не должно превышать 50 мг/л, а в воде, используемой для производства пива, их концентрация должна быть ещё ниже в связи с тем, что их некоторое количество вносится также с хмелем. Они могут быть преобразованы в нитриты (NO-2), которые токсичны для дрожжей[21].
Патогенные для человека микроорганизмы не способны выживать в пиве по многим причинам: пиво содержит этанол (обычно 3,5—5 % по объёму), присутствия горьких веществ хмеля, низкого рН (3,4—4,8), малого количества кислорода (ниже 0,1 промилле), повышенного содержания CO2. Ещё одним барьером может выступать дефицит питательных веществ для микроорганизмов и возможная повторная ферментация в сосуде. Более того, многие этапы производства пива снижают риск загрязнения, например, кипячение сусла, пастеризация, фильтрация, асептический розлив[22]. Тем не менее, в пиве могут развиваться микроорганизмы, ответственные за его порчу, такие как бактерии (например, уксуснокислые бактерии, Lactobacillus sp., Pediococcus sp., Z. mobilis, Klebsiella sp.) и дрожжи (например, Saccharomyces sp., Pichia sp.). Порча пива проявляется помутнением, неприятными ароматами и вкусом, хотя в целом не представляет опасности для здоровья[23].
Эффективность пастеризации в борьбе с бактериями зависит от температуры и времени выдержки пива при данной температуре. Так называемая условная единица пастеризации (PE англ. pasteurization unit) находится по следующей формуле:
- PE = время [мин] • 1,393 (используемая температура −60 °C)
При использовании температуры 60°С в течение одной минуты получается 1 PE; при температуре 70 °С она составит 27,5PE[24]. Значение 8-30 PE обычно используется для стабилизации пива. Избегают неоправданно высоких значений из-за возможных неблагоприятных органолептических изменений и излишних затрат энергии[25].
В целом свежее пастеризованное пиво по вкусу не отличается от непастеризованного, в то время как в случае непастеризованного пива, несколько недель существует значительный риск его порчи. По этой причине в 1980-е годы в магазинах нередко можно было встретить кислое пиво, а пастеризованное пиво приравнивалось к пиву более высокого качества. В настоящее время увеличенный срок хранения непастеризованного пива достигается за счёт микрофильтрации, которая стерилизует пиво не только от микроорганизмов, но и от ценных белков и полифенолов[26].
Ферментативные реакции при затирании
Целью затирания солода является получение сусла, содержащего соответствующее количество сбраживаемых сахаров, питательных веществ для дрожжей и вкусовых соединений (или прекурсоров)[27]. При затирании происходит расщепление углеводов, β-глюканов и белков под действием амилаз, β-глюканаз и протеаз соответственно[28].
Углеводы составляют около 90 % экстракта базового сусла, из которых обычно 67—77 % составляют сбраживаемые сахара. Наиболее важным сбраживаемым сахаром является мальтоза[29].
Соложеный ячмень является основным источником углеводов в процессе производства пива[28][29], но также может быть заменён другими злаками в различных формах, такими как пшеница, рис, кукуруза и сахарные сиропы[29]. Солод содержит амилолитические ферменты, расщепляющие растворённый (склеенный) крахмал на сахара, которые дрожжи затем используют для производства спирта[28].
Содержание углеводов в готовом пиве обычно составляет от 3 до 61 г/л. Лагеры обычно характеризуются более высокой степенью сбраживания, чем пиво верхового брожения, и, следовательно, более низким содержанием углеводов[29].
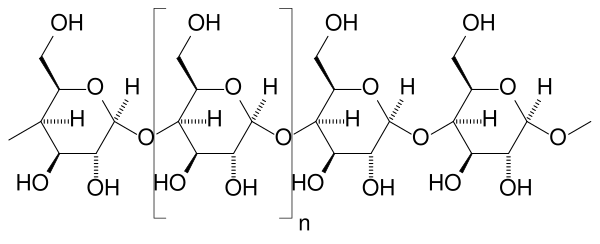
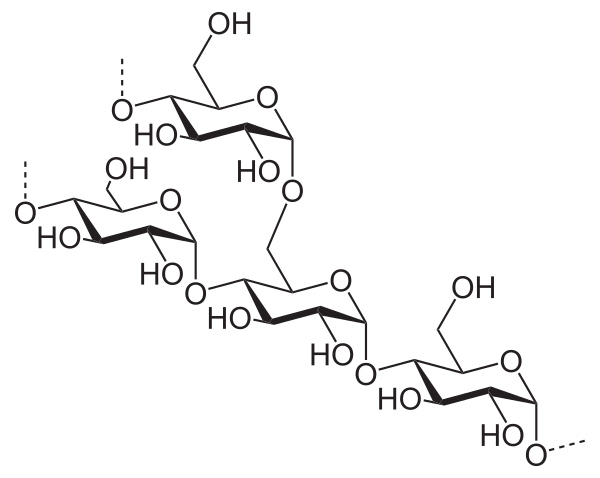
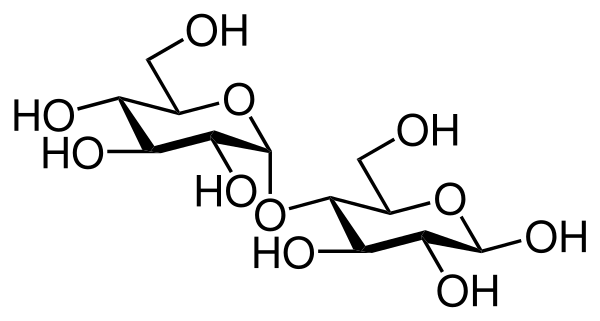
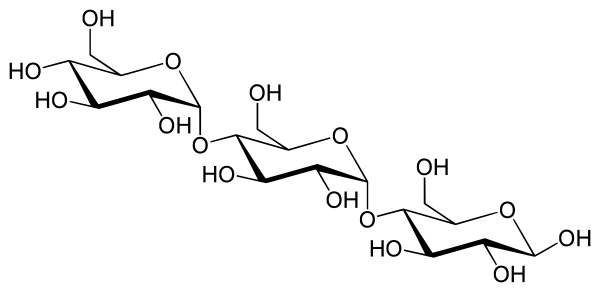
Крахмал состоит из двух полимеров глюкозы: амилозы (обычно 20—25 %) и амилопектина (75—80 %). Амилоза представляет собой линейный полимер, состоящий из звеньев глюкозы (до 6000), связанных α-1,4-гликозидной связью. Амилопектин состоит из цепей, состоящих из молекул глюкозы, связанных α-1,4-гликозидными связями, и боковых цепей, образованных α-1,6-гликозидными связями. Растворение крахмала в воде происходит при повышенной температуре и называется желатинизацией[30]. Температура склеивания зависит от происхождения крахмала, но обычно составляет от 65 до 75°С[31]. При затирании, благодаря взаимодействию ферментов и хорошему разрыхлению солода, оно может начинаться при более низкой температуре[32][31]. Затем гранулы крахмала, содержащиеся в солоде, набухают и ломаются, а его вязкость возрастает[30]. Затем ферменты солода гидролизуют крахмал. К ним относятся α-амилаза, β-амилаза, предельная декстриназа и α-глюкозидаза[33].
α-амилаза относится к эндоамилазам — она разрезает α-1,4-гликозидные связи внутри молекулы крахмала случайным образом, за исключением связей, расположенных в непосредственной близости от разветвлений[31]. Продуктом её деятельности являются декстрины различной длины[32] и небольшое количество ферментирующих сахаров (глюкозы, мальтозы, мальтотриозы), особенно, когда она затрагивает уже относительно небольшие молекулы. α-амилаза в результате быстрого уменьшения размера частиц крахмала вызывает значительное снижение вязкости затора, поэтому её называют «разжижающим ферментом». Она повышает доступность крупных молекул крахмала для действия β-амилазы. α-амилаза выдерживает температуру выше 70 °С, при которой β-амилаза очень быстро денатурирует[31].
β-амилаза относится к экзоамилазам. Она атакует невосстанавливающие концы амилозы и амилопектина, гидролизуя каждую вторую α-1,4-гликозидную связь. В результате его действия высвобождается мальтозный сахар, из-за чего её называют «ферментом осахаривания». Активность фермента прекращается при приближении к точке ветвления, поэтому в течение достаточно длительного времени он способен гидролизовать целые молекулы амилозы, но только наружные участки амилопектина, оставляя предельные декстрины[31].
Предельная декстриназа представляет собой фермент, ответственный за расщепление α-1,6-гликозидной связи и, таким образом, устранение ответвлений амилопектина и декстринов. Однако активность этого фермента при затирании низкая[33][34], о чём свидетельствует значительное количество разветвлённых декстринов в сброженном сусле и пиве[33].
α-глюкозидаза представляет собой экзоамилазу, которая высвобождает одиночные молекулы глюкозы с восстанавливающего конца полисахаридов, расщепляя α-1,4-гликозидные связи. Этот фермент оптимально работает при температуре 35—40 °C[35], он термолабилен и поэтому не имеет большого значения в процессе затирания[33].
В результате действия амилолитических ферментов окончательно получаем:
- неферментируемые декстрины разной длины;
- мальтотриоза используется сильно ферментирующими дрожжами только после использования мальтозы и других дисахаридов, то есть только во время старения[34]. Она может быть использована быстрее штаммами дрожжей низового брожения, чем при верховом брожении[36]. Мальтотриоза образуется в больших количествах, когда условия затирания благоприятствуют действию α-амилазы[31];
- мальтоза и небольшое количество других дисахаридов (например, сахароза), используемых дрожжами;
- простые сахара (глюкоза, фруктоза)[33] используются дрожжами в первую очередь[34].
Основным компонентом клеточных стенок эндосперма ячменя являются β-глюканы — линейные полимеры глюкозы, которые в описываемом здесь случае связаны β-1,3-гликозидами (примерно 30 %) и β-1,4-гликозидами (примерно 70 %). Степень деградации β-глюкана зависит от степени замачивания ячменя, количества ферментов, разрушающих клеточные стенки, и структуры стенок[29]. В реакциях ферментативного разложения участвуют:
- β-глюкансолюбилаза — карбоксипептидаза, удаляющая сложноэфирные связи между белками и β-глюканами;
- эндо-β-глюканазы — гидролизуют β-глюканы до три- и тетрасахаридов;
- экзо-β-глюканазы — гидролизуют β-глюканы до глюкозы[29].
Арабиноксиланы являются основным компонентом клеточных стенок алейронового слоя[37]. Арабиноксиланы являются частично водорастворимыми полимерами и переходят из солода в сусло как путём физического растворения в воде, так и под действием арабиноксилангидролаз. Они состоят из β-(1,4)-ксиланов, к которым присоединены остатки арабинозы в положении С2 или С3 ксилозы[38].
Как неполный распад β-глюканов, так и избыток выделяющихся арабиноксиланов могут вызвать проблемы с фильтрацией (эти соединения повышают вязкость сусла) и образование помутнения при хранении пива[37]. β-глюканы могут осаждаться даже при относительно низкой концентрации, но арабиноксиланы более устойчивы к разложению и их концентрация в готовом пиве в несколько раз выше[37].
Наиболее распространённым белком в зерне ячменя является гордеин(40—50 %), относящийся к проламинам. Кроме того, существуют, в том числе, альбумины, глютелины, глобулины, серпины и ферменты. Белки играют важную роль в образовании и поддержании пены, влияя на текстуру, цвет и пищевую ценность пива. Они могут участвовать в образовании мути[33]. Частичное разложение белков при соложении и затирании приводит к образованию аминокислот, необходимых для метаболизма дрожжей, а также участвующих в реакциях Майяра[39].
Только около 20 % белков ячменя растворимы в воде[40]. Специальный параметр в виде числа Кольбаха используется для оценки протеолитической активности и растворимости белков солода[39][41].
В польских условиях содержание белка в зерне ячменя обычно слишком велико (более 11,5 %), что приводит к неравномерному прорастанию при солодоращении, снижению экстрактивности солода и избытку соединений азота, а значит, к склонности к образованию помутнений. Содержание белка ниже 9 % указывает на слишком низкую ферментативную активность[41].
Содержание свободного аминоазота, то есть доступной для дрожжей формы азота в виде аминокислот, коротких пептидов и ионов аммония, должно быть не менее 200 мг/дм³, а в случае использования несоложеного сырья — не менее 150 мг/дм³[41]. В то же время недостаток белков высокой и средней молекулярной массы приводит к плохому пенообразованию и отсутствию ощущения «наполненности» в текстуре пива, поэтому желательно добиться оптимальной степени их разложения[39]. Стабильная, тонкая пенная шапка пива является не только важной визуальной характеристикой. Ингредиенты ароматизаторов накапливаются в пене в большей или меньшей степени. Пена медленно высвобождает ароматические компоненты, характерные для данного видавидов пива, и это помогает сохранять его свежим при употреблении[42].
Концентрация белков снижается не только при их ферментативном расщеплении, но и на последующих стадиях производства пива:
- при кипячении сусла, когда оно коагулирует и удаляется в виде горячего осадка;
- при понижении рН в процессе брожения подвергаются седиментации;
- при выдержке пива, когда они прилипают к дрожжевым клеткам[40].
В процессе затирания важно получить оптимальную степень гидролиза крахмала, белков и β-глюканов и использовать максимальное количество солодового экстракта. Это зависит от условий затирания, то есть в основном от:
- температуры и времени выдержки браги при заданной температуре (так называемые перерывы);
- рН затора;
- плотности затора[32].
Оптимальные диапазоны температур и рН для ферментативного разложения при затирании следующие:
| Ферменты | Температура (°С) [28] | рН [32] | Действие |
|---|---|---|---|
| β-глюканаза | 40-45 | 5,4-5,8 | разрушать клеточные стенки |
| экзопептидазы | 40 | 7,0-8,0 | расщепляют белки, гидролизуя концевые пептидные связи |
| эндопептидазы | 50-65 | 4,0-4,6 | расщепляют белки внутри полипептидной цепи |
| β-амилаза | 60-65 | 5,4-5,6 | расщепляют крахмал с образованием ферментируемых сахаров |
| α-амилаза | 65-75 | 5,6-6,8 | расщепляют крахмал, в основном образуя декстрины |
Несмотря на разные оптимальные условия работы, ферменты встречаются в заторе одновременно, и количество их активных молекул под влиянием повышения температуры может только уменьшаться (инактивироваться), если только не используются экзогенные ферменты микробного происхождения. При определении способа затирания на практике учитывают температуры, близкие к оптимуму нескольких ферментов:
- 37—45 °С — β-глюкановый разрыв, ферментативное расщепление компонентов клеточной стенки;
- 45—55 °С — распад белка, образование аминокислот;
- 62—65 °С — разрыв мальтозы, образование бродильного экстракта;
- 70—76 °С — перерыв в осахаривании, интенсивное образование предельных декстринов из крахмала;
- 76—78 °С — конец затирания, инактивация ферментов[32][43].
Длительное затирание при температурах 62—64 °С приводит к образованию большого количества сбраживаемых сахаров, достижению высокой степени аттенюации и высокого содержания алкоголя. Длительное истирание при температуре 72—75 °C приводит к тому, что в пиве остаётся много декстринов, а степень аттенюации низкая[34]. Декстрины не имеют вкуса, но влияют на вязкость и способствуют ощущению «наполненности», придают пиву текстуру[44].

Схема повышения настойной браги (слева) и отварной браги (справа)
Для получения соответствующих температур и зазоров используются различные стратегии. При восходящем методе настаивания брагу медленно нагревают до нужной температуры, делая паузы. При отварном методе часть браги кипятят (в основном для лучшего склеивания крахмала) и затем смешивают с остальным [32] .
Для получения соответствующих температур и зазоров используются различные стратегии. При восходящем методе настаивания брагу медленно нагревают до нужной температуры, делая паузы. При отварном методе часть браги кипятят (в основном для лучшего склеивания крахмала) и затем смешивают с остальным [32] .
Наконец, температура затора повышается примерно до 78°С (англ. mash-out). Хотя фильтрация более эффективна при ещё более высоких температурах из-за снижения вязкости, этот предел, тем не менее, не превышают. При фильтрации в раствор всё ещё переходит неразложившийся крахмал, который может гидролизоваться ещё активной α-амилазой. При более высоких температурах этот фермент может вообще не быть активным, и в готовом пиве может быть обнаружен крахмал, вызывающий помутнение[34].
На многих пивоваренных заводах упор на сокращение времени производства и снижение затрат популяризировали в производстве пива метод, называемый пивоварением высокой плотности (HGB)[45], который не требует дополнительных инвестиций[46]. Он заключается в получении сусла с гораздо более высоким содержанием экстракта, чем предполагаемый экстракт готового пива. После брожения такое пиво разбавляют водой до нужной экстрактивности. Это позволяет не только повысить эффективность варочного цеха, но, прежде всего, сэкономить энергию, так как добавленную позже воду не нужно нагревать и кипятить[47]. Достигаемая таким образом более высокая концентрация спирта (до разбавления) увеличивает осаждение белково-полифенольных комплексов, что способствует коллоидной стабильности. Соответствующее разбавление позволяет легко контролировать конечное содержание сахара и алкоголя в пиве[46].
Необходимую высшую экстрактивность иногда получают кратчайшим путём, например добавлением сахара или глюкозно-фруктозного сиропа, который затем увеличивает степень брожения пива[47]. Заменители солода вносят в сусло только углеводы, они не содержат питательных веществ, необходимых для дрожжей[46]. Однако пиво, произведённое с их участием, может быть более устойчивым к выдержке. Можно производить пиво полностью без солода, из 100 % несоложёного ячменя с добавлением экзогенных ферментов, качество которых сравнимо с получаемым из солода[48].
Метод HGB, особенно с большими экстрактами, отрицательно влияет на дрожжи через осмотический стресс, повышенную концентрацию этанола, CO2, что, в свою очередь, приводит к перепроизводству сложных эфиров (фруктовые ароматы, ароматы растворителей), длительной адаптационной фазе роста дрожжей, снижению стабильности пены и увеличению количества остаточных сахаров в пиве[45]. Кроме того, ухудшается состояние дрожжей, что снижает их эффективность в случае инокуляции (формировании) следующего сусла. Чем выше экстракт сусла, тем больше необходимое время ферментации. Одним из способов повышения эффективности брожения в таких условиях является увеличение количества дрожжей, добавляемых в закваску сусла. Это вызывает более высокую аттенюацию (более высокое содержание этанола), немного более высокую концентрацию сивушных спиртов и более высокий уровень диацетила в зелёном пиве. Ещё одним методом улучшения брожения является добавление в сусло питательных веществ для дрожжей (содержащих цинк, магний и липиды)[45].
Карбонильные соединения
Наиболее важными карбонильными соединениями в пиве являются ацетальдегид и вицинальные дикетоны (имеющие карбонильные группы в соседних положениях), поскольку они имеют самые низкие пороги обнаружения[49].
Ацетальдегид является предшественником этанола и ацетатов. В малых концентрациях даёт приятный фруктовый аромат; но в более высоких, он вызывает неприятный, раздражающий запах, напоминающий запах зелёного незрелого яблока или свежескошенной травы[3][50]. Его концентрация считается одним из важнейших факторов, влияющих на аромат и стабильность пива[50]. Более того, это может способствовать снижению срока годности пива, поэтому цель состоит в том, чтобы ограничить количество этого соединения[51]. В недефектном готовом пиве содержание ацетальдегида обычно составляет от 2 до 10 мг/л[52] и рекомендуется не превышать 35 мг/л[53].
Ацетальдегид образуется под действием пируватдекарбоксилазы в процессе декарбоксилирования пирувата. Наиболее интенсивно он образуется в фазу активного роста дрожжей, при наиболее сильном выделении CO2. На поздней стадии брожения ацетальдегид восстанавливается до этанола алкогольдегидрогеназой Adh1. Эта реакция происходит, когда присутствуют ферментируемые источники углерода. Его биологическая функция заключается в регенерации NAD+. Когда источники углерода истощаются, произведённый этанол используется для выработки энергии. Изофермент алкогольдегидрогеназы — Adh2 окисляет этанол до ацетальдегида. Это, в свою очередь, может быть использовано в цикле Кребса или в глюконеогенезе[54]. Таким образом, самые высокие уровни ацетальдегида во время бурного брожения, падают до низкого уровня в конце брожения и после медленно увеличиваются с течением времени, например. из-за окисления этанола и активности дрожжей[55]. Вмешиваясь в экспрессию гена ADH2, можно эффективно снизить количество ацетальдегида в пиве. Таким образом, с помощью традиционного метода мутагенеза удалось получить штамм дрожжей, который продуцирует на 80 % меньше ацетальдегида, чем обычно используемые промышленные штаммы[51].
Более высокая концентрация ацетальдегида отмечается при повышенной температуре брожения, но его деградация в таких условиях происходит быстрее. Более высокие концентрации достигаются также при высоком содержании соединений азота в сусле, что увеличивает интенсивность брожения[56]. Более того, различные штаммы Saccharomyces cerevisiae способны вырабатывать его в различных диапазонах концентраций[57][58]. В готовом пиве ацетальдегид легко образуется из этанола при наличии кислорода. Однако большинство коммерческого пива разливается в бутылки с очень низкой концентрацией кислорода (ниже 0,2 мг/л), что существенно ограничивает этот процесс[59].
В выдержанном пиве особое влияние на аромат оказывает высокая концентрация транс-2-ноненаля и ацетальдегида. Наличие активных форм кислорода способствует их избыточному образованию[60]. Радикал, который встречается в наибольшем количестве в старом пиве, представляет собой 1-гидроксиэтильный радикал, образованный реакцией этанола с гидроксильными радикалами. Основным продуктом его разложения является ацетальдегид[61]. Ацетальдегид со временем подвергается реакциям альдольной конденсации, что может привести к образованию неблагоприятных соединений. Путём конденсации ацетальдегида и гептаналя может образовыванться транс-2-ноненаль[62][63]. Транс-2-ноненаль создаёт нежелательные запахи, известные как запах мокрого картона. Другие алифатические альдегиды (C4—C10) также отрицательно влияют на аромат и могут придавать неприятный букет стареющему пиву[64].
Наиболее важными вицинальными дикетонами пива являются диацетил (2,3-бутандион) и 2,3-пентандион[65]. Они образуются при брожении как побочные продукты дрожжей в ходе биосинтеза аминокислот. Аромат диацетила описывается как маслянистый, напоминающий молочную карамель, а аромат 2,3-пендандиона похож на аромат ириски. Они наиболее ярко выражены в светлом пиве, где не преобладают другие ароматы. По этой причине необходимо минимизировать их количество, особенно в лагерах[66].
Диацетил и 2,3-пентандион образуются в результате спонтанного неферментативного окислительного декарбоксилирования α-ацетогидроксикислот, являющихся промежуточными продуктами биосинтеза валина и изолейцина[67]. На основе отрицательной обратной связи доступность валина в дрожжевой клетке связана с ингибированием обратной связи ацетолактатсинтазы, которая необратимо превращает пируват в α-ацетолактат (предшественник диацетила), а α-кетобутират в α-ацетогидроксибутират (предшественник 2,3-пентандиона)[68].
Диацетил также может образовываться в результате активности инфекционных бактерий, в основном молочнокислых бактерий[69], среди которых наиболее проблемным типом в пивоварении является род Pediococcus[65].
При синтезе валина в клетках дрожжей лимитирующей стадией реакции является превращение α-ацетолактата в 2,3-дигидроксиизовалерат. Некоторые молекулы α-ацетолактата секретируются вне дрожжевой клетки в сусло, где они подвергаются неферментативному окислительному декарбоксилированию до диацетила или неокислительному декарбоксилированию с образованием ацетоина[67]. Последний, предпочтительный тип декарбоксилирования можно стимулировать лёгким нагреванием в анаэробных условиях и поддержанием низкого окислительно-восстановительного потенциала в сусле[70]. Пивные дрожжи не продуцируют фермент α-ацетолактатдекарбоксилазу, который катализирует эту реакцию[71].
Таким образом, продукция диацетила зависит от интенсивности биосинтеза валина, который, в свою очередь, зависит от потребности и доступа клеток к этой аминокислоте[67]. Чем больше валина в дрожжевой клетке, тем меньше будет произведено предшественников этих соединений. Однако высокая доступность валина в сусле не останавливает полностью биосинтез этой аминокислоты. Валин не относится к аминокислотам, быстро усваиваемым дрожжами (к которым относятся глутаминовая кислота, аспарагиновая кислота, аспарагин, глутамин, серин, треонин, лизин и аргинин)[72], и его поглощение в течение первых 12 часов ферментации происходит обычно очень медленно[67]. Добавление легкоусвояемых аминокислот, а также высокая концентрация свободного аминного азота (который включает эти предпочтительные аминокислоты) приводят к увеличению производства диацетила. В таком случае поглощение валина клетками происходит слишком медленно, аминокислоты конкурируют за доступ к пермеазам, и он должен более интенсивно биосинтезироваться, увеличивая концентрацию предшественников вицинального дикетона. Повышение концентрации диацетила происходит также при слишком низком уровне свободного аминного азота (ниже 150 ppm) — в этом случае также необходим биосинтез валина. Дополнение сусла одним валином (100—300 мг/л) может, однако, снизить концентрацию диацетила после ферментации до 33 % в случае Saccharomyces pastorianus[73].
Содержание валина в сусле также можно регулировать условиями затирания. Оптимальные условия для выделения из солода наибольшего количества валина 50 °С, рН 5,4, продолжительность 60—75 мин[67]. Важен и способ производства солода — его низкая температура сушки способствует сохранению большего количества валина и других аминокислот[74]. Наибольшее количество валина содержится в овсяных солодах — 5,0—5,7 % белковых аминокислот. Для сравнения, ячменный солод содержит в среднем 4,7—4,9 %, а пшеничный солод — 4,4 %[67].
Дрожжи способны поглощать и восстанавливать вицинальные дикетоны до спиртов, которые имеют очень высокий порог обнаружения и практически не влияют на аромат. 2,3-пентандион восстанавливается до 2,3-пентандиола, а диацетил восстанавливается до ацетоина, который в конечном итоге восстанавливается до 2,3-бутандиола. С точки зрения биологии дрожжей такое восстановление выгодно ещё и потому, что его продукты менее токсичны, чем субстраты[75]. Многие различные, специфические и неспецифические НАДН или НАДФН-зависимые кетонредуктазы участвуют в восстановлении. Однако алкогольдегидрогеназа, вероятно, наиболее активна в этом процессе[65]. Точные механизмы этих процессов ещё недостаточно изучены[67].
Восстановление вицинальных дикетонов начинается уже при турбулентном брожении, но только при выдержке (молчаливом брожении) их концентрации падают до уровней ниже порога обнаружения. Лагерам нужно больше времени[73]. Процесс удаления диацетила является ограничивающим этапом созревания пива[66]. В то же время делается экономический упор на сокращение продолжительного и энергозатратного процесса созревания, возможно, без негативного влияния на качество пива[73].
На снижение влияют параметры, связанные с проницаемостью мембран (например, температура, оксигенация)[76], связанные со скоростью размножения дрожжей (например, pH, температура) и связанные с активностью ферментов, ответственных за это снижение. Более высокие температуры брожения ускоряют образование диацетила в результате более быстрого роста дрожжей, увеличивают его максимальную концентрацию, достигаемую при брожении пива, но в то же время большая биомасса дрожжей в этих условиях быстрее снижает концентрацию диацетила. Наиболее быстрое превращение α-ацетолактата в диацетил, а также восстановление диацетила происходит при рН 3,5. Таким образом, время созревания можно сократить, достигнув минимально возможного значения рН пива[67]. Однако типичные значения pH выше, около 4,5, и его снижение не всегда полезно с точки зрения других сенсорных характеристик[77].
Экспериментально показано, что уровень экзогенного диацетила, добавляемого в ферментационный бульон, быстро падает до уровня контрольного ферментационного бульона. Однако чем позднее это происходит при брожении, тем медленнее снижается его концентрация[76]. Эти результаты позволяют предположить, что лимитирующей стадией является не восстановление диацетила, а спонтанное декарбоксилирование α-ацетолактата в диацетил, и что важно хорошее состояние дрожжей в этом процессе[67]. Поэтому в созревающее зелёное пиво целесообразно добавлять 5—10 % сбраживаемого сусла[78]. Этот процесс называется «краузенинг» от немецкого слова Kräusen, означающего брожение сусла в фазе высокого диска. Он эффективно удаляет диацетил и другие нежелательные ароматы, активно преобразуемые дрожжами. Его также можно использовать в закрытых резервуарах для естественного насыщения пива CO2[79].
Чрезмерный уровень диацетила является проблемой при попытках непрерывного брожения с иммобилизованными дрожжевыми клетками. Это связано, в частности, с недостаточным временем ферментации для усвоения и восстановления этого соединения, с повышенной экспрессией гена ацетолактатсинтазы (ALS) и изменением обмена аминокислот в иммобилизованных дрожжевых клетках. Между тем эти проблемы могут быть решены за счёт использования генетически модифицированных дрожжей, например, с введенным бактериальным геном α-ацетолактатдекарбоксилазы[71]. Однако на практике для борьбы с избыточным количеством вицинальных дикетонов не применяют генетически модифицированные штаммы дрожжей, экзогенные ферменты или интенсивное нагревание. В последнем случае пиво пришлось бы нагревать до 90 °С, чтобы полностью избавиться от α-ацетолактата в течение 10 минут[65].
Многие другие альдегиды и кетоны отрицательно влияют на аромат пива. Их источниками являются реакции Майяра при сушке солода, распад жирных кислот и реакции окисления при хранении. Наиболее важные карбонильные соединения в пиве включают[80]:
| Карбонильное соединение | Аромат | Источник |
|---|---|---|
| 2-метилпропаналь | злаки, растворитель, фрукты | деградация валина; это также может быть результатом окисления при хранении и выдержке пива. |
| 2-метилбутаналь | миндаль, яблоко и солод | расщепление изолейцина по Штрекеру; это также может быть результатом окисления |
| 3-метилбутаналь | солодовый, шоколадный, миндальный | расщепление лейцина по Штрекеру; это также может быть результатом окисления |
| гептаналь | пряный, фруктовый, винный | расщепление жирных кислот при выдержке пива |
| октановое число | пряный, фруктовый, апельсиновый | расщепление жирных кислот при выдержке пива |
| фурфурол | карамель, хлеб, жареное мясо | продукт реакции Майяра |
Спирты и сложные эфиры
Этанол является одним из основных продуктов метаболизма дрожжей. В первую очередь это соединение отвечает за согревающие свойства пива, хотя это сенсорное впечатление в этом напитке снижается из-за присутствия CO2. Этанол усиливает восприятие сладости и реагирует с кислотами, в том числе хмелевого происхождения, с образованием сложных эфиров[81]. Это способствует приданию пиву тела[82]. Этанол, как и сахара, снижает способность ощущать нежелательные альдегидные ароматы[83]. Он создаёт один из основных барьеров, ограничивающих рост инфекционных бактерий[84].
Высшие спирты (сивушные спирты) содержат более 2 атомов углерода в молекуле, имеют более высокую молекулярную массу и температуру кипения, чем этанол[85]. Они возникают как побочные продукты спиртового брожения. На сенсорные свойства больше всего влияют пропанол-1, изобутанол и изомеры амилового спирта: 2-метилбутанол и 3-метилбутанол. Они способствуют согревающему характеру пива и усиливают аромат этанола[86]. Они могут придавать цветочные ароматы, подобные растворителям[87], а их избыток может вызывать неприятный резкий запах и вкус[85].
Высшие спирты можно получить катаболическим или анаболическим путями. Катаболический путь преобладает в сусле, богатом аминокислотами, где высокое содержание α-кетокислот тормозит анаболический путь. В случае дефицита аминокислот в бульоне α-кетокислоты образуются de novo из сахаров и преобладает анаболический путь[86].
Катаболический путь, так называемый путь Эрлиха предполагает, что аминокислота претерпевает реакцию трансаминирования до α-кетокислоты, затем декарбоксилирования до сивушного альдегида и восстановления до высшего спирта[87]. Реакция трансаминирования представляет собой обратимую реакцию, регулируемую ферментами, которые катализируют перенос аминогрупп между аминокислотами и соответствующими им α-кетокислотами с помощью глутаматдегидрогеназы. Стадия декарбоксилирования декарбоксилазами необратима. Алкогольдегидрогеназы и ацетальдегиддегидрогеназы способны восстанавливать сивушные альдегиды до спиртов[87][88].
Те же α-кетокислоты, участвующие в пути Эрлиха, могут возникать при синтезе аминокислот de novo из соединений, образующихся в результате углеводного обмена. За это отвечает ряд различных ферментов, в зависимости от биосинтетического семейства аминокислот. Следовательно, на содержание сивушных веществ в пиве влияет доступность аминокислот в окружающей среде, определяемая, в том числе, по составу шихты и типу питательных веществ[89]. Условия брожения также важны. Окисление альдегидов преобладает в оксигенированных бульонах с дефицитом глюкозы. Аминокислоты затем превращаются в основном в сивушные кислоты[90]. Более высокие температуры брожения увеличивают количество высших спиртов, в то время как в случае брожения под давлением наблюдается противоположный эффект[86]. Ключевым фактором для производства сивушных спиртов является используемый штамм дрожжей. В целом штаммы дрожжей верхового брожения производят больше высших спиртов, чем штаммы дрожжей низового брожения[91].
Высшие спирты являются предшественниками сложных эфиров. Эфиры — продукты конденсации органических кислот и спиртов. Хотя их концентрация в пиве очень низкая, даже эти небольшие количества очень хорошо ощущаются и могут повлиять на конечный аромат пива[92]. Более того, наличие небольшой концентрации различных эфиров может оказывать синергетический эффект[93]. Они могут придать пиву сладкий фруктовый аромат[94], но в избытке они приводят к неприятной вкусовой горечи[87]. В целом, сложные эфиры нежелательны в большинстве лагеров, где ожидается чистый солодовый профиль.
При синтезе сложных эфиров органические кислоты соединяются с коферментом А при участии ацил-КоА-синтетаз с образованием ацил-КоА. На втором этапе молекулы ацил-КоА соединяются со спиртом при участии алкоголь-ацилтрансфераз с образованием сложных эфиров[87]. Сложные эфиры в пиве можно разделить на две основные группы: эфиры уксусной кислоты и этиловые эфиры жирных кислот со средней длиной цепи[95].

Биосинтез сложных эфиров у Saccharomyces cerevisiae
Сначала образуется ацил-КоА, который затем реагирует со спиртом. В случае сложных эфиров уксусной кислоты ацетил-КоА (ацил-КоА) реагирует со спиртом. При образовании этиловых эфиров этанол (спирт) реагирует с ацил-КоА.
Сначала образуется ацил-КоА, который затем реагирует со спиртом. В случае сложных эфиров уксусной кислоты ацетил-КоА (ацил-КоА) реагирует со спиртом. При образовании этиловых эфиров этанол (спирт) реагирует с ацил-КоА.
Биосинтез эфиров уксусной кислоты осуществляется следующим образом. Ацетил-КоА, который после этерификации образует ацетаты, получают окислительным декарбоксилированием пирувата или прямой активацией ацетата АТФ (реакция ацетилирования КоА). В анаэробных условиях не используется в цикле Кребса, поэтому подвергается этерификации — соединяется со спиртами. Катализатором реакции являются алкогольацилтрансферазы (ААТазы), кодируемые генами ATF1 и ATF2. Сверхэкспрессия этих генов может значительно увеличить концентрацию этих эфиров в пиве[87].
Этиловые эфиры жирных кислот со средней длиной цепи образуются в результате этерификации более длинных цепей ацил-КоА этанолом[87][95] . Эта реакция катализируется другими алкоголь-ацилтрансферазами — ацил-КоА/этанол О-ацилтрансферазами (AEATases), кодируемыми генами EEB1 и EHT1[87]. Однако в аэробных условиях молекулы ацил-КоА могут подвергаться β-окислению с образованием единиц ацетил-КоА, вступающих в цикл Кребса. Синтез сложного эфира в этих условиях ингибируется. Кроме того, присутствие ненасыщенных жирных кислот ингибирует их синтез за счёт ингибирования алкоголь-ацилтрансферазы[86][96] .
Хотя можно обнаружить более 100 эфиров в пиве[93], только шесть из них считаются наиболее влиятельными в формировании букета. Это: этилацетат (ароматизатор растворителя), изоамилацетат (банан), изобутилацетат (фрукты), 2-фенилэтилацетат (роза, мед), этилгексаноат (сладкое яблоко, анис) и этилоктаноат (кислое яблоко)[87][95]. Наиболее распространён этилацетат, концентрация которого достигает 10—20 ppm. Концентрации остальных эфиров обычно не превышают 1 ppm[97]. Дрожжи верхового брожения обычно производят больше сложных эфиров, чем дрожжи низового брожения. В пиве верхового брожения обычно ощутимы как этилацетат, так и этилгексаноат. В специфических бельгийских ламбиках, полученных путём спонтанного брожения с использованием диких дрожжей и бактерий (энтеробактерий, клоккеров, педиококков, уксуснокислых бактерий, штаммов сахаромицетов, деккера — ранее бреттаномицетов), присутствуют значительные количества этилдеканоата, отсутствующие в других видах пива[98].
Со временем выдержки эфирный профиль пива может значительно измениться, как под влиянием живых дрожжей (в нефиксированном пиве), так и за счёт самопроизвольной конденсации органических кислот с этанолом[92]. Органические кислоты, полученные из окисленных компонентов хмеля, могут образовывать сложные эфиры с винным, сладким характером, в то время как фруктовые эфиры со временем могут подвергаться гидролизу[87].
Добавка в сусло ZnSO4 может более чем удвоить концентрацию некоторых эфиров[99]. Точно так же увеличение концентрации свободного аминного азота (например, путём добавления протеаз в сусло) приводит к увеличению конечной концентрации сложных эфиров[100]. Более высокие температуры благоприятствуют образованию сложных эфиров, влияющих не только на кинетику реакции, но и на метаболизм дрожжей и химический состав пива[99]. Повышенное давление во время ферментации вызывает чрезмерную концентрацию CO2 и, как следствие, замедляет реакции декарбоксилирования, важные для образования спиртов и предшественника эфиров уксусной кислоты — ацетил-КоА[101].
Наиболее эффективным средством контроля концентрации спиртов и эфиров являются генетические модификации штаммов дрожжей. Например, штаммы дрожжей, у которых отсутствует ген IAH1, кодирующий изоамилацетат-гидролизующую эстеразу, могут давать пиво, в 19 раз более богатое этим эфиром[102]. Штаммы, лишённые гена BAT2 и сверхэкспрессирующие ген ATF1 (кодирующий алкоголь-ацетилтрансферазу), эффективно снижают концентрацию нежелательных высших спиртов и повышают концентрацию желаемых эфиров[103].
На основе приведённых выше зависимостей можно успешно разработать систему контроля концентрации сивушных эфиров и спиртов. Это позволяет получать пиво с желаемым уровнем этих соединений даже при использовании большого количества несоложеного сырья или при использовании нестандартных температур при брожении[104].
Фенольные соединения
Фенольные соединения, полученные из солода и хмеля, придают пиву аромат, терпкость, тело и прозрачность. В качестве антиоксидантов они противодействуют неблагоприятным последствиям окисления, продлевая срок хранения пива и положительно влияя на его полезные для здоровья свойства[105]. Мы можем выделить следующие классы фенольных соединений в пиве:
- простые фенолы (монофенолы), которые можно разделить на производные коричной кислоты (феруловая, кумаровая, синапиновая кислота, 4-винилфенол, 4-винилгваякол) и производные бензойной кислоты (ванилиновая кислота, ванилин, салициловая кислота, салициловый альдегид);
- флавоноиды, в состав которых входят катехины (или флаван-3-масла, такие как: катехины, эпикатехины, галлокатехины и их сложные эфиры), проантоцианидины (ди-, три- и олигомерные продукты конденсации мономеров флаван-3-ола, так называемые конденсированные дубильные вещества), халконы (например, ксантогумол), флаваноны (например, изоксантогумол), флавонолы (кверцетин, кемпферол);
- другие фенольные соединения, например, стильбеноиды (ресвератрол)[106][107].
Большинство фенольных соединений, содержащихся в пиве, практически не ощущаются, но могут проявлять синергетический эффект[108]. Относительно легко узнаваемые фенольные соединения в пиве включают гваякол, фенол, ванилин, эвгенол, 4-винилгваякол и 4-винилфенол[109].
Аромат простых фенольных соединений может быть как приятным (напоминающий ваниль, копчёности, гвоздику), так и неприятным (обычно именуемый «аптечным», «больничным»). Восприятие аромата 4-винилгваякола существенно меняется с увеличением его концентрации: на уровнях, близких к порогу обнаружения, это ваниль, при средних значениях — гвоздика, при очень высоких значениях — крепкий копченый или «аптечный» ароматы[108]. Это явление объясняется наличием обонятельных рецепторов, активирующихся только при более высоких концентрациях данного вещества[110].
Среди свободных фенольных кислот феруловая кислота (ФК) и п-кумаровая кислота (пКА) достигают относительно высоких концентраций в сусле. Эти гидроксикоричные кислоты (ГКА) в основном связаны с полисахаридами в клеточной стенке растений. В зерне они этерифицируются преимущественно арабиноксиланами, которые, помимо β-глюканов, являются важнейшими некрахмальными полисахаридами зерна[38]. Здоровое зерно ячменя содержит 4—10 % арабиноксилана, наиболее распространённого в алейроновой клеточной стенке[37]. Гидроксикоричные кислоты связаны с остатками арабинофуранозы в положении О5, при этом они отщепляются и растворяются в сусле за счет действия коричной эстеразы (КФ 3.1.1.73), встречающейся в природе в ячмене и ячменном солоде, во взаимодействии с синергетическими арабиноксилангидролазы[38].
Ферментативно растворенные фенольные кислоты ценятся за их антиоксидантные свойства, благодаря которым они способствуют стабильности пива[38]. Имея высокие пороги обнаружения, они, как правило, не влияют на аромат. Однако феруловая кислота и п-кумаровая кислота могут декарбоксилироваться с образованием соединений, сильно влияющих на букет пива — 4-винилгваякола и 4-винилфенола соответственно. Этот процесс происходит за счёт:
- высоких температур (например, при кипячении сусла, пастеризации пива);
- ферментативного декарбоксилирования во время брожения за счёт активности декарбоксилазы фенилакриловой кислоты дрожжей верхового брожения (фермент Pad1);
- активности инфекционных микроорганизмов (Enterobacteriaceae, молочнокислых бактерий, уксуснокислых бактерий, диких дрожжей Деккера)[109].
Термическое декарбоксилирование феруловой кислоты до 4-винилгваякола происходит в основном при кипячении сусла. Изменения начинаются при температуре 90 °С, а их уровень увеличивается со временем и интенсивностью нагрева. Термическое декарбоксилирование объясняет присутствие 4-винилгваякола в количестве, превышающем порог обнаружения в пиве, сброженном лагерными дрожжами[109].
Ферментативное декарбоксилирование регулируется геном PAD1, кодирующим phenylacrylic acid decarboxylase. Он активен только в случае верхового брожения и диких дрожжей. Ароматы, создаваемые этими соединениями, нежелательны в светлом пиве низового брожения, тогда как в бельгийском и немецком пиве Weizen они создают характерные приятные ароматические букеты[109].
Штамм дрожжей является важнейшим фактором, определяющим конечное содержание летучих фенолов в пиве за счёт участия в декарбоксилировании, но обязательным условием является наличие их предшественников. Содержание и эффективность извлечения оксикоричных кислот зависит от условий затирания. Максимальное ферментативное выделение феруловой кислоты происходит при температуре около 40 °С и рН 5,8 и почти полностью останавливается при 65 °C и pH ниже 4[38][111]. В случае водной (неферментативной) экстракции значение рН не влияет на эффективность этого процесса. При непрерывном перемешивании сусла его выделяется на 45 % больше, чем при не перемешивании сусла. Замес также имеет большое значение — было показано, что сусло, приготовленное из 50 % несоложеной пшеницы, содержит на 15—43 % меньше свободной феруловой кислоты, чем сусло из 100 % солодового ячменя[38].
В пиве, подвергнутом самопроизвольному брожению с использованием диких дрожжей, в небольшом количестве присутствуют винилфенолы, а также присутствуют этилфенолы: 4-этилфенол (4ЭФ) и 4-этилгваякол (4ЭГ). Эти соединения обычно не встречаются в неинфицированном пиве низового и верхового брожения[109]. Запах 4-этилпроизводных описывается как запах «животного загона» и «бинта»[112], они имеют более низкие пороги обнаружения. Они образуются путём декарбоксилирования гидроксикоричной кислоты до производного винилфенола с помощью фермента, аналогичного ферменту Pad1 у S. cerevisiae, с последующим восстановлением до соответствующего этилфенола с помощью Dekkera spp.[109]. Это восстановление не происходит у S. cerevisiae[113].
Было подсчитано, что фенольные соединения, наряду с меланоидинами и диоксидом серы, составляют 22—68 % антиоксидантной активности пива низового брожения, но фенольные соединения являются наиболее важными антиоксидантами в пиве[114]. Считается, что они благотворно влияют на здоровье, так как противодействуют окислительному стрессу в клетках, проявляют антиканцерогенные и антимутагенные свойства[115].
Хотя общее содержание полифенолов в белом вине намного выше, чем в пиве, оно обладает большей антиоксидантной активностью, чем пиво. Это связано с более высоким содержанием в пиве процианидинов, эпикатехинов и феруловой кислоты. Не все полифенолы биологически активны и биодоступны[116].
Сегодня уровень кислорода в пиве часто составляет всего 0,1 мг/дм³, но даже этого количества достаточно, чтобы со временем вызвать симптомы окислительного старения пива. Антиоксиданты играют ключевую роль в обеспечении физико-химической и ароматической стабильности[114].
Полифенолы солода растворяются в сусле во время затирания так же, как и монофенолы, но медленнее. Многие из них теряются в результате окисления, адсорбции на пульпе и осаждения при образовании комплексов с белками[105]. Использование в бункере несоложеного сырья дополнительно негативно влияет на содержание фенолов в сусле[115][117].
Наибольшее влияние на антиоксидантные свойства ячменя оказывают катехины, в том числе процианидин В3 и продельфинидин В3. Однако после процесса соложения и пивоварения их содержание резко снижается. Среди ингредиентов солодового происхождения наибольшую долю в создании антиоксидантных свойств пива имеют простые фенолы — феруловая кислота и синапиновая кислота, которые подвержены относительно небольшим потерям в процессе производства[117]. После всего технологического процесса общее содержание фенолов в пиве снижается примерно вдвое, особенно дубильных веществ (примерно на 90 %) и флавоноидов (примерно на 75 %)[115], в основном при фильтрации, пивоварении (горячий шлам, так называесый прорыв, охлаждением сусла и выдержкой (холодный шлам).
Антиоксидантные свойства хмеля описаны в более поздних публикациях как независимые от содержания в них полифенолов. Показано, что антиоксидантные свойства хмеля зависят в основном от гумулонов (α-кислоты) и лупулонов (β-кислоты). Значительно больше радикалов образуется в неразмолотом сусле. В то же время изомеризация α-кислот в изо-α-кислоты при кипячении сусла снижает его антиоксидантную способность[118].
Созревание пива в винных бочках, используемых в некоторых видах крафтового пива, оказывает большое влияние на содержание полифенолов. Было показано, что пиво, произведённое таким образом, имеет в 2,5 раза более высокое общее содержание полифенолов по сравнению с другим крафтовым пивом и в 3,6 раза больше, чем промышленное пиво. С этим тесно связана антиоксидантная активность[119].
Соответствующий уровень восстановительной силы предотвращает образование нежелательных ароматов, таких как транс-2-ноненаль. Это соединение не подвергается восстановительной активности дрожжей, поскольку оно связывается с соединениями азота, такими как аминокислоты или белки. Со временем он высвобождается в результате кислотного гидролиза, особенно при низком pH пива или при хранении пива при неподходящей температуре[120][121]. Высокое содержание фенолов за счёт повышения восстановительной способности пива улучшает органолептическую стабильность пива за счёт ингибирования синтеза транс-2-ноненаля и затруднения связывания с соединениями азота[120].
Полифенолы, хотя и улучшают полезные свойства и окислительную стабильность пива, могут оказывать негативное влияние на его коллоидную стабильность. Их высокое содержание способствует образованию белково-полифенольных комплексов, вызывающих помутнение. Белки, входящие в состав таких комплексов, происходят в основном из ячменя, они имеют размер 10—30 кДа, сильно гликозилированы, богаты пролином и глутаминовой кислотой, они составляют 3—7 % всех белков пива[122]. При участии пролина образуются нековалентные, обратимые гидрофобные взаимодействия и водородные связи между белками и полифенолами[123][124]. Более того, пролин предотвращает образование альфа-спирали и способствует формированию более открытой структуры[123]. Помутнение, вызванное этими комплексами, образуется при охлаждении пива до температуры, близкой к 0 °С и исчезают при нагревании (холодный осадок)[122]. Со временем хранения пива образуется всё больше постоянных ковалентных связей, что, вероятно, связано с окислением полифенолов и их последующей полимеризацией[125]. Чем больше фенольных мономеров в таком полимеризованном соединении, тем больше активность в образовании помутнения[123].
В пиве преобладают haze active proteins, с высокой долей пролина в цепи, над haze active polyphenols, которые включают в основном флаванолы, поэтому снижение содержания полифенолов представляется наиболее эффективным методом[124]. Их удаляют адсорбирующими средствами, в том числе поливинилполипирролидон (ПВПП), соединение, структурно подобное полипролину[123][124]. Однако этот агент удаляет только около половины образующих мутность полифенолов, потому что их молекулы захвачены между связывающими белками[124][126]. Более того, это также лишает пиво желаемых немутных полифенолов с антиоксидантными свойствами[124]. Для повышения эффективности стабилизации дополнительно удаляют белки. Этого можно достичь, например, с помощью силикагеля, к гидроксильным группам которого адсорбируются богатые пролином белки, оставляя белки с низким содержанием пролина, образующие пену в пиве[122]. Содержание белка также снижается при использовании бентонита, но его не рекомендуется использовать из-за ухудшения пенообразования (удаляет все белки)[123]. Другой метод заключается в изменении соотношения белок-полифенол и осаждении белково-полифенольных комплексов при низких температурах с использованием белков, богатых пролином, таких как желатин, изингласс или галлотанин (дубильная кислота), эквивалентный пивному полифенолу.
На образование белково-фенольных комплексов, помимо концентрации богатых пролином белков и полифенолов, влияет рН и, в меньшей степени, содержание спирта[123].
Полифенолы, особенно флавоноиды, могут вызывать вяжущие свойства и терпкость. Это сложный сенсорный опыт с ощущением сухости, стянутости и шероховатости на слизистой оболочке полости рта[127][128]. Химический механизм его образования идентичен механизму помутнения. Белки слюны, действующие как оральная смазка, особенно богатые пролином, связываются с полифенолами пива с образованием нерастворимых комплексов, что снижает увлажняющий потенциал слюны и вызывает ощущение стянутости[127]. Развитие вяжущих свойств стимулируется кислородом (окисление способствует полимеризации) и низким pH пива[129], при этом температура хранения пива не имеет большого значения[127].
Липиды
Липиды влияют на метаболизм дрожжей и качество пива. Концентрация длинноцепочечных жирных кислот в пиве обычно очень низкая, однако они могут влиять на свойства пива. Мутность сусла во многом связана с наличием жирных кислот. Осветление сусла приводит к снижению содержания жирных кислот, особенно длинноцепочечных и ненасыщенных[130].
В результате разложения линолевая кислота и линоленовая кислота образуют неблагоприятные соединения, связанные со старением пива, особенно при неадекватных условиях хранения пива (например, транс-2-ноненаль)[131]. Эта деградация происходит за счёт ферментативного или автоокисления жирных кислот. Это оказывает большое влияние на образование карбонильных соединений. В ферментативном окислении ненасыщенных жирных кислот участвуют липоксигеназы (LOX), активность которых зависит от температуры сушки солода, условий его хранения и затирания[132].
Липиды отрицательно влияют на стабильность пены. Кроме того, насыщенные жирные кислоты могут способствовать феномену фонтанирования. Однако в ферментационном бульоне липиды, включая длинноцепочечные ненасыщенные жирные кислоты, благоприятно влияют на размножение дрожжей в анаэробных условиях и на процесс ферментации[131].
Когда дрожжи ферментируются, они производят жирные кислоты со средней длиной цепи, такие как капроновая, каприловая и каприновая кислоты. Они являются источником неприятного прогорклого козьего аромата. На их производство влияет штамм дрожжей, исходный экстракт, состав сусла и степень его аэрации. Эти кислоты проявляют синергетический эффект, поэтому их неблагоприятный эффект может проявиться, даже если ни один из них не превышает порог обнаружения[133][134]. Более высокие концентрации этих соединений отмечаются в пиве низового брожения[135].
Вещества, полученные из хмеля
В пивоварении используется женский хмель. Их секреторные железы (лупулин) содержат горькие смолы и эфирные масла, придающие пиву горечь и аромат[136][137]. Ухудшение аромата со временем, а также ухудшение свойств горечи часто является основным фактором, ограничивающим срок годности и сохраняемость пива[138]. Традиционное разделение хмеля различает горький и ароматный хмель[136].
Смолы хмеля содержат α-кислоты и β-кислоты. Наиболее важными для получения горечи являются α-кислоты, составляющие 2—15 % сухого вещества хмеля в зависимости от сорта и условий выращивания. Около 80 % горечи пива обычно приходится на них. Наиболее важными соединениями в группе α-кислот являются гумулон, когумулон, адгумулон, а также прегумулон и постгумулон. Они отличаются строением боковой цепи[138].
α-кислоты должны быть изомеризованы для превращения в соединения, более растворимые в воде[136][139]. При кипячении сусла происходит термическая изомеризация α-кислот в изо-α-кислоты (изогумулон, изокогумулон, изоадгумулон). Затем образуются цис- и транс-изомеры. Однако изомеризуется не более 50 % α-кислот и в пиве остается не более 25 % исходного потенциала горечи[138]. Помимо придания горечи, изо-α-кислоты повышают микробиологическую стабильность пива, проявляя антибактериальные свойства в отношении грамположительных бактерий[140].
При хранении пива доля транс-изо-α-кислот снижается, тогда как цис-изо-α-кислоты остаются стабильными. Чем быстрее происходит разложение, тем выше температура хранения пива. Уровень горечи также со временем снижается и становится более острым, «затяжным». Заменителями изо-α-кислот являются коммерчески доступные экстракты, содержащие восстановленные изо-α-кислоты, обеспечивающие горечь и большую стабильность. Это могут быть дигидро-, тетрагидро- или гексагидроизо-α-кислоты[138].
β-кислоты представляют собой группу соединений, в которую входят лупулон, колупулон, адлупулон, прелупулон и постлупулон. Они плохо растворимы в воде и не подвергаются изомеризации, в отличие от α-кислот. В результате в пиве присутствуют только их следовые концентрации[136].
Вопреки видимому, горький вкус и сладкий вкус в пиве демонстрируют низкую отрицательную корреляцию, что означает, что подслащивание горького пива не снижает восприятие горечи. Интенсивность горького вкуса при этом не меняется, только усиливается впечатление «полноты вкуса»[94].
Хмель содержит 0,5—3 % эфирных масел[136], основными компонентами которых являются терпены и их кислородсодержащие производные[141]. В состав масел входят:
- монотерпены, например лимонен (с запахом лимона), β-мирцен, α-пинен, п-цимол;
- терпеновые спирты, например линалоол (цветочный ароматизатор), гераниол, нерол (розовый ароматизатор), мирценол;
- сесквитерпены, например фарнезен, гумулен, селинен , β-кариофиллен;
- сесквитерпеновые спирты, например неролидол, α-кадинол ;
- альдегиды и кетоны;
- сложные эфиры;
- соединения серы, в том числе тиоэфиры, сульфиды[136].
Большинство эфирных масел очень летучи и мало растворимы в сусле. Их присутствие в пиве зависит от их химических свойств и способа охмеления. Например, после 90 минут варки 85—95 % масел испаряется, а остальное в значительной степени полимеризуется с образованием смол. Многое теряется в результате адсорбции дрожжевыми клетками и фильтрации. В результате лишь немногие из них присутствуют в пиве в неизмененном виде[136]. Для увеличения содержания масла в пиве применяют так называемую «холодное охмеление», то есть добавление хмеля после бурного брожения. Однако следует подчеркнуть, что зависимость между увеличением доз хмеля и содержанием эфирных масел в готовом пиве не является линейной[142].
Соединения серы
Соединения серы, образующиеся в результате метаболической активности дрожжей, могут возникать в результате трансформации серосодержащих органических соединений (серные аминокислоты, витамины) или могут возникать из неорганических компонентов сусла (сульфаты)[143]. Нелетучие соединения серы могут разлагаться и превращаться в более летучие соединения, которые влияют на аромат и качество пива. Бактериальные инфекции также могут быть источником нежелательных соединений серы[144]. Эти ароматы описаны, в частности, как капуста, чеснок, лук, тухлые яйца и подобные запахи[55]. Кроме того, летучие соединения серы обеспечиваются солодом и хмелем[145].
Точный механизм образования многих соединений серы ещё недостаточно изучен[146]. В значительной степени их синтез является результатом ферментативных реакций метаболизма дрожжей, поэтому важен правильный подбор штамма дрожжей[147].
Диоксид серы хорошо растворим в воде и существует химическое равновесие между SO2 · H2O, SO3- и SO32-, которое зависит от рН и температуры. Присутствие этих соединений в пиве может быть результатом экзогенного добавления сульфитов или может быть вызвано метаболизмом дрожжей — они могут восстанавливать сульфаты, присутствующие в окружающей среде[148]. SO2 обладает антиоксидантными и антибактериальными свойствами, что делает его эффективным консервантом. Более того, он может связывать нежелательные карбонильные соединения (например, транс-2-ноненаль), уменьшая их негативное влияние на органолептические свойства пива[149].
Производство обоих сульфитов SO32- и сульфидов S2- зависит от штамма дрожжей, но точные генетические механизмы этих трансформаций неизвестны[150]. Обычно штаммы S. cerevisiae создают 10—30 мг/л сульфитов, но некоторые могут вырабатывать их в концентрациях свыше 100 мг/л[151].
Сероводород является нежелательным побочным продуктом метаболизма дрожжей с очень низким порогом обнаружения, составляющим несколько частей на миллиард. Он придаёт неприятный запах тухлых яиц[152]. Более того, он очень реакционноспособен и участвует в образовании других нежелательных летучих соединений серы[153], поэтому даже следовые количества этого химического соединения могут оказывать существенное влияние на качество пива[154]. У дрожжей S. cerevisiae H2S получается в пути SRS (англ. Sulfate Reduction Sequence)[55]. Является важным метаболическим предшественником биосинтеза цистеина и метионина, активируемым в условиях дефицита этих аминокислот. Сероводород также может образовываться при расщеплении цистеина непосредственно до сульфидов цистеиндесульфгидразой англ. cysteine desulfhydrase)[155] и высвобождаться при автолизе клеток[55]. Концентрация H2S зависит от наличия соединений серы, штамма дрожжей, условий ферментации и наличия питательных веществ в окружающей среде[55][154].
Биосинтез аминокислоты серы поглощает анионы сульфидов. Однако при дефиците азота биосинтез аминокислот подавляется, и анионы сульфидов диффундируют из клеток в виде сероводорода[156]. На интенсивность производства H2S влияет присутствие в окружающей среде усвояемого азота[155] и, в меньшей степени, пантотеновой кислоты[152][157]. Пантотеновая кислота, участвуя в синтезе кофермента А, необходима для синтеза О-ацетилсерина (ОАС) и О-ацетилгомосерина (ОАГ) — соединений, связывающих H2S[55]. Добавление аминного азота снабжает дрожжи легкодоступным источником азота и снижает образование H2S, однако большое количество доступных серных аминокислот может увеличить уровень этого соединения[151][158]. Косвенно факторы, улучшающие физиологическое состояние дрожжей, такие как высокое содержание кислорода и липидов, снижают продукцию H2S. Избыток H2S можно удалить при контакте с медью, с которой это соединение образует нерастворимый сульфид меди (II)[143][151].
Путь SRS инициирует транспорт сульфатов из среды в дрожжевые клетки с помощью сульфатных sulfate permease. Сульфаты восстанавливаются до сульфидов с помощью АТФ-сульфуразы (EC 2.7.7.4) и сульфитредуктазы. Затем О-ацетилсерин (ОАС) и О-ацетилгомосерин (ОАН) связывают образовавшиеся сульфиды, образуя соответственно цистеин и гомоцистеин, которые в дальнейшем могут превращаться в метионин. Фермент, катализирующий реакцию связывания сульфидов О-ацетилсерина и О-ацетилгомосерина, кодируется геном МЕТ17. Инактивация этого гена увеличивает секрецию H2S через дрожжи[153]. Однако сверхэкспрессия этого гена должна значительно снижать количество высвобождаемого H2S, хотя этот эффект наблюдался не у всех штаммов[55][154].
Диметилсульфид (ДМС) — это сульфид, который пахнет приготовленными овощами, особенно приготовленной кукурузой или капустой. Порог обнаружения DMS составляет около 30 мкг/л[159]. Однако иногда его умеренные концентрации (ниже 100 мкг/л) считаются благоприятными[160].
Существует два основных способа получения ДМС в пиве:
- S-метилметионин (СММ) содержится во многих растениях, в том числе при прорастании ячменя, пшеницы и овса он разрушается при воздействии тепла, высвобождая ДМС. Тот же механизм отвечает за высвобождение этого соединения в вареных овощах. Кроме того, некоторые грибы и бактерии продуцируют ферменты, которые специфически гидролизуют сульфоновые соединения до ДМС.
- восстановление диметилсульфоксида (ДМСО) до ДМС микроорганизмами[161].
Прекурсоры ДМС — СММ и ДМСО — получают из солода. Низкому содержанию предшественников ДМС в солоде способствуют низкая степень пропитки, низкая влажность и низкая температура прорастания солода и его меньшая рыхлость[43]. СММ подвергается термическому разложению, поэтому его концентрация ниже, когда для сушки солода используются более высокие температуры. В лагерах, приготовленных из светлых, не интенсивно высушенных солодов, дефект в виде избыточной уловимости ДМС в аромате встречается чаще, чем в других видах пива. ДМС, образующийся при сушке солода, так же, как и выделяющийся при кипячении сусла, испаряется[162]. Однако, если ДМС не полностью удален при сушке или кипячении сусла, или если при осветлении горячего сусла (в водовороте) он был извлечен из СММ, то он будет присутствовать в пиве в свободном состоянии[163]. Некоторые, однако, также будут испаряться вместе с другими газами во время ферментации[162]. Если при производстве солода удаляется недостаточное количество ДМС, его может быть невозможно восполнить при варке, поэтому требуется, чтобы содержание СММ в солоде как предшественнике ДМС не превышало 5 мг/кг[164].
Высвобождающийся летучий ДМС может окисляться до нелетучего ДМСО, который хорошо растворяется в воде и переходит в сусло во время затирания. Некоторые дрожжи и бактерии могут затем превратить его обратно в ДМС[162][163].Обычно дрожжи снижают содержание ДМСО не более чем на 25 % во время ферментации. Образование ДМС из ДМСО зависит от многих факторов, в том числе на штамм дрожжей, температуру брожения (более эффективно при 8 °С, чем при 25 °С), рН (больше образуется при более высоком рН) и состав сусла. Пиво, ферментированное в открытых чанах, в конечном итоге содержит значительно меньше ДМС, чем пиво, ферментированное в закрытых ёмкостях для брожения[161]. Высокие концентрации легкоусвояемого азота поддерживают активность редуктаз ДМСО на низком уровне[165]. Бактериальные инфекции способствуют значительному повышению уровня ДМС[161]. Было высказано предположение, что ферментативное превращение ДМСО в ДМС дрожжами может быть его основным источником в готовом пиве[159].
Хмель является основным источником тиолов в пиве, но большое их количество также образуется при кипячении и брожении сусла. Некоторые связаны в форме цистеиновых конъюгатов, из которых летучие тиолы могут высвобождаться под действием дрожжевой β-лиазы[166][167]. Тип вовлеченных тиолов зависит от сорта хмеля. Может быть, среди прочего 3-сульфанилгексан-1-ол с запахом грейпфрута (например, Cascade, Amarillo, Citra, Mosaic, Saaz), 3-метил-2-бутен-1-тиол (3-МБТ), напоминающий запах выделений желез скунса (Tomahawk, Nelson Sauvin) и 4-метилпентан-2-он-4-тиол (4-метил-4-меркаптопентан-2-он) (4-MMP), который напоминает кошачью мочу или листья чёрной смородины[166][167].
Метантиол можно получить катаболизмом метионина дрожжами[168]. Он имеет очень низкий порог обнаружения и пахнет тухлыми яйцами или капустой[151]. Декарбоксилирование и восстановление метионина приводят к образованию метионола (3-(метилтио)-пропан-1-ол)[168]. Его аромат описывается как луковый, бульонный[169].
Воздействие светового излучения на пиво может привести к фотолизу изо-α-кислот в присутствии рибофлавина и образованию «вонючего» аромата 3-метил-2-бутен-1-тиола (3-МБТ)[170]. Изо-α-кислоты наиболее сильно разлагаются под действием УФ-излучения в диапазоне 280—320 нм или под действием синего света (350—500 нм)[171]. Многие полифенолы могут уменьшить образование этих нежелательных соединений[172], а коричневое стекло бутылки может обеспечить частичную защиту. Однако прозрачное или зелёное стесло бутылки не обеспечивает защиты от их возникновения. Однако, если пиво разливается в такие бутылки, рекомендуется использовать в производстве пива восстановленные изо-α-кислоты, которые не разлагаются на соединения, создающие неприятный аромат, или удалять из пива рибофлавин[170]. Такие действия могут препятствовать образованию 3-МБТ, но всё же под действием света могут образовываться другие неблагоприятные соединения, напоминающие по аромату лук[171], в том числе метионол и 2-метилпропаналь[173].
Тиолы могут как положительно, так и отрицательно влиять на аромат пива; это также зависит от их концентрации[174]. Однако они являются нестабильными ароматическими соединениями в пиве. Они могут очень сильно разлагаться в первый год хранения[167]. К их дополнительным положительным свойствам относятся повышение окислительной стабильности пива и нейтрализация гидроксиэтильного радикала[175].
Примечания
Литература
- Kunze W. Technologia piwa i słodu. — Warszawa, 1999. — ISBN 9783921690499.
- Briggs D. E., Boulton C. A., Brookes P. A., Stevens R. Brewing science and practice. — Cambridge, 2004. — ISBN 1855734907.
- Булгаков Н. И. Биохимия солода и пива. — 2-е изд.. — М.: Пищевая промышленность, 1976. — 358 с.