Фенол
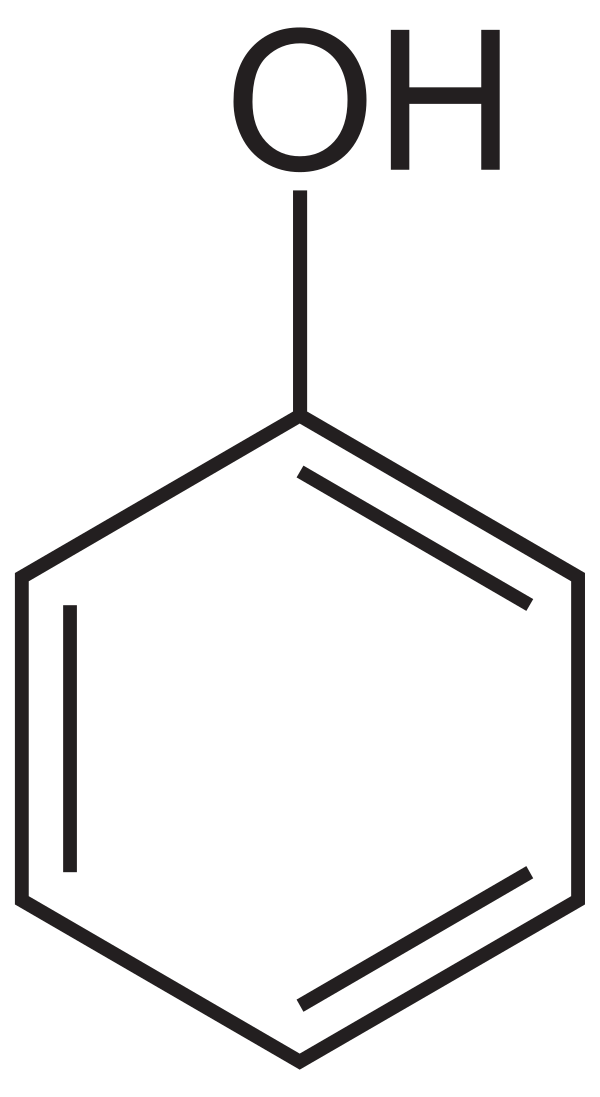
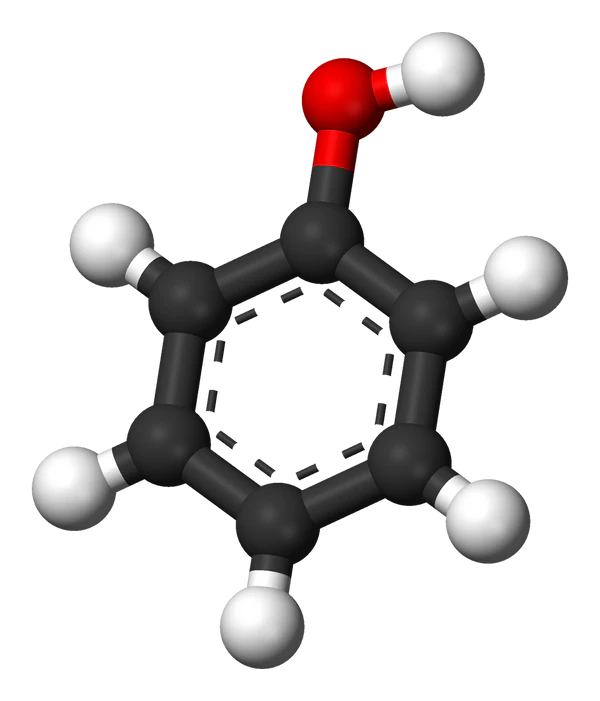
Фено́л (гидро́ксибензо́л, от устар. «карбо́ловая кислота́», химическая формула — C6H6O или C6H5OH) — органическое соединение, возглавляющее класс фенолов.
При стандартных условиях фенол — это бесцветные игольчатые кристаллы, розовеющие на воздухе, с характерным запахом. Токсичен, является сильным ирритантом.
Что важно знать
| Фенол | |
|---|---|
| Общие | |
| Систематическое наименование |
Гидроксибензол |
| Традиционные названия | Фенол, карболовая кислота, карбо́лка, бензоло́л; оксибензо́л |
| Хим. формула | C6H6O |
| Рац. формула | C6H5OH |
| Физические свойства | |
| Состояние | Твёрдое |
| Молярная масса | 94,11 г/моль |
| Плотность | 1,07 г/см³ |
| Энергия ионизации | 8,5 ± 0,1 |
| Термические свойства | |
| Температура | |
| • плавления | 41 °C |
| • кипения | 181,84 °C |
| • вспышки | 79 (в закрытом тигле), 85 (в открытом) °C |
| Пределы взрываемости | 1,8 ± 0,1 |
| Мол. теплоёмк. | 134,7 (кр.) Дж/(моль·К) |
| Энтальпия | |
| • образования | −162,944 кДж/моль |
| Давление пара | 0,4 ± 0,1 |
| Химические свойства | |
| Константа диссоциации кислоты | 9,89 ± 0,01[1] |
| Растворимость | |
| • в воде | 6,5 г/100 мл |
| Структура | |
| Гибридизация | sp2-гибридизация |
| Классификация | |
| Рег. номер CAS | 108-95-2 |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 996 |
| UNII | 339NCG44TV |
| CompTox Dashboard EPA | DTXSID5021124 |
| Рег. номер EINECS | 203-632-7 |
| SMILES | |
| InChI | |
| RTECS | SJ3325000 |
| ChEBI | 15882 |
| Номер ООН | 1671 |
| ChemSpider | 971 |
| ECHA InfoCard | 100.003.303 |
| Безопасность | |
| ЛД50 | 140 мг/кг (морская свинка, внутрижелудочно) |
| Токсичность | Токсичен, весьма едкий, является сильным ирритантом |
| Фразы риска (R) | R23/24/25, R34, R48/20/21/22, R68 |
| Фразы безопасности (S) | S24/25, S26, S28, S36/37/39, S45 |
| Краткие характер. опасности (H) |
H301, H311, H331, H314, H341, H373 |
| Меры предостор. (P) |
P260, P301+P310, P303+P361+P353, P305+P351+P338, P361, P405, P501 |
| Сигнальное слово | опасно |
| Пиктограммы СГС |
|
| NFPA 704 | |
История
Фенол был обнаружен в 1834 году Фридлибом Фердинандом Рунге, который извлёк его (в нечистом виде) из каменноугольной смолы[2]. Рунге назвал фенол «Karbolsäure» (угольно-масляная кислота, карболовая кислота). Каменноугольная смола оставалась основным источником получения фенола до развития нефтехимической промышленности. В 1841 году французский химик Огюст Лоран получил фенол в чистом виде[3].
В 1836 году Огюст Лоран придумал название «фен» для бензола[4], это корень слов «фенол» и «фенил». В 1843 году французский химик Шарль Герхардт придумал название «фенол»[5].
Антисептические свойства фенола использовал сэр Джозеф Листер (1827—1912) в своей пионерской технике антисептической хирургии. Листер решил, что сами раны должны быть тщательно очищены. Затем он покрыл раны кусочком тряпки или ворса[6], покрытого фенолом или «карболовой кислотой», как он её называл. Раздражение кожи, вызванное постоянным воздействием фенола, в конечном итоге привело к внедрению асептических методов в хирургию.
Физические свойства
Представляет собой бесцветные игольчатые кристаллы, розовеющие на воздухе из-за окисления, приводящего к образованию окрашенных веществ (это связано с промежуточным образованием хинонов). Обладает специфическим запахом (таким, как запах гуаши, так как в состав гуаши входит фенол). Умеренно растворим в воде (6 г на 100 г воды), в растворах щелочей, в спирте, в бензоле, в ацетоне. 5%-й раствор в воде — антисептик, широко применявшийся в медицине в прошлом.
Химические свойства
Из-за наличия ароматического кольца и гидроксильной группы фенол проявляет химические свойства, характерные как для спиртов, так и для ароматических углеводородов.
По гидроксильной группе:
- Обладает слабыми кислотными свойствами (более сильными, чем у спиртов), при действии щелочей образует соли — феноляты (например, фенолят натрия — C6H5ONa)[7]:
Фенол — настолько слабая кислота, что даже угольная кислота вытесняет его из фенолятов:
Более интенсивно феноляты разлагаются под действием сильных кислот, например, под действием серной кислоты:
Взаимодействие с металлическим натрием:
Фенол непосредственно не этерифицируется карбоновыми кислотами, эфиры можно получить при взаимодействии фенолятов с ангидридами или галогенангидридами кислот:
Образование простых эфиров. Для получения простых эфиров фенола действуют галогеналканами или галогенпроизводными аренов на феноляты. В первом случае получают смешанные жирно-ароматические простые эфиры:
Во втором случае получают чисто-ароматические простые эфиры:
Реакция проводится в присутствии порошкообразной меди, которая служит катализатором.
При перегонке фенола с цинковой пылью происходит замещение гидроксильной группы водородом[8]:
Фенол вступает в реакции электрофильного замещения по ароматическому кольцу. Гидроксогруппа, являясь одной из самых сильных донорных групп (вследствие уменьшении электронной плотности на функциональной группе), увеличивает реакционную способность кольца к этим реакциям и направляет замещение в орто- и пара-положения[9]. Фенол с лёгкостью алкилируется, ацилируется, галогенируется, нитруется и сульфируется.
Реакция Кольбе — Шмитта служит для синтеза салициловой кислоты и её производных (ацетилсалициловой кислоты и других).
Взаимодействие с бромной водой (качественная реакция на фенол):
Образуется 2,4,6-трибромфенол — твёрдое вещество белого цвета.
Взаимодействие с концентрированной азотной кислотой:
Взаимодействие с хлоридом железа(III) (качественная реакция на фенол[10]):
Реакция присоединения: гидрирование фенола в присутствии металлических катализаторов приводит к образованию циклогексанола и циклогексанона:
Окисление фенола: вследствие наличия гидроксильной группы в молекуле фенола устойчивость к окислению намного ниже, чем у бензола. В зависимости от природы окислителя и условия проведения реакции получаются различные продукты. Так, под действием пероксида водорода в присутствии железного катализатора образуется небольшое количество двухатомного фенола — пирокатехина:
При взаимодействии более сильных окислителей (хромовая смесь, диоксид марганца в кислой среде) образуется пара-хинон.
Получение
В настоящее время производство фенола в промышленном масштабе осуществляется тремя способами:
- кумольный метод. В каскаде барботажных колонн кумол подвергают некаталитическому окислению воздухом с образованием гидропероксида кумола (ГПК). Полученный ГПК, при катализе серной кислотой, разлагают с образованием фенола и ацетона. Кроме того, ценным побочным продуктом этого процесса является α-метилстирол. 95 % всего производимого в мире фенола производят этим методом. Способ был изобретён советскими учёными П. Г. Сергеевым, Н. М. Горнасталевой, Р. Ю. Удрисом, Б. Д. Кружаловым. По сравнению с большинством других процессов, процесс кумола использует относительно мягкие условия синтеза и относительно недорогое сырьё. Однако, чтобы работать экономно, должен быть спрос как на фенол, так и на ацетон[11][12]. В 2010 году мировой спрос на ацетон составлял примерно 6,7 миллиона тонн, 83 процента из которых были удовлетворены ацетоном, полученным кумольным методом;
- окисление толуола, с промежуточным образованием бензойной кислоты (около 3 %);
- выделением из каменноугольной смолы.
Фенол также можно получить восстановлением хинона.
Биологическая роль
Протеиногенная аминокислота тирозин является структурным производным фенола и может быть рассмотрена как пара-замещённый фенол или α-замещённый пара-крезол. В природе распространены и другие фенольные соединения, в том числе полифенолы. В свободном виде фенол встречается у некоторых микроорганизмов и находится в равновесии с тирозином. Равновесие поддерживает фермент тирозин-фенол-лиаза (КФ 4.1.99.2).
Биологическое значение фенола обычно рассматривается в рамках его воздействия на окружающую среду. Фенол — один из промышленных загрязнителей. В чистом виде фенол довольно токсичен для животных и человека. Фенол губителен для многих микроорганизмов, поэтому промышленные сточные воды с высоким содержанием фенола плохо поддаются биологической очистке.
Применение
Мировое производство фенола на 2006 год составляет 8,3 млн т/год. По объёму производства фенол занимает 33-е место среди всех выпускаемых химической промышленностью веществ и 17-е место среди органических веществ. По данным на 2006 год мировое потребление фенола имеет следующую структуру:
- 43 % фенола расходуется на производство бисфенола А, который, в свою очередь, используется для производства поликарбонатов и эпоксидных смол;
- 30 % фенола расходуется на производство фенолформальдегидных смол;
- 12 % фенола гидрированием превращается в циклогексанол, используемый для получения искусственных волокон — нейлона и капрона[13];
- в России большое количество фенола используется в нефтепереработке, в частности, для селективной очистки масел на технологических установках типа 37/1 и А-37/1. Фенол проявляет высокую селективность и эффективность при удалении из масел смолистых веществ, различных полициклических ароматических углеводородов с короткими боковыми цепями, а также соединений, содержащих серу[14];
- остальной фенол расходуется на другие нужды, в том числе на производство антиоксидантов (ионол), неионогенных ПАВ — полиоксиэтилированных алкилфенолов (неонолы), других фенолов (крезолов), лекарственных препаратов (аспирин), антисептиков (ксероформа) и пестицидов. Раствор 1,4 % фенола применяется в медицине, как обезболивающее и антисептическое средство[15].
- в скотоводстве — дезинфекция животных растворами фенола и его производных.
- в косметологии — для проведения глубокого пилинга.Фенол и его производные обусловливают консервирующие свойства коптильного дыма.
Токсические свойства
Фенол — токсичное вещество. По степени воздействия на человеческий организм фенол относится к высокоопасным веществам (Класс опасности 2). При вдыхании вызывает нарушение функций нервной системы. Пыль, пары и раствор фенола раздражают слизистые оболочки глаз, дыхательных путей, кожу, вызывая химические ожоги. Доказательства канцерогенности фенола для людей отсутствуют[16].
Предельно допустимые концентрации (ПДК) фенола[17][18] [19][20]:
- ПДКр.з. = 1 мг/м³ (2 класс опасности)
- ПДКр.с. = 0,3 мг/м³ (2 класс опасности)
- ПДКм.р. = 0,01 мг/м³
- ПДКс.с. = 0,006 мг/м³
- ПДКв. = 0,001 мг/л.
Попадая на кожу, фенол очень быстро всасывается даже через неповреждённые участки и уже через несколько минут начинает воздействовать на ткани головного мозга. Сначала возникает кратковременное возбуждение, а потом — паралич дыхательного центра. Даже при воздействии минимальных доз фенола наблюдается чихание, кашель, головная боль, головокружение, бледность, тошнота, упадок сил. Тяжёлые случаи отравления характеризуются бессознательным состоянием, синюшностью, затруднением дыхания, нечувствительностью роговицы, скорым, едва ощутимым пульсом, холодным потом, нередко судорогами. Смертельная доза для человека при попадании внутрь — 1—10 г, для детей — 0,05—0,5 г[21].
ПДК в воздухе рабочей зоны — 1 мг/м³ (максимально-разовая) и 0,3 мг/м³ (среднесменная). Порог восприятия запаха фенола у разных людей разный; и он может достигать (среднее значение в группе) 5,8-7,5 мг/м³[22]. А у отдельных работников он может быть значительно больше среднего значения. По этой причине можно ожидать, что использование широко распространённых фильтрующих СИЗОД в сочетании с «заменой фильтров по появлении запаха под маской» (как это почти всегда рекомендуется в РФ поставщиками) приведёт к чрезмерному воздействию паров фенола на, по крайней мере, часть работников, и причинить вред их здоровью[23] — из-за запоздалой замены противогазных фильтров. Для защиты от фенола следует использовать более эффективные изменение технологии и средства коллективной защиты.
Наглядным примером воздействия фенола на окружающую среду стал случай весной 1990 года в Уфе. В результате техногенной аварии на предприятии ПО «Уфахимпром» произошла утечка большого количества фенола в речку Шугуровка, впадающую в более крупную реку Уфу, являющуюся источником хозяйственно-питьевого водоснабжения города Уфы. Загрязнение воды в районе Южного водозабора превышало ПДК более чем в 100 раз. Опасность загрязнения питьевой воды фенолом проявляется в том, что при очистке вод использовался хлор, который, взаимодействуя с фенолом, образовывал хлорпроизводные (смесь хлорфенолов) — более токсичные вещества (некоторые в 100—250 раз превышают токсичность самого фенола). Население Уфы было оповещено об опасности употребления водопроводной воды для питья. Общая численность населения, потреблявшего питьевую воду, загрязнённую фенолом из Южного водозабора Уфы, составила 672 876 человек[24].
Примечания














![{\displaystyle {\mathsf {C_{6}H_{5}ONa+C_{6}H_{5}Cl{\xrightarrow[{}]{Cu}}C_{6}H_{5}OC_{6}H_{5}+NaCl}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/6bc5440e942ad1032d9bac43b770cdead2e43681)

![{\displaystyle {\mathsf {C_{6}H_{5}OH+CO_{2}{\xrightarrow[{}]{NaOH}}C_{6}H_{4}OH(COONa)}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/8746d83f76859c5bf80d5bc833151804dc210186)



![{\displaystyle {\mathsf {6C_{6}H_{5}OH+FeCl_{3}\rightarrow H_{3}[Fe(C_{6}H_{5}O)_{6}]+3HCl}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/298928dbc2a7b0fca344f5d84657a2595c0b18e1)

![{\displaystyle {\mathsf {C_{6}H_{5}OH+2H_{2}O_{2}{\xrightarrow[{-H_{2}O}]{kat:Fe}}C_{6}H_{4}(OH)_{2}}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/a3412295398fa56c30b01ef5f9cc5de7c91fdae7)