Серповидноклеточная анемия
Серповиднокле́точная анеми́я (СКА; дрепаноцито́з) — анемия из группы генетических заболеваний, при которых эритроциты меняют свою форму с дисковидной на серповидную. В основе болезни лежит специфическая мутация в гене HBB, кодирующем бета-цепь гемоглобина, что приводит к синтезу аномального гемоглобина S (HbS) и его полимеризации в условиях гипоксии. Заболевание характеризуется снижением концентрации гемоглобина в крови, болевыми кризами, частыми инсультами, а также патологией лёгких и почек. Продолжительность жизни пациентов в развитых странах примерно на 20 лет ниже средней[2].
Общие сведения
История
Первое описание клинической картины СКА датируется 1670 годом и было сделано на примере африканской семьи. В 1910 году американские исследователи Джеймс Херрик и Эрнест Айронс наблюдали случай гемолитической анемии с характерными серповидными эритроцитами у темнокожего студента из Гренады. В 1949 году Линус Полинг с коллегами установил связь заболевания с патологической формой гемоглобина. В 1957 году Вернон Инграм описал молекулярный дефект болезни — замену глутамина на валин в шестой позиции бета-глобина. Первая пересадка костного мозга пациенту с этим диагнозом была проведена в 1984 году. С 1998 года в США для терапии заболевания было разрешено рутинное применение гидроксимочевины, а с 2014 года начались клинические исследования методов генетической коррекции[2].
Классификация
СКА представляет собой одну из форм серповидно-клеточной болезни — группы патологических состояний, вызванных мутациями в гене бета-глобина, которые изменяют физико-химические свойства гемоглобина[3].
Этиология
СКА связана с мутацией в гене HBB, который расположен на коротком плече одиннадцатой хромосомы. Мутация в шестом кодоне первого экзона этого гена приводит к замене аминокислоты глутамина на валин, из-за чего снижается растворимость дезоксигенированной формы гемоглобина S. Для развития болезни необходимо наличие мутаций в обеих копиях гена HBB (гомозиготное носительство). Заболевание наследуется по аутосомно-рецессивному типу[2][4].
Патогенез
Патогенез СКА характеризуется двумя основными компонентами: гемолизом и вазоокклюзивными кризами. Дефект в гене бета-глобина делает молекулу серповидного гемоглобина S склонной к превращению в ригидные удлинённые полимеры в дезоксигенированном состоянии. Изначально процесс серповидного превращения является циклическим, и эритроциты осциллируют между нормальной двояковогнутой формой и аномальной серповидной формой, которая приобретается в условиях низкого давления кислорода. Однако со временем изменения становятся необратимыми, и эритроциты приобретают постоянную серповидную форму, что повышает риск гемолиза и вазоокклюзивных кризов. Множественные факторы, присущие серповидным эритроцитам, такие как низкое сродство гемоглобина S к кислороду, физиологически высокая активность 2,3-дифосфоглицерата и повышенная активность сфингокиназы-1, приводят к дезоксигенации, способствующей полимеризации гемоглобина S. Кроме того, высокая концентрация гемоглобина S, аномальная активность ионных каналов, ведущая к обезвоживанию клетки, и повторяющиеся повреждения мембраны эритроцитов также увеличивают риск полимеризации[5].
Окислительный стресс способствует гемолизу за счёт аутоокисления гемоглобина S, что приводит к повреждению клеточной мембраны эритроцитов. Повышенная экспрессия ксантиндегидрогеназы и ксантиноксидазы при сниженной экспрессии НАДФН-оксидазы усиливает окислительный стресс внутри серповидных эритроцитов. Гемолизированная клетка высвобождает свободный гемоглобин, который связывает оксид азота, и аргиназу-1, которая конкурирует за L-аргинин, что препятствует действию и образованию оксида азота и способствует окислительному стрессу и сосудистому ремоделированию[5].
Помимо полимеризации гемоглобина S и внутрисосудистого гемолиза, несколько других факторов также способствуют вазоокклюзии. Например, серповидные эритроциты экспрессируют на своей поверхности различные молекулы адгезии, а свободный гем, гемоглобин, активные формы кислорода и эндотелий взаимодействуют друг с другом, а также с нейтрофилами и тромбоцитами, способствуя развитию вазоокклюзии и тромбоза[5].
Эпидемиология
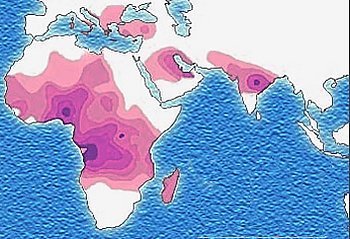
Распространённость серповидноклеточной анемии в мире довольно высока: общее число больных превышает четыре миллиона человек, из которых не менее ста тысяч проживают в США. Более семидесяти пяти процентов всех случаев заболевания диагностируется в регионах Африки к югу от Сахары, особенно в Нигерии и Гане. В мире с этой болезнью рождается один из трёхсот шестидесяти пяти детей африканского происхождения. Высокая заболеваемость также отмечается в Индии, Саудовской Аравии и странах Средиземноморья. На территории СНГ серповидноклеточная анемия наиболее часто встречается у жителей Азербайджана и Республики Дагестан в составе Российской Федерации[2][3].
Диагностика
СКА обычно манифестирует в раннем детстве, поскольку в первые полгода жизни дети защищены высоким уровнем фетального гемоглобина. Основным клиническим проявлением является вазоокклюзивный криз, возникающий при закупорке микроциркуляторного русла серповидными эритроцитами. Болевые кризы начинаются внезапно и могут продолжаться от нескольких часов до нескольких дней. Боль способна поражать любые участки тела, включая живот, кости, суставы и мягкие ткани. У детей раннего возраста часто встречается дактилит с болезненным отёком кистей и стоп. По мере взросления боль смещается в длинные кости конечностей, а в подростковом возрасте — в тела позвонков, особенно поясничной области. Провоцирующими факторами кризов выступают гипоксия, обезвоживание, лихорадка и переохлаждение. Многие пациенты также испытывают хроническую боль низкой интенсивности в костях и суставах[3][6].
Вследствие повреждения селезёнки развивается функциональная аспления, что обусловливает крайнюю восприимчивость к инфекциям, особенно вызванным пневмококком. Остеомиелит, вызываемый стафилококками и сальмонеллами, часто возникает в участках костей, ослабленных инфарктами. Одним из наиболее тяжёлых проявлений служит поражение центральной нервной системы в виде ишемического инсульта у детей или геморрагического у взрослых, что приводит к стойким неврологическим нарушениям. Также могут возникать когнитивные нарушения при бессимптомных инфарктах мозга. Со стороны сердца вследствие хронической анемии и микроинфарктов развивается дилатация всех камер. Хронический гемолиз приводит к образованию камней в жёлчном пузыре. Почки теряют способность концентрировать мочу, что усугубляет обезвоживание, возможно развитие почечной недостаточности. Характерны трофические язвы голеней в области лодыжек, плохо поддающиеся заживлению. Приапизм представляет собой частую проблему у мужчин, приводящую к фиброзу и эректильной дисфункции. Асептический некроз головки бедренной кости развивается у трети пациентов к тридцати годам, вызывая тяжёлый болевой синдром[3][6].
Клинический анализ крови: характерно снижение концентрации гемоглобина до 50-90 г/л и гематокрита до 17-29 %. Отмечается повышение общего количества лейкоцитов до 12-20 тысяч/мкл с преобладанием нейтрофилов, а также увеличение числа тромбоцитов. Скорость оседания эритроцитов часто снижена. Количество ретикулоцитов обычно повышено, однако этот показатель может варьировать в зависимости от степени исходного гемолиза[3][6].
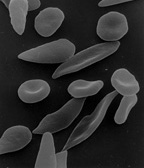
Микроскопия мазка крови: в мазке периферической крови пациентов с СКА обнаруживаются вытянутые эритроциты с заострёнными концами, имеющие характерную серповидную форму. У части пациентов также присутствуют дополнительные находки. К ним относятся тельца Жолли, представляющие собой остатки дезоксирибонуклеиновой кислоты внутри эритроцитов, что обычно наблюдается у лиц с удалённой селезёнкой и отражает аутоинфаркт селезёнки, характерный для этого заболевания. Также могут выявляться клетки-мишени, которые чаще встречаются при талассемии, но нередко наблюдаются при СКА, особенно при сочетании с талассемией. Присутствие полихроматофильных клеток, являющихся ретикулоцитами, свидетельствует об ответной реакции костного мозга на гемолиз. В некоторых случаях в мазке периферической крови также можно обнаружить ядерные эритроциты[5].
Биохимический анализ крови: характерно повышение активности лактатдегидрогеназы[3][6].
Клинический анализ мочи: у пациентов с СКА часто наблюдаются гематурия и изостенурия[6].
Молекулярно-генетический анализ крови методом секвенирования: позволяет выявить мутацию в гене HBB[3].
Рентгенография костей скелета: при раннем дактилите на снимках виден только отёк мягких тканей, а периостальное новообразование кости появляется через 7-10 дней. Остеонекроз становится видимым на рентгенограммах лишь на поздних стадиях, после значительного повреждения кости. Расширение костномозгового канала, истончение коркового слоя, резорбция трабекул и очаговые просветления могут обнаруживаться через 2-3 недели после начала симптомов, но обычно исчезают в течение нескольких недель. В первые 1-2 недели рентгенография менее чувствительна для диагностики остеомиелита по сравнению с другими методами, однако впоследствии на снимках появляются кортикальная деструкция, периостальная реакция, а со временем могут формироваться свищевые ходы и секвестры[6].
Магнитно-резонансная томография позволяет выявить аваскулярный некроз головок бедренной и плечевой костей, отличить остеомиелит от костного инфаркта, а также обнаружить ранние признаки остеонекроза. Метод даёт возможность диагностировать острые и хронические инфаркты костного мозга, его гиперплазию, остеомиелит, остеонекроз, костные секвестры, свищевые ходы и поднадкостничные абсцессы. Ключевым диагностическим признаком остеомиелита служит кортикальная деструкция. У детей с СКА томография выявляет немые инфаркты головного мозга[6].
Транскраниальная допплерография позволяет выявить детей с СКА, имеющих высокий риск инсульта, путём регистрации аномально высокой скорости кровотока в крупных артериях виллизиева круга, а именно в средней мозговой или внутренней сонной артериях. Скорость кровотока, обычно повышенная вследствие тяжёлой анемии, становится локально увеличенной при стенозе, уменьшающем диаметр артерии[3][6].
Ультразвуковое исследование брюшной полости у пациентов с болями в животе применяется для исключения холецистита, жёлчнокаменной болезни или внематочной беременности, а также для измерения размеров селезёнки и печени. Этот метод позволяет визуализировать камни в жёлчных протоках и выявить признаки утолщения стенок жёлчного пузыря или воспаления протоков, указывающие на возможный холецистит[6].
Дифференциальная диагностика
Дифференциальная диагностика СКА проводится со следующими заболеваниями[5]:
- талассемия;
- аутоиммунная гемолитическая анемия (как тепловыми, так и холодовыми антителами);
- пароксизмальная ночная гемоглобинурия;
- дефекты мембраны эритроцитов (наследственный сфероцитоз, наследственный эллиптоцитоз);
- ферментные дефекты (дефицит пируваткиназы, дефицит глюкозо-6-фосфатдегидрогеназы);
- лекарственно-индуцированный гемолиз;
- гемолиз, связанный с трансфузией (острая или отсроченная гемолитическая реакция);
- микроангиопатическая гемолитическая анемия (атипичный или типичный гемолитико-уремический синдром, тромботическая тромбоцитопеническая пурпура);
- инфекционные причины (малярия, бабезиоз, риккетсии, клостридии, бартонелла);
- гемолиз, вызванный васкулитом.
Осложнения
К острым осложнениям СКА относятся[5]:
- острый грудной синдром;
- секвестрационные кризы (селезёночная или печёночная секвестрация);
- жировая эмболия;
- инфаркт или некроз кости;
- коагулопатия, повышающая риск артериальных и венозных тромбозов (инсульт, инфаркт миокарда, венозные тромбозы);
- офтальмологические осложнения (кровоизлияние в стекловидное тело, отслойка сетчатки, окклюзия артерии или вены сетчатки);
- апластические кризы, связанные с парвовирусной инфекцией;
- папиллярный некроз почек.
К хроническим осложнениям СКА относятся[5]:
- задержка роста и развития;
- кардиальные осложнения (кардиомегалия, кардиомиопатия, гипертрофия левого желудочка, аритмия, застойная сердечная недостаточность);
- лёгочные осложнения (отёк лёгких, серповидноклеточная болезнь лёгких, лёгочная гипертензия);
- гепатобилиарные осложнения (увеличение печени, внутрипечёночный холестаз, жёлчнокаменная болезнь, вирусные гепатиты);
- осложнения со стороны селезёнки (увеличение селезёнки, гипоспленизм, отсутствие функции селезёнки);
- почечные осложнения (острая и хроническая почечная недостаточность, пиелонефрит, медуллярная карцинома почки);
- костно-мышечные осложнения (дегенеративные изменения, остеомиелит, септический артрит, остеонекроз, остеопения и остеопороз);
- офтальмологические осложнения (пролиферативная ретинопатия, кровоизлияние в стекловидное тело, отслойка сетчатки, непролиферативные изменения сетчатки);
- эндокринные осложнения (первичный гипогонадизм, гипопитуитаризм, гипоталамическая недостаточность);
- перегрузка железом вследствие повторных трансфузий и хронического гемолиза.
Лечение
Лечение СКА включает медикаментозную терапию, трансфузии, трансплантацию и хирургические вмешательства. Пациентам с тяжёлыми болевыми кризами назначают препараты, стимулирующие синтез фетального гемоглобина. Трансфузии эритроцитов применяют при жизнеугрожающих состояниях. Для профилактики осложнений переливают кровь, совместимую по основным антигенам. При перегрузке железом назначают препараты, связывающие избыток железа, с регулярным контролем его уровня и функции органов. Трансплантация костного мозга рекомендуется молодым пациентам с тяжёлыми осложнениями при наличии совместимого родственного донора. Процедура противопоказана при тяжёлых органных нарушениях, инфекциях и некоторых других состояниях. Хирургические вмешательства проводят с учётом повышенных рисков. Наиболее частые операции — холецистэктомия, спленэктомия, тонзилэктомия, эндопротезирование суставов[3].
Прогноз
Прогноз при СКА зависит от множества факторов. По данным исследований прошлых лет, средняя продолжительность жизни женщин составляла 42 года, мужчин — 48 лет. К факторам, повышающим риск ранней смерти, относятся острый грудной синдром, почечная недостаточность, судороги, большое количество лейкоцитов и низкая концентрация фетального гемоглобина. Более современные исследования показывают, что на выживаемость также влияют повышенная скорость кровотока в сердце по данным эхокардиографии, лёгочная гипертензия, наличие астмы, терминальная почечная недостаточность, требующая диализа, и выраженность гемолиза[5].
Диспансерное наблюдение
Диспансерное наблюдение пациентов с СКА осуществляется пожизненно под руководством врача-гематолога и педиатра или терапевта с привлечением других специалистов по показаниям. Кратность осмотров зависит от проводимой терапии: в период подбора лечения визиты более частые, при стабильном течении — один раз в три месяца. Регулярные осмотры офтальмолога, кардиолога, невролога и эндокринолога проводятся не реже одного раза в год[3].
Инструментальное обследование включает ежегодное дуплексное сканирование сосудов головного мозга, электрокардиографию, эхокардиографию, суточное мониторирование артериального давления, ультразвуковое исследование органов брюшной полости и почек. При выявлении отклонений частота исследований увеличивается. При перегрузке железом дополнительно проводятся магнитно-резонансная томография для оценки накопления железа в органах и эластометрия печени. Лабораторный контроль включает клинический анализ крови: на фоне стимуляции фетального гемоглобина каждые три месяца, на фоне трансфузий — ежемесячно. Биохимический анализ крови проводится с периодичностью от трёх до двенадцати месяцев в зависимости от терапии. При трансфузиях обязателен контроль антиэритроцитарных антител перед каждым переливанием. Ежегодно оценивается гормональный профиль[3].
Профилактика
Профилактика включает агрессивное лечение лихорадки с немедленным назначением антибиотиков, санацию очагов инфекции, коррекцию дефицита витаминов. При приапизме проводят профилактику повторных эпизодов и обучают пациентов своевременному обращению за помощью. Профилактика поражения центральной нервной системы при СКА направлена на предотвращение ишемических инсультов. При повышении скорости кровотока по средней мозговой артерии выше критического уровня назначаются регулярные трансфузии эритроцитной массы для снижения доли аномального гемоглобина, что значительно уменьшает риск развития инсульта. При выявлении гиперкоагуляции применяются антикоагулянты для профилактики тромбозов. Пациентам, перенёсшим инсульт, рекомендуется трансплантация гемопоэтических стволовых клеток для предотвращения повторных атак. У взрослых с транзиторными ишемическими атаками проводится вторичная профилактика антитромбоцитарными препаратами или антикоагулянтами, а также могут использоваться хронические трансфузии эритроцитов. Повышение уровня гомоцистеина корректируется препаратами фолиевой кислоты[3].
Вакцинопрофилактика проводится по расширенному графику, включающему обязательную вакцинацию против пневмококковой, менингококковой инфекции, гемофильной палочки, гепатита В, гриппа и COVID-19. Детям раннего возраста показана длительная профилактика пенициллинами[3].
Примечания
Литература
- Sundd P., Gladwin M. T., Novelli E. M. Pathophysiology of Sickle Cell Disease (англ.) // Annual Review of Pathology: Mechanisms of Disease. — 2019. — 24 January (vol. 14). — P. 263—292. — doi:10.1146/annurev-pathmechdis-012418-012838.
- Российское общество детских онкологов и гематологов, Национальное гематологическое общество, Федерация лабораторной медицины". Серповидно-клеточные нарушения (неопр.). Рубрикатор клинический рекомендаций. Министерство Здравоохранения Российской Федерации (26 ноября 2024).