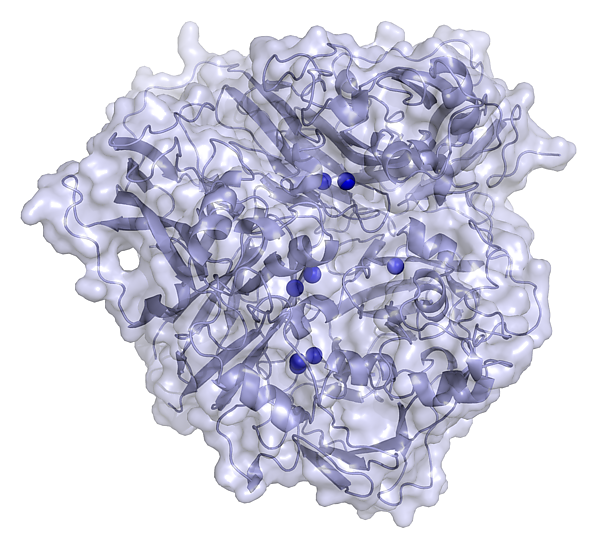
Церулоплазмин
Церулоплазмин — медь-содержащий белок (металлопротеин), присутствующий в плазме крови. В церулоплазмине содержится около 95 % общего количества меди сыворотки крови человека. Врожденный дефицит церулоплазмина приводит к дефектам развития головного мозга и печени. Был описан в 1948 году[5].
Общие сведения
| Церулоплазмин | |||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||||||||||||||||||||||||||||||
| Идентификаторы | |||||||||||||||||||||||||||||||||||||||||||||||
| Псевдонимы | CP, CP-2, ceruloplasmin (ferroxidase), Ceruloplasmin, AB073614 | ||||||||||||||||||||||||||||||||||||||||||||||
| Внешние ID | OMIM: 117700 MGI: 88476 HomoloGene: 75 GeneCards: CP | ||||||||||||||||||||||||||||||||||||||||||||||
| Шифр КФ | 1.16.3.1 | ||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||
Физические свойства церулоплазмина человека
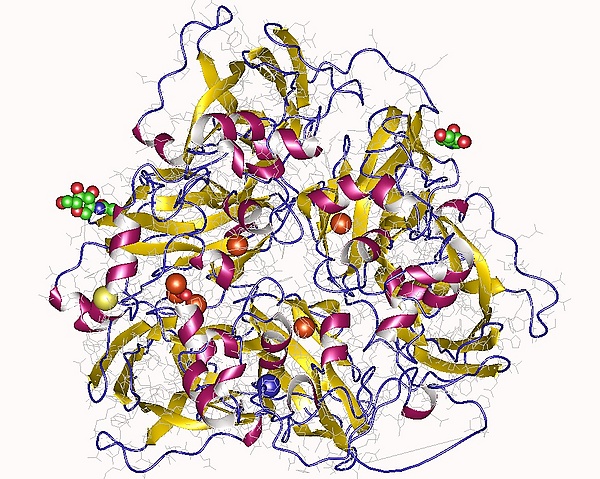
Церулоплазмин человека, благодаря входящим в его состав ионам меди, имеет голубой цвет. Средняя молекулярная масса колеблется в диапазоне 150 000—160 000 г/моль[6]. На одну молекулу приходится 6-7 ионов меди (Cu+2).
До внедрения меди в белок он называется апоцерулоплазмин, после — холоцерулоплазмин.
Показано, что ген церулоплазмина человека подвергается альтернативному сплайсингу[7].
Основные аминокислоты церулоплазмина: аспарагиновая, глутаминовая, треонин, глицин, лейцин.
Физиологическая роль
Церулоплазмин обнаруживается не только в плазме человека и приматов, но и у свиньи, лошади, козы, оленя, собаки, кошки и др. животных. Белок играет важную ферментативную роль — он катализирует окисление полифенолов и полиаминов в плазме[6].
Синтез церулоплазмина в печени осуществляют гепатоциты и скорость этого процесса регулируется гормонами. На протяжении всей жизни уровень этого белка в плазме остается стабильным, за исключением неонатального этапа и периода беременности у женщин.
Церулоплазмин не проникает либо слабо проникает через гематоэнцефалический барьер. В мозге человека белок производится определёнными популяциями глиальных клеток, связанных с микрососудами, а в сетчатке глаза — клетками внутреннего нуклеарного слоя[8]. Астроцитами синтезируется особая форма церулоплазмина[9], порождённая альтернативным сплайсингом и содержащая GPI-якорь, она предположительно необходима для выведения железа из клеток ЦНС[10].
Клиническое значение
Пониженный уровень церулоплазмина отмечаются при болезни Вильсона — Коновалова и болезни Менкеса. В первом случае это обусловлено нарушением процесса «нагрузки» апоцерулоплазмина медью вследствие мутации гена ATP7B. Во втором случае нарушен захват меди в кишечнике из-за мутаций гена ATP7A.
Концентрация церулоплазмина также возрастает при воспалительных процессах, травмах.
В ряде исследований отмечаются повышенные уровни церулоплазмина у больных шизофренией[11]. В единственном на данный момент небольшом исследовании лиц с обсессивно-компульсивным расстройством также были отмечены повышенные уровни церулоплазмина[12].
Исследования на животных
У мышей, нокаутных по церулоплазмину, отмечается отложение железа в мозжечке и стволе мозга, потеря дофаминергических нейронов, нарушение двигательной координации[13].
Примечания
Ссылки
- Церулоплазмин — институт экспериментальной медицины, Санкт-Петербург
- Церулоплазмин — от метаболита до лекарственного средства — В. И. Ващенко, Т. Н. Ващенко, 2006, «Психофармакология и биологическая наркология»