Синдром Пламмера — Винсона
Синдро́м Пла́ммера — Ви́нсона (СПВ; синдро́м Па́терсона — Ке́лли, синдро́м Па́терсона — Бра́ун-Ке́лли, сидеропени́ческая дисфаги́я) — редкое клиническое состояние, характеризующееся триадой признаков: дисфагией, железодефицитной анемией и стриктурой пищевода[1].
Общие сведения
История
СПВ назван в честь Генри Стэнли Пламмера (1874—1936) и Портера Пейсли Винсона (1890—1959), врачей клиники Мэйо. В 1912 году Пламмер описал серию клинических случаев длительной железодефицитной анемиии в сочетании дисфагией и спазмом верхнего отдела пищевода без анатомического стеноза. В 1919 году Винсон сообщил о другом случае «ангуляции» пищевода и приписал первое описание этой сущности более раннему отчёту Пламмера. Несколько лет спустя он опубликовал серию клинических случаев дисфагии, в которых больные были вылечены бужированием, при этом большинство пациентов были женщинами[2].
Другое название — синдром Патерсона — Келли, данное в честь Дональда Росса Патерсона (1863—1939) и Адама Брауна-Келли (1865—1941), британских ларингологов, которые опубликовали свои находки независимо друг от друга в 1919 году. Они были первыми, кто описал характерные клинические особенности синдрома. Патерсон дал наиболее полное описание, но без указания на анемию. Он также первым обратил внимание на связь с раком пищевода. Браун-Келли не только описал признаки и симптомы состояния, но и рассмотрел роль анемии[2].
Этиология
Этиология СПВ остаётся неизвестной. Предполагаемые этиологические факторы включают алиментарные и железодефицитные состояния, генетическую предрасположенность и аутоиммунные процессы. Доказательства в пользу этих предполагаемых механизмов остаются слабыми, за исключением дефицита железа, который неизменно играет важную роль[3].
Поскольку пациенты с СПВ могут также страдать от недостаточности питания, в качестве возможной причины предполагался и дефицит витаминов группы B, однако доказательства этого слабы. С синдромом также ассоциируются такие заболевания, как целиакия, болезнь Крона, ревматоидный артрит и патология щитовидной железы, что позволяет предположить вовлечение иммунной дисрегуляции в его патогенез[3].
Патогенез
Точный патогенез СПВ и формирования стриктуры пищевода до конца не изучен. Выдвигается предположение, что дефицит железа вызывает дисфункцию железозависимых ферментов, что приводит к окислительному стрессу и повреждению ДНК. Нарушение работы железозависимых окислительных ферментов вызывает миастенические изменения в мышцах, ответственных за глотание, атрофию слизистой оболочки пищевода и формирование мембран как осложнение со стороны эпителия. Также повторяющееся повреждение эпителия из-за дефицита железа приводит к атрофии слизистой и дегенерации глоточных мышц, что приводит к развитию пищеводных перепонок. Сама перепонка локализуется ниже перстневидно-глоточной мышцы и асимметрично прикреплена к передней стенке пищевода. Она представляет собой тонкую слизистую мембрану, состоящую из многослойного плоского эпителия[3].
Предполагается, что воспаление и атрофия слизистой оболочки, особенно в области перстневидного хряща (посткрикоидная область), играют роль в патогенезе синдрома. Именно эта область испытывает максимальную травму при проглатывании твёрдого пищевого комка, что повышает риск формирования перепонки[3].
Существует альтернативное объяснение образования перепонок, согласно которому у некоторых пациентов может присутствовать эктопия слизистой оболочки желудка в верхней части пищевода. Секреция соляной кислоты этим участком предположительно вызывает локальное воспаление и последующее формирование стриктуры. Однако данная гипотеза имеет существенное слабое место: она не может объяснить, почему перепонки не образуются в нижнем отделе пищевода. Этот вопрос остаётся открытым, особенно учитывая тот факт, что слизистая оболочка именно нижней трети пищевода подвергается гораздо более частому и интенсивному воздействию соляной кислоты при желудочном рефлюксе[4].
При гистологическом исследовании перепонки у пациентов с СПВ демонстрируют фиброз, атрофию эпителия, гиперплазию эпителия, гиперкератоз, гиперплазию базальных клеток и некоторые признаки хронического воспаления[3].
Эпидемиология
Точные данные о распространённости СПВ до сих пор отсутствуют. В медицинской литературе это состояние описывается преимущественно в виде единичных клинических случаев. В первой половине XX века считалось, что данное заболевание наиболее характерно для представителей белой расы, проживающих в северных странах. До 90 % всех заболевших составляли женщины, преимущественно в возрасте от 40 до 70 лет[5].
Диагностика
Ключевыми клиническими проявлениями СПВ являются триада симптомов: дисфагия с локализацией в области перстневидного хряща, наличие мембранозных стриктур в верхнем отделе пищевода и железодефицитная анемия. Дисфагия обычно носит безболезненный, но прогрессирующий характер, развиваясь в течение нескольких лет. Она проявляется как затруднение при проглатывании твёрдой пищи, что нередко приводит к вынужденным диетическим ограничениям и потере массы тела. В клинической картине часто доминируют симптомы, связанные с анемическим синдромом: выраженная слабость, бледность кожных покровов, повышенная утомляемость и тахикардия. К характерным признакам также относятся воспаление языка (глоссит), ангулярный хейлит (заеды в углах рта) и койлонихия — специфическая деформация ногтевых пластин в виде «ложек». В некоторых случаях к проявлениям синдрома могут присоединяться спленомегалия и увеличение объёма щитовидной железы[5].
- Эзофагогастродуоденоскопия: определяются гладкие, тонкие, сероватого цвета стриктуры. Они имеют эксцентрично или центрально расположенное входное отверстие. Типичной локализацией таких стриктур являются проксимальные отделы пищевода. Важной характеристикой является их хрупкость: эти мембранозные структуры могут быть случайно пропущены или разорваны во время процедуры, если эндоскоп не проводится под тщательным визуальным контролем[5].
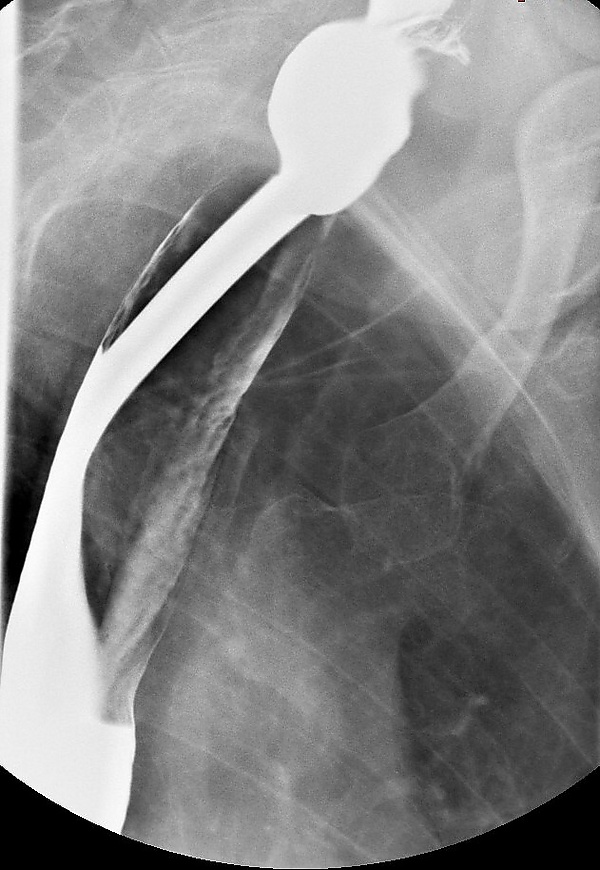
- Рентгенография пищевода с пероральным контрастированием: позволяет оценить акт глотания в процессе продвижения бариевой взвеси из полости рта в пищевод, выявить даже незначительные перепонки, а также дифференцировать истинные и ложные стриктуры[3][5].
- Клинический анализ крови: характерна анемия, снижение количества эритроцитов и гематокрита[4][5].
- Биохимический анализ крови: характерны повышение общей железосвязывающей способности, снижение концентрации ферритина, снижение концентрации сывороточного железа[4][5].
Дифференциальная диагностика
В перечень заболеваний для дифференциальной диагностики СПВ входят рак пищевода, дивертикулы пищевода, нервно-мышечные заболевания пищевода (ахалазия кардии, кардиоспазм и диффузный эзофагоспазм), склеродермия, пептические и ожоговые стриктуры, грыжа пищеводного отверстия диафрагмы и объёмные образования средостения, сдавливающие пищевод[5].
Осложнения
Лечение
Терапия СПВ представляет собой комплексный подход, направленный на решение трёх ключевых задач: устранение первопричины железодефицитного состояния, восполнение дефицита железа в организме и механическое устранение препятствия в пищеводе[4].
Основой лечения является длительная терапия препаратами железа, позволяющая нормализовать показатели гемоглобина и восполнить тканевые запасы железа. Важно отметить, что уже само по себе восстановление концентрации железа часто приводит к значительному улучшению акта глотания и уменьшению выраженности дисфагии[4].
При сохранении симптомов на фоне медикаментозной терапии применяются современные эндоскопические методики механического воздействия на пищеводную перепонку. Арсенал вмешательств включает баллонную дилатацию, при которой суженный участок расширяют под контролем зрения с помощью специального баллона; бужирование ригидными или гибкими дилататорами системы Савари — Жильяра для постепенного увеличения просвета пищевода; а также эндоскопическое рассечение стриктуры с использованием лазерной вапоризации или электрокоагуляционной диссекции[4].
Прогноз
Прогноз для пациентов с СПВ в целом благоприятный. В большинстве случаев для полного устранения симптомов достаточно всего одной процедуры — эзофагогастродуоденоскопии с одновременным бужированием пищевода в сочетании с курсом заместительной терапии препаратами железа. Однако в долгосрочной перспективе сохраняется повышенный риск развития плоскоклеточного рака глотки или верхнего отдела пищевода[3].
Диспансерное наблюдение
Не разработано.
Профилактика
Не разработана.
Примечания
Литература
- Саенко А. А., Долгушина А. И., Коробицына О. В., Олевская Е. Р., Хихлова А. О., Кузнецова А. С., Генкель В. В., Хусаинова Г. М. Пациентка с одышкой, дисфагией и меноррагией: синдром Пламмера — Винсона на фоне болезни Виллебранда // Российский журнал гастроэнтерологии, гепатологии, колопроктологии : Журнал. — 2025. — Т. 35, № 3. — С. 114—120. — doi:10.22416/1382-4376-2025-35-3-114-120.
- Ветшев Ф. П., Осминин С. В., Ветшев С. П., Дергунова А. П. Опыт лечения больных с синдромом Пламмера—Винсона // Доказательная гастроэнтерология : Журнал. — 2019. — Т. 8, № 3. — С. 71—76. — doi:10.17116/dokgastro2019803171.