Аутоиммунная гемолитическая анемия
Аутоимму́нная гемолити́ческая анеми́я (АИГА) — приобретённое гематологическое заболевание, характеризующееся разрушением эритроцитов (гемолизом) вследствие выработки аутоантител против антигенов собственных эритроцитов. Патологический процесс может протекать как экстраваскулярно (в макрофагальной системе селезёнки и печени), так и внутрисосудисто. Формы АИГА разделяются в зависимости от серологических свойств аутоантител и температурного оптимума их активности. Каждая форма подразделяется на первичную (идиопатическую) и вторичную, возникающую на фоне других заболеваний. Несмотря на установленную органную специфичность и изученные механизмы гемолиза, точные причины инициальной продукции аутоантител к эритроцитам остаются не полностью ясными[3].
Общие сведения
История
Первые описания гемолитических анемий относятся к середине XIX века. В 1843 году Андрэль описал спонтанную анемию, возникающую без предшествующей кровопотери, и предположил, что её причиной было разрушение эритроцитов. В 1852 году Фогель установил связь между снижением количества эритроцитов и появлением гемоглобина в моче, связав это с инфекционными заболеваниями. Важный вклад в понимание механизмов гемолиза внесли Ванлер и Мазиус (1871), которые связали преждевременное разрушение эритроцитов с развитием желтухи и описали сфероциты в периферической крови. В 1879 году Маккензи исследовал пароксизмальную холодовую гемоглобинурию, обнаружив гемоглобин в моче и связав гемолиз с вазомоторными нарушениями. В конце XIX века произошло разделение гемолитических анемий на врождённые и приобретённые формы. Знаковым событием стало открытие Ландштейнером в 1901 году системы групп крови ABO, за которым последовало описание Донатом и Ландштейнером в 1904 году первого аутоантитела, вызывающего пароксизмальную холодовую гемоглобинурию. Французские учёные Шоффар и Видаль развили эти представления, описав аутогемолизины при приобретённой гемолитической желтухе и введя термин «приобретённая гемолитическая анемия». В 1911 году Микели выполнил первую спленэктомию при приобретённой гемолитической анемии, а Банти ввёл термин «гемолитическая спленомегалия» и описал роль ретикулоэндотелиальной системы в разрушении эритроцитов[4].
Термин «аутоиммунная гемолитическая анемия» был впервые введён Янгом и соавторами в 1951 году. Они предположили, что выработка аутоантител возникает вследствие нарушения регуляторных механизмов иммунной системы. Первоначально некоторые исследователи отвергали аутоиммунную природу заболевания, предлагая название «антиглобулин-позитивная гемолитическая анемия», однако к 1960 году аутоиммунная теория получила всеобщее признание. В начале 1960-х годов изучались возрастные особенности АИГА. Хотя изначально считалось, что тепловая форма АИГА редко встречается у детей, в 1962 году было документально подтверждено её наличие у новорождённого. В 1970-х годах были детализированы характеристики аутоантител: установлено преобладание подклассов IgG1 и IgG3 при тепловой форме АИГА, но также обнаружена значительная роль IgG2 и IgA антител. В 1980-х годах исследования сфокусировались на иммунологических механизмах АИГА и взаимоотношениях аутоантител и антигенов. Установлена роль главного комплекса гистосовместимости II класса в презентации антигенов макрофагами T-клеткам, важность цитокинов в активации антиген-специфичных T-клеток. Подтверждена роль Fc-рецепторов для IgG и C3b-рецепторов в процессе фагоцитоза. Уточнена специфичность аутоантител к антигенам групп крови[4].
Классификация
АИГА подразделяется на первичную и вторичную формы. Первичная АИГА составляет более 60 % случаев. Вторичная АИГА возникает при различных патологических состояниях[5].
Дополнительная классификация АИГА основана на температурных характеристиках опсонизации и разрушения эритроцитов. Выделяют семь основных типов заболевания, дифференцируемых преимущественно по серологическим признакам[5][6]:
- тепловая АИГА;
- холодовая АИГА;
- смешанная АИГА;
- пароксизмальная холодовая гемоглобинурия, также известная как АИГА с положительной пробой Доната — Ландштейнера;
- АИГА с отрицательной прямой пробой Кумбса;
- лекарственно-индуцированная АИГА;
- синдром лимфоцитов-пассажиров (связанный с трансплантацией и проявляющийся как АИГА со специфическими характеристиками).
Этиология
В основе АИГА могут лежать различные факторы. Одним из ключевых является перекрёстная реакция между антигенами инфекционных агентов и собственными молекулами организма, известная как «молекулярная мимикрия». Другим важным механизмом является лекарственно-индуцированная модификация мембраны эритроцитов через адсорбцию или связывание лекарственных препаратов. При В-клеточных лимфопролиферативных заболеваниях может происходить продукция аутоантител клонами лимфоцитов. Нарушение толерантности к собственным антигенам также может быть обусловлено наличием герминальных мутаций, нарушающих созревание иммунной системы, как при врождённых иммунодефицитах. Дополнительным фактором является постоянная экспозиция аутоантигенов эритроцитов, что наблюдается у пациентов с неэффективным эритропоэзом, например, при врождённых анемиях и миелодиспластических синдромах. Эти механизмы в совокупности способствуют нарушению иммунологической толерантности и развитию аутоиммунного ответа против собственных эритроцитов[7].
Патогенез
Патогенез АИГА представляет собой сложный многокомпонентный процесс, включающий несколько ключевых механизмов. Основу заболевания составляет продукция антиэритроцитарных аутоантител В-клеточным компартментом, которая сопровождается нарушением гомеостаза Т-лимфоцитов. Финальное разрушение эритроцитов происходит через систему мононуклеарных фагоцитов и активацию каскада комплемента. Важным определяющим фактором патогенеза и тяжести АИГА является эффективность компенсаторного ответа костного мозга[7].
- Антиэритроцитарные аутоантитела продуцируются В-лимфоцитами на разных стадиях созревания. При тепловой АИГА IgG-аутоантитела обычно поликлональны и вырабатываются лимфоцитами костного мозга и селезёнки, в то время как IgM при холодовой АИГА чаще моноклональны и продуцируются CD20+ CD5- лимфоидным инфильтратом костного мозга. Аналогичные механизмы наблюдаются при АИГА, вторичной к лимфопролиферативным заболеваниям[7].
- Со стороны Т-клеточного звена наблюдается дисбаланс между Th1, Th2, Th17 и регуляторными Т-клетками, а также нарушение продукции цитокинов, способствующее нарушению иммунной толерантности. Отмечается гиперaктивность Th2-ответа с повышением уровней интерлейкинов-4, −6 и −10, одновременно со снижением интерферона-γ, что стимулирует гуморальный аутоиммунитет. Также наблюдается повышенная активность цитотоксических CD8+ Т-лимфоцитов, натуральных киллеров и активированных макрофагов с увеличением уровней ИЛ-2 и ИЛ-12. Повышение активности трансформирующего фактора роста-бета способствует дифференцировке Th17, которые продуцируют ИЛ-17, усиливающий провоспалительный и аутоиммунный ответ[7].
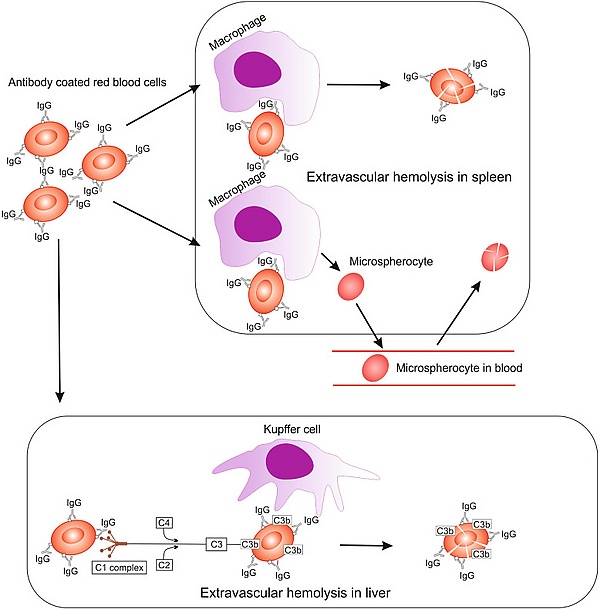
- Гемолиз, опосредованный моноцитарно-макрофагальной системой, характерен для тепловой АИГА и происходит преимущественно экстраваскулярно в селезёнке. Механизм включает распознавание Fc-фрагмента IgG клетками моноцитарно-макрофагальной системы с последующим фагоцитозом эритроцитов и антитело-зависимой цитотоксичностью. Селезёнка также функционирует как лимфоидный орган, способный продуцировать аутоантитела[7].
- Система комплемента активируется по классическому пути преимущественно пентамерным IgM (в основном холодовым, реже — тепловым), а также мономерным IgG, с вариабельной активностью в зависимости от подкласса. Это приводит к фагоцитозу C3b-покрытых клеток (экстраваскулярный гемолиз) или, реже, к активации терминального комплекса комплемента с развитием внутрисосудистого гемолиза[7].
- Костный мозг компенсирует анемию путём усиления эритропоэза, что отражается увеличением количества ретикулоцитов в периферической крови[7].
Эпидемиология
Согласно исследованиям, ежегодная заболеваемость АИГА составляет 1—2 случая на 100 000 населения. Среди всех вариантов заболевания наиболее распространённой формой является тепловая АИГА, на которую приходится около двух третей всех случаев. Второй по частоте формой является холодовая АИГА, составляющая 15—20 % случаев. Смешанная АИГА, представляющая собой сочетание тепловой и холодовой форм, занимает третье место по распространённости[5].
Диагностика
Клинические проявления АИГА характеризуются сходством при всех формах заболевания, но варьируют по степени тяжести. Общие симптомы, включая слабость, вялость, повышенную утомляемость и тахикардию, обусловлены анемическим синдромом. При физикальном обследовании выявляются бледность и желтушность кожи и слизистых оболочек, а также спленомегалия различной степени выраженности[3].
При тепловой форме АИГА незначительный гемолиз может протекать субклинически, однако при его усилении развивается тяжёлая тканевая гипоксия. Выраженное пожелтение кожи наблюдается при массивном гемолизе. Умеренная спленомегалия характерна для активного гемолиза, тогда как диспропорциональное увеличение селезёнки указывает на вторичный характер заболевания, особенно при лимфопролиферативных заболеваниях[5].
При холодовой форме АИГА симптомы связаны с температурными колебаниями. Быстрое охлаждение провоцирует гемолиз, при этом доминируют проявления анемии. Воздействие холода вызывает акроцианоз, а длительное воздействие может привести к ишемии и некрозу тканей[5].
Смешанная форма АИГА составляет менее 10 % случаев, характеризуется хроническим течением и активацией антител в широком температурном диапазоне[5].
Пароксизмальная холодовая гемоглобинурия преимущественно встречается у детей и ассоциирована с инфекциями. Клинические проявления включают боль в спине или ногах, абдоминальные спазмы, лихорадку, озноб, желтуху и потемнение мочи[5].
Клинический анализ крови: снижение концентрации гемоглобина, уменьшение количества эритроцитов, повышение среднего объёма эритроцитов, ретикулоцитоз, возможное появление нормобластов (ядерных предшественников эритроцитов). Возможно развитие лейкоцитоза со сдвигом формулы влево, повышение скорости оседания эритроцитов[3][7].
Биохимический анализ крови: характерно повышение концентрации билирубина преимущественно за счёт непрямой фракции, повышение активности лактатдегидрогеназы, снижение концентрации гаптоглобина[3][7].
При микроскопии мазка крови часто наблюдаются характерные изменения: полихроматофилия, анизоцитоз и пойкилоцитоз. В случаях тепловой формы АИГА с образованием значительного количества сфероцитов выявляются классические диагностические признаки сфероцитарной анемии: сфероциты в мазке периферической крови, а также снижение осмотической резистентности эритроцитов как до, так и после инкубации[3][7].
Дифференциальная диагностика
Дифференциальная диагностика АИГА проводится со следующими заболеваниями[8]:
- трансфузионные реакции;
- микроангиопатическая гемолитическая анемия;
- тромботическая тромбоцитопеническая пурпура;
- гемолитико-уремический синдром;
- HELLP-синдром;
- Т-клеточный лейкоз из больших гранулярных лимфоцитов;
- лекарственно-индуцированная тромботическая микроангиопатия;
- гемолитическая болезнь новорождённых;
- дефицит глюкозо-6-фосфатдегидрогеназы;
- наследственный сфероцитоз;
- серповидно-клеточная анемия;
- талассемии.
Осложнения
Наиболее частыми осложнениями АИГА являются[9]:
- некроз кожи;
- кожные изъязвления;
- дефицит витамина В9;
- тромбоэмболические осложнения;
- острая почечная недостаточность.
Поскольку АИГА представляет собой аутоиммунный процесс, многие методы лечения носят иммуносупрессивный характер. Это повышает вероятность развития инфекций, в том числе оппортунистических. Помимо общего повышения инфекционного риска, каждый препарат имеет свои специфические риски осложнений: психозы, экзогенный синдром Кушинга, стероидный сахарный диабет, ожирение, артериальная гипертензия, остеопороз (при применении стероидов), кардиотоксичность (циклофосфамид), нефротоксичность (циклоспорин), анафилаксия (плазмаферез) или нейтропения (микофенолат)[3][9].
Лечение
Основой терапии АИГА являются иммуносупрессивные препараты. При лёгких бессимптомных формах возможна выжидательная тактика. Первой линией лечения служат глюкокортикостероиды, преимущественно преднизолон, которые подавляют функциональную активность макрофагов и предотвращают фагоцитоз антитело-связанных эритроцитов. Хотя начальный ответ на терапию отмечается у большинства пациентов, значительная часть сталкивается с рецидивами при снижении дозировки или отмене препарата[10].
В качестве альтернативы стандартной схеме применяется пульс-терапия метилпреднизолоном, демонстрирующая повышенную эффективность и улучшенный профиль безопасности. При неэффективности или непереносимости кортикостероидов терапией второй линии является ритуксимаб — моноклональное антитело против CD20-антигена В-лимфоцитов, показывающий высокий процент стойких ремиссий. Альтернативным методом остаётся спленэктомия, эффективная у значительной части пациентов, но несущая риски тромботических и инфекционных осложнений[10].
В экстренных ситуациях и при тяжёлых инфекционных осложнениях может применяться внутривенный иммуноглобулин, однако его эффект обычно носит временный характер. В резистентных случаях рассматриваются препараты третьей линии, включая различные иммуносупрессанты. Плазмаферез эффективен в качестве терапии «скорой помощи» в острых ситуациях. Активно исследуются новые терапевтические подходы с применением современных моноклональных антител, ингибиторов внутриклеточных сигнальных путей и компонентов комплемента[10].
Прогноз
Все группы аутоиммунных гемолитических анемий ассоциированы с повышенной смертностью по сравнению с общей популяцией. По данным исследований, показатели однолетней выживаемости и медиана выживаемости составили 82,7 % и 9,8 года для первичной АИГА, 69,1 % и 3,3 года для вторичной АИГА. Прогноз был сопоставим с общей популяцией только у пациентов с первичной АИГА моложе 30 лет. Во всех других возрастных и диагностических подгруппах различия были существенными. Накопленная причинно-специфическая смертность в течение 1 года была повышена среди пациентов по сравнению с контрольной группой[11].
Примечания
Литература
- Васильченкова П.И., Гальцева И.В., Лукина Е.А. Аутоиммунная гемолитическая анемия: современное состояние вопроса // Онкогематология. — 2023. — Т. 18, № 2. — С. 60—67. — doi:10.17650/1818-8346-2023-18-2-60-67.
- Shah S., Padrnos L. Complications of Autoimmune Hemolytic Anemia (англ.) // Hematology/Oncology Clinics of North America. — 2022. — April (vol. 36, no. 2). — P. 353—363. — doi:10.1016/j.hoc.2021.12.003.
- Fattizzo B., Barcellini W. Autoimmune hemolytic anemia: causes and consequences (англ.) // Expert Review of Clinical Immunology. — 2022. — July (vol. 18, no. 7). — P. 731—745. — doi:10.1080/1744666X.2022.2089115.