Щавелевая кислота
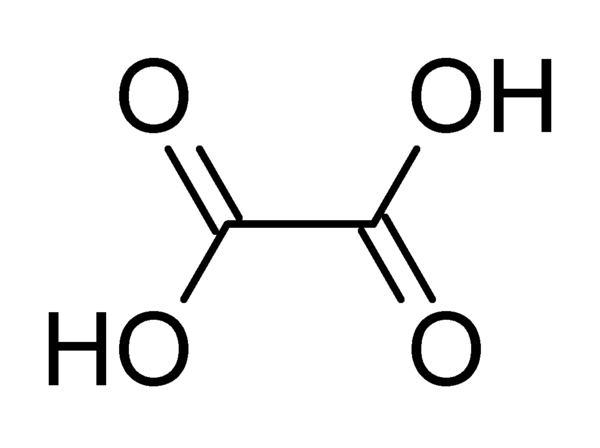
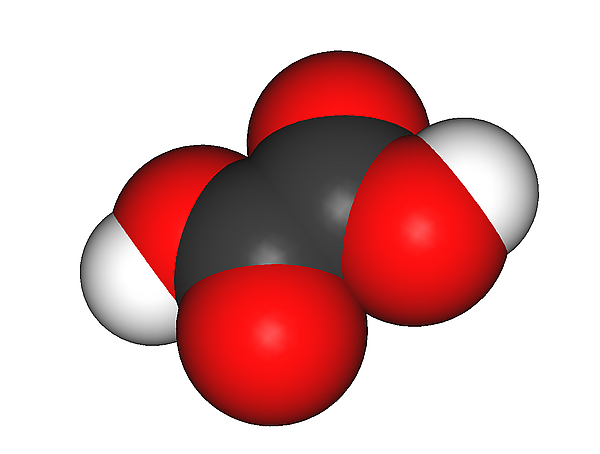
Щаве́левая кислота (этандио́вая кислота, химическая формула — C2H2O4, или HOOC—COOH) — сильная химическая органическая кислота, относящаяся к классу предельных карбоновых кислот. Является простейшей двухосновной карбоновой кислотой.
При стандартных условиях, щавелевая кислота — это двухосновная предельная карбоновая кислота, представляющая собой кристаллическое вещество белого цвета.
Соли и сложные эфиры щавелевой кислоты называются оксала́тами.
Что важно знать
| Щавелевая кислота | |
|---|---|
| Общие | |
| Систематическое наименование |
Этандиовая кислота |
| Традиционные названия | Щавелевая кислота |
| Хим. формула | C2H2O4 |
| Рац. формула | HOOC−COOH |
| Физические свойства | |
| Состояние | Кристаллическое |
| Молярная масса |
90,04; 126,0625 (дигидрат) г/моль |
| Плотность | 1,36 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 189,5 °C |
| • сублимации | 215 ± 1[1] |
| • кипения | 365 |
| • разложения | 100—130 °C |
| • вспышки | 166 °C |
| Мол. теплоёмк. | 108,8 Дж/(моль·К) |
| Энтальпия | |
| • образования | −817,38 кДж/моль |
| • сгорания | −251,8 |
| • растворения | −9,58 кДж/моль |
| • сублимации | 90,58 кДж/моль |
| Давление пара | 0,001 ± 0,001[1] |
| Химические свойства | |
| Константа диссоциации кислоты | 1,25; 4,14 |
| Растворимость | |
| • в воде |
10 г/100 г (20 °C); 25 г/100 г (44,5 °C); 120 г/100 г (100 °C) |
| Структура | |
| Кристаллическая структура | Моноклинная |
| Дипольный момент | 0,1⋅10−30 Кл·м |
| Классификация | |
| Рег. номер CAS | 144-62-7 |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 971 |
| UNII | 9E7R5L6H31 |
| CompTox Dashboard EPA | DTXSID0025816 |
| Рег. номер EINECS | 205-634-3 |
| SMILES | |
| InChI | |
| RTECS | RO2450000 |
| ChEBI | 16995 |
| Номер ООН | 3261 |
| ChemSpider | 946 |
| ECHA InfoCard | 100.005.123 |
| Безопасность | |
| Предельная концентрация | 0,5 мг/дм3 (в воде водоёмов хозяйств бытового пользования) |
| ЛД50 | 149,4 мг/кг |
| Токсичность | ирритант |
| Сигнальное слово | Опасно |
| Пиктограммы СГС |
Пиктограммы СГС: |
| NFPA 704 | |
История
Впервые щавелевая кислота синтезирована в 1824 году немецким химиком Фридрихом Вёлером из дициана.
Нахождение в природе
Получение
В промышленности щавелевую кислоту получают окислением углеводов, спиртов и гликолей смесью и в присутствии , либо окислением этилена и ацетилена в присутствии или , а также окислением пропилена жидким .
Перспективен способ получения щавелевой кислоты из и едкого натра через формиат натрия:
- .
Известен также метод получения щавелевой кислоты окислением ацетилена перманганатом калия в нейтральной среде при низкой температуре с последующей обработкой кислотой[2]:
Свойства
- Энтальпия сгорания (ΔH0сгор) −251,8 кДж/моль
- Температура декарбоксилирования 166—180 °C
Применение
В лабораториях щавелевую кислоту применяют для получения хлороводорода и иодоводорода:
- .
Также щавелевая кислота используется для лабораторного синтеза диоксида хлора:
- .
Щавелевая кислота и оксалаты находят применение в текстильной и кожевенной промышленности как протрава. Они служат компонентами анодных ванн для осаждения металлических покрытий — алюминия, титана и олова.
Щавелевая кислота и оксалаты являются реагентами, используемыми в аналитической и органической химии. Они входят в составы для удаления ржавчины и оксидных плёнок на металле; применяются для осаждения из раствора редкоземельных элементов.
Производные щавелевой кислоты — диалкилоксалаты, главным образом диэтилоксалат и дибутилоксалат — применяются как растворители целлюлозы. Ряд сложных эфиров щавелевой кислоты и соединений группы замещённых фенолов используются как хемилюминесцентные реагенты.
Щавелевая кислота используется в пчеловодстве для защиты от клеща Варроа.
Особенности обращения и физиологическое действие
Щавелевая кислота и её соли токсичны в высоких концентрациях. Некоторые соли щавелевой кислоты, — оксалаты, в частности, оксалат кальция и оксалат магния очень плохо растворимы в воде и оседают в почечных лоханках в виде конкрементов различного размера (в виде песка, камней), иногда причудливой формы (так называемые коралловые камни).
ПДК в воде водоёмов хозяйств бытового пользования — 0,5 мг/дм³. Лимитирующий показатель вредности — общесанитарный.
Щавелевая кислота вызывает ожоги при контакте с ней либо при приёме внутрь[3]. Она не является мутагеном или канцерогеном; является опасной в случае вдыхания; опасна и чрезвычайно разрушительна по отношению к биологическим тканям слизистых оболочек и верхних дыхательных путей. Опасна в случае проглатывания в чистом виде; вызывает химические ожоги при контакте с кожей или попадании в глаза. Симптомы включают чувство жжения, кашель, хрипы, ларингит, одышку, спазм, воспаление и отёк гортани, воспаление и отёк бронхов, пневмонит, отёк лёгких[4].
У людей щавелевая кислота при приёме перорально имеет минимальную летальную дозу (LDLo) 140-150 мг/кг[5].
Сообщалось, что смертельная оральная доза составляет от 15 до 30 граммов[6].
Токсичность щавелевой кислоты обусловлена почечной недостаточностью, вызванной осаждением в почках твёрдого оксалата кальция[7], основного компонента кальциевых камней в почках. Щавелевая кислота также может вызывать боль в суставах из-за образования в них аналогичных отложений (аналогично подагре). Приём внутрь больших количеств этиленгликоля приводит к образованию щавелевой кислоты в организме в качестве метаболита, что, в свою очередь, может привести к острой почечной недостаточности.
Примечания
Литература
- Тутурин Н. Н.,. Щавелевая кислота // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907.
- Арциховский В. М. Щавелевая кислота в растениях // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907.
- Зефиров Н. С. и др. Химическая энциклопедия. — М.: Большая Российская Энциклопедия, 1998. — Т. 5: Три — Ятр. — 783 с. — ISBN 5-85270-310-9.












![{\displaystyle {\ce {NaOH + CO ->[] HCOONa ->[][{\ce {-H_2}}]}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/15a0b828888d8a4f5ebfc1151440fa14350d6da3)
![{\displaystyle {\ce {-> NaOOC-COONa ->[{\ce {+ H^+}}] HOOC-COOH}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/17d78d294162fab6e75cb26dbd60075c12b755f7)