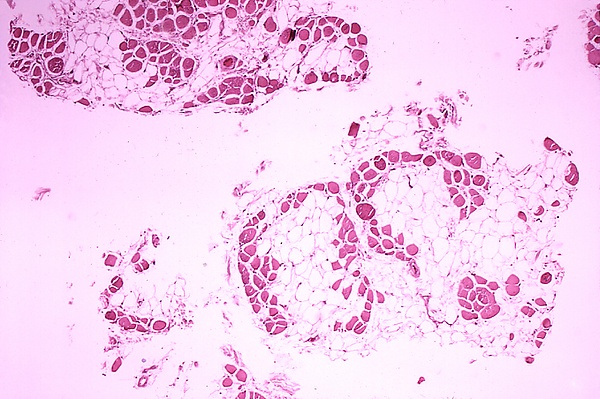
Мышечная дистрофия Дюшенна
Мы́шечная дистрофи́я Дюше́нна (МДД, миодистрофи́я Дюше́нна) — это тяжёлое наследственное заболевание с Х-сцепленным рецессивным типом наследования, относящееся к группе первичных миопатий. Его причиной являются патогенные мутации в гене дистрофина (DMD), что приводит к прогрессирующей дегенерации мышечной ткани. Основу клинической картины составляют двигательные нарушения: прогрессирующая мышечная слабость и атрофия, трудности при ходьбе, частые падения, характерный симптом Говерса (вставание «лесенкой»), псевдогипертрофия икроножных мышц, быстрое формирование контрактур суставов, снижение выносливости и потеря ранее приобретённых двигательных навыков. Заболевание также сопровождается немоторными проявлениями, включая задержку речевого и когнитивного развития, нарушения артикуляции и поведенческие особенности. Течение МДД носит неуклонно прогрессирующий характер. Поражение распространяется на сердечную мышцу, приводя к развитию кардиомиопатии и сердечной недостаточности, которые к подростковому и взрослому возрасту становятся одной из ключевых проблем. Стратегия ведения пациентов с МДД включает как симптоматическую, так и патогенетическую терапию, направленную на коррекцию основного генетического дефекта[1][2].
Общие сведения
История
Ранние случаи заболевания, которое впоследствии стало известно как МДД, фиксировались уже в первой половине XIX века. Первое описание принадлежит неаполитанским врачам Г. Конте и Л. Джойа (1836 г.), но их наблюдения не получили широкого признания, будучи ошибочно приняты за проявление туберкулёза. В 1847 году английский врач В. Литтл сообщил о болезни со сходной клинической картиной. Однако систематическое изучение начал Эдвард Мерион, который в 1851 году детально описал симптомы, высказал предположения о возможном наследственном характере и, основываясь на результатах аутопсии, впервые выдвинул гипотезу о дефекте клеточной мембраны как основе болезни. Позднее, в 1868 году, французский невролог Гийом Дюшен дал классическое и полное описание заболевания, включавшее наблюдение жирово-фиброзного перерождения мышц в биоптатах, благодаря чему болезнь была названа его именем. Ещё одним важным клиническим наблюдением стало описание Уильямом Говерсом в 1886 году характерного «приёма» для вставания с пола, который стал одним из патогномоничных симптомов. Несмотря на то что МДД была известна как клиническая единица с 1860-х годов, её этиология оставалась нераскрытой более века. Лишь в 1986 году лаборатория Луиса Кункеля идентифицировала ответственный ген DMD, а в 1987-м было доказано, что мутации в нём приводят к отсутствию белка дистрофина[3][4].
Классификация
МДМ относится к дистрофинопатиям[5]
Этиология
Генетической основой МДД является мутация в гене DMD, кодирующем белок дистрофин. Этот ген, один из крупнейших в геноме человека, расположен в Х-хромосоме и наследуется по Х-сцепленному рецессивному типу, что объясняет преимущественную заболеваемость лиц мужского пола, в то время как женщины чаще являются носительницами патологического варианта гена. Мутация в большинстве случаев передаётся по наследству, однако примерно в трети наблюдений возникает de novo (спорадически). Спектр мутаций разнообразен: примерно 65 % составляют крупные делеции одного или нескольких экзонов (всего ген содержит 79 экзонов), около 10 % — дупликации, а оставшиеся случаи приходятся на точечные и малые мутации, среди которых 10-15 % представляют собой нонсенс-мутации (стоп-кодоны), приводящие к преждевременному прекращению синтеза белка[2][6].
Результатом этих генетических нарушений является дефицит или функциональная неполноценность белка дистрофина. Этот высокомолекулярный белок выполняет критически важную структурную и механическую роль в мышечных волокнах скелетной мускулатуры, миокарда и диафрагмы. Его ключевая функция — связывание внутриклеточного цитоскелета (актиновых филаментов) с белковым комплексом в сарколемме (сарко- и дистрогликанами), который, в свою очередь, соединяется с внеклеточным матриксом. Таким образом, дистрофин формирует эластичную связь, обеспечивающую структурную целостность мембраны мышечного волокна во время циклов сокращения и расслабления. Он действует как амортизатор, защищающий сарколемму от повреждения при механической нагрузке и способствующий возвращению мышцы в исходное состояние после сокращения. Отсутствие или выраженный дефект дистрофина приводит к потере стабильности мембраны, хроническому повреждению мышечных волокон, их некрозу и прогрессирующему замещению соединительной и жировой тканью, что и лежит в основе клинических проявлений болезни[2][6].
Патогенез
Патогенез МДД представляет собой сложный каскад патологических процессов, инициируемых дефицитом или функциональной неполноценностью ключевого структурного белка — дистрофина. Этот высокомолекулярный белок, относящийся к спектриновому суперсемейству, локализуется на внутренней поверхности сарколеммы (мембраны мышечного волокна) скелетной мускулатуры, миокарда и диафрагмы. Основная функция дистрофина — формирование механической и эластичной связи между внутриклеточным цитоскелетом (актиновыми филаментами) и внеклеточным матриксом. Эта связь осуществляется через дистрогликановый комплекс в сарколемме. Дистрофин выступает в роли критического амортизатора, который обеспечивает структурную целостность мембраны мышечного волокна во время циклов сокращения и расслабления, защищая её от повреждения при механической нагрузке и способствуя возвращению мышцы в исходное состояние. Отсутствие или выраженный дефект дистрофина приводит к разрыву этой стабилизирующей связи. В результате сарколемма теряет стабильность, становится хрупкой и подверженной хроническому повреждению. Это запускает каскад вторичных процессов[7]:
- следствием мембранной нестабильности становится дисрегуляция кальция. Повышенная проницаемость сарколеммы, наряду с дисфункцией кальциевых каналов и саркоплазматического ретикулума, приводит к патологическому повышению уровня внутриклеточного кальция. Кальциевая перегрузка активирует протеазы (кальпаины), которые разрушают структурные белки клетки, и запускает другие сигнальные пути, ведущие к дегенерации и некрозу мышечных волокон;
- некроз волокон и постоянный выброс внутриклеточного содержимого (молекулярных паттернов повреждения) инициируют хронический воспалительный процесс. В здоровой мышце острое воспаление после повреждения строго контролируется и сменяется регенеративной фазой. При МДД из-за постоянного повреждения воспаление становится хроническим и деструктивным. Мышечная ткань инфильтрируется иммунными клетками, в первую очередь провоспалительными макрофагами и лимфоцитами (CD4+ и CD8+ Т-клетки), которые не только очищают некротический материал, но и сами способствуют повреждению волокон через цитокины и цитотоксические механизмы. Это воспаление нарушает нормальный цикл регенерации;
- хроническое воспаление, окислительный стресс и кальциевая перегрузка негативно влияют на митохондриальную функцию и энергетику. В митохондриях дистрофической мышцы нарушается структура, снижается способность к синтезу АТФ и увеличивается продукция активных форм кислорода (АФК). Источниками избыточных АФК являются как митохондриальная электрон-транспортная цепь, так и фермент NOX2 (НАДФН-оксидаза 2), активность которого повышена. АФК повреждают белки сократительного аппарата (актин, миозин), липиды мембран и ДНК, усугубляя клеточную дисфункцию и способствуя открытию митохондриальных пор, что ведёт к гибели клеток;
- наконец, повторяющиеся циклы повреждения и неполноценной регенерации на фоне хронического воспаления приводят к прогрессирующему фиброзу — замещению мышечной ткани рубцовой соединительной. Ключевую роль в этом играют факторы роста, например, трансформирующий фактор роста бета, которые стимулируют фибробласты к избыточному синтезу компонентов внеклеточного матрикса, преимущественно коллагенов I и III типа. Фиброзная ткань увеличивает жёсткость мышцы, ещё больше ограничивает её сократительную функцию и создаёт барьер для потенциальных терапевтических вмешательств и естественной регенерации.
Таким образом, патогенез МДД представляет собой порочный круг, где первичный дефект белка дистрофина запускает каскад вторичных процессов — нестабильность мембраны, кальциевый дисбаланс, хроническое воспаление, митохондриальную дисфункцию, окислительный стресс и фиброз. Эти процессы взаимно усиливают друг друга, приводя к необратимой потере мышечных волокон и прогрессирующей мышечной слабости[7].
Эпидемиология
Распространённость МДД в мире оценивается на уровне 1 случая на 5000 новорождённых мальчиков. Данные по распространённости МДД в России отсутствуют[6].
Диагностика
Диагноз МДД часто устанавливается с запозданием, уже после появления очевидных симптомов, так как в первые 2-3 года жизни интенсивное естественное развитие мышц может маскировать начальные дистрофические процессы. Тем не менее, тщательное обследование на этом этапе часто выявляет задержку речевого и моторного развития: дети позже начинают держать голову, сидеть и ходить (нередко после 18 месяцев). По мере прогрессирования болезни, обычно с 3-5 лет, формируется классическая клиническая картина. Появляется и нарастает мышечная слабость, преимущественно в проксимальных отделах конечностей, что приводит к снижению переносимости нагрузок, быстрой утомляемости, неуклюжести и частым падениям. Детям становится трудно подниматься по лестнице. Характерным признаком является симптом Говерса: ребёнок, вставая с пола, активно помогает себе руками, «взбираясь» по собственным бёдрам. Походка становится переваливающейся («утиной»), часто наблюдается ходьба на носках. При осмотре выявляются псевдогипертрофия (ложное увеличение) икроножных мышц, «крыловидные» лопатки, усиленный поясничный лордоз, снижение мышечного тонуса и сухожильных рефлексов. Формируются контрактуры суставов, в первую очередь голеностопных. Параллельно с поражением скелетной мускулатуры развивается кардиомиопатия, которая может длительное время протекать субклинически из-за ограниченной физической активности пациентов, но со временем прогрессирует до дилатационной формы, сопровождаясь нарушениями ритма и проводимости, а на поздних этапах — симптомами хронической сердечной недостаточности (тахикардия, отеки, одышка). После потери способности к самостоятельной ходьбе (в среднем в возрасте 10-13 лет) прогрессирует слабость мышц верхних конечностей и туловища, формируются тяжёлые контрактуры и выраженный сколиоз. Ключевой проблемой становится дыхательная недостаточность, обусловленная слабостью дыхательной мускулатуры. Жизненная ёмкость лёгких неуклонно снижается, что приводит к хроническим респираторным инфекциям и часто — к синдрому обструктивного апноэ сна[6].
Помимо двигательных и висцеральных нарушений, для МДД характерны немоторные проявления. Примерно у трети пациентов наблюдаются интеллектуальные нарушения разной степени выраженности, особенности нейрокогнитивного развития, памяти и поведения[6].
Развитие клинической картины при МДД происходит постадийно[6]:
- бессимптомная (доклиническая) стадия: на этом этапе заболевание может быть случайно обнаружено по результатам лабораторных исследований;
- ранняя амбулаторная стадия: пациент сохраняет способность к самостоятельной ходьбе, однако появляются и нарастают характерные симптомы. Типичным признаком является псевдогипертрофия (ложное увеличение) икроножных мышц. Способность подниматься по лестнице сохраняется;
- поздняя амбулаторная стадия: самостоятельное передвижение возможно, но значительно затруднено. Все симптомы предыдущей стадии прогрессируют: нарастают трудности при ходьбе, пациент окончательно теряет способность подниматься по лестнице и вставать с пола без посторонней помощи;
- ранняя неамбулаторная стадия: пациент утрачивает способность к самостоятельной ходьбе и для передвижения постоянно нуждается в инвалидной коляске. На этом этапе активно развиваются ортопедические осложнения, прежде всего сколиоз. При этом сохраняется достаточная двигательная активность рук для самостоятельного управления креслом-коляской;
- поздняя неамбулаторная стадия: происходит значительное ограничение функций верхних конечностей, становится трудно удерживать положение сидя. Ключевыми клиническими проблемами становятся прогрессирующая сердечная и дыхательная недостаточность, определяющие прогноз и качество жизни.
При электрокардиографии у пациентов с МДД часто выявляются признаки гипертрофии и перегрузки правого желудочка (высокие зубцы R, глубокие Q в соответствующих отведениях), а также инверсия зубца Т[8].
Электромиография при МДД, как правило, демонстрирует характерный миопатический паттерн: двигательные единицы имеют полифазную структуру, короткую длительность и сниженную амплитуду потенциалов действия[8].
Эхокардиография позволяет выявить признаки дилатационной кардиомиопатии практически у всех пациентов к позднему подростковому или молодому взрослому возрасту[9].
При ультразвуковом исследовании поражённых мышц отмечается повышение их эхогенности с одновременным снижением визуализации контура подлежащей кости[8].
При необходимости для детальной оценки структурных изменений миокарда и сосудов выполняется магнитно-резонансная томография сердца с контрастным усилением. Данное исследование позволяет визуализировать состояние правого и левого желудочков, а также магистральных и периферических сосудов[6].
Биохимический анализ крови: характерно повышение активности креатинфосфокиназы, трансаминаз и лактатдегидрогеназы[6].
При гистологическом исследовании биоптатов мышц на ранних стадиях заболевания обнаруживаются преимущественно вариабельность размеров мышечных волокон, а также очаги с признаками дегенерации и регенерации. По мере прогрессирования патологии изменения становятся более выраженными: отмечаются значительные различия в калибре волокон, множественные дегенерирующие и регенерирующие волокна. Также визуализируются округлые, непрозрачные волокна, волокна с центрально расположенными ядрами, признаки расщепления волокон, а также прогрессирующее замещение мышечной ткани соединительной и жировой. На поздних стадиях количество регенерирующих волокон значительно снижается. В терминальной фазе мышца практически полностью замещается жировой тканью, в которой остаются лишь отдельные островки сохранившихся мышечных волокон[8].
При иммуногистохимическом исследовании биоптатов мышц с окрашиванием на АТФ-азу выявляется преобладание коллагеновых волокон I типа и утрата чёткого гистохимического мозаичного рисунка, характерного для нормальной мышцы[8].
Иммуноцитохимические исследование позволяет обнаружить сохранение фетальной и медленной изоформ миозина во многих мышечных волокнах[8].
Молекулярно-генетический анализ методом секвенирования по Сенгеру: характерно выявление мутации в гене DMD[6].
Дифференциальная диагностика
Дифференциальная диагностика МДД проводится со следующими заболеваниями[8][9]:
- мышечная дистрофия Беккера;
- промежуточная форма мышечной дистрофии;
- миотоническая мышечная дистрофия;
- конечностно-поясная мышечная дистрофия;
- врождённая миотоническая дистрофия;
- врождённая мышечная дистрофия;
- мышечная дистрофия Эмери — Дрейфуса;
- спинальная мышечная атрофия.
Осложнения
Течение МДД сопровождается развитием системных осложнений, которые значительно утяжеляют состояние пациента и определяют качество жизни[6][8]:
- остеопороз развивается практически у всех пациентов, часто ещё на амбулаторной стадии, и прогрессирует с возрастом. Снижение плотности костной ткани, в сочетании с частыми падениями, приводит к высокому риску переломов длинных трубчатых костей, частота которых составляет от 21 % до 44 %. Даже незначительные травмы (например, растяжение связок голеностопного сустава) и связанная с ними иммобилизация могут ускорить потерю способности к ходьбе;
- двигательные нарушения и ортопедические осложнения: вследствие прогрессирующей мышечной слабости и дисбаланса формируются стойкие контрактуры суставов (голеностопных, коленных, тазобедренных, локтевых), развивается выраженный S-образный сколиоз, требующий ношения корсета или хирургической коррекции. Эти изменения способствуют ранней зависимости от инвалидной коляски;
- кардиореспираторные осложнения: ключевыми и жизнеугрожающими являются сердечная и дыхательная недостаточность. Кардиомиопатия прогрессирует до дилатационной формы, сопровождается нарушениями ритма и проводимости. Поражение дыхательной мускулатуры приводит к снижению жизненной ёмкости лёгких, рецидивирующим инфекциям, синдрому обструктивного апноэ сна и потребности в респираторной поддержке;
- желудочно-кишечные осложнения и проблемы с питанием: часто отмечаются дисфункция желудочно-кишечного тракта и нутритивные расстройства, приводящие к дисбалансу питательных веществ, обезвоживанию, патологической потере или набору массы тела. На поздних стадиях присоединяются дисфагия (нарушение глотания) и контрактура нижней челюсти;
- нежелательные явления, связанные с терапией: длительный приём системных глюкокортикостероидов, являющихся стандартом патогенетической терапии, вызывает ряд серьёзных побочных эффектов. К ним относятся задержка роста и полового созревания, надпочечниковая недостаточность, нарушение толерантности к глюкозе и развитие сахарного диабета 2-го типа, артериальная гипертензия, ускоренное развитие остеопороза и формирование катаракты.
Лечение
Лечение МДД является комплексным и включает следующие направления[6]:
- патогенетическая медикаментозная терапия: основу лечения составляет длительная терапия системными глюкокортикостероидами (преднизолон), которая считается «золотым стандартом». Гормоны назначаются на этапе стабилизации моторных функций с целью замедления потери мышечной силы, отсрочки развития контрактур и сколиоза, а также для сохранения кардиореспираторных функций. Для подгруппы пациентов (примерно 18-20 %) с нонсенс-мутацией в гене DMD применяется таргетный препарат аталурен. Он способствует синтезу полноразмерного белка дистрофина за счёт преодоления преждевременного стоп-кодона. Терапия аталуреном показана амбулаторным пациентам старше 2 лет и, по данным исследований, способна значимо продлить период самостоятельной ходьбы и сохранить дыхательную функцию;
- симптоматическая медикаментозная терапия:
- кардиопротективная терапия: с целью профилактики и лечения кардиомиопатии пациентам с раннего возраста (обычно с 6 лет) назначаются ингибиторы АПФ или блокаторы рецепторов ангиотензина II. При развитии систолической дисфункции, тахикардии или признаков сердечной недостаточности к терапии добавляются бета-адреноблокаторы, диуретики и антагонисты альдостерона;
- профилактика остеопороза: всем пациентам показан мониторинг и медикаментозная коррекция концентрации витамина D в крови. При развитии остеопении или патологических переломов назначаются бисфосфонаты;
- эндокринная коррекция: пациентам с задержкой полового развития и гипогонадизмом на фоне приёма глюкокортикостероидов может быть рекомендована заместительная терапия тестостероном.
- немедикаментозное лечение:
- респираторная поддержка: по мере прогрессирования дыхательной недостаточности, начиная с неамбулаторной стадии, применяются методики для облегчения откашливания (механические инсуффляторы-эксуффляторы), а затем — неинвазивная вентиляция лёгких в ночное или дневное время;
- нутритивная поддержка: при развитии дисфагии, аспирации или снижении массы тела организуется зондовое питание или устанавливается гастростома;
- физическая активность: рекомендуется регулярная, дозированная физическая активность и лечебная физкультура под контролем специалиста для поддержания мобильности и профилактики контрактур.
- хирургическое лечение: на амбулаторной стадии может выполняться пластика ахиллова сухожилия для коррекции эквиноварусной деформации стоп и улучшения ходьбы. На неамбулаторной стадии основным показанием к операции является прогрессирующий сколиоз (искривление более 20°), для коррекции которого выполняется спондилодез (артродез позвоночника).
- паллиативная помощь является неотъемлемой частью ведения пациентов с прогрессирующей МДД и направлена на улучшение качества жизни пациента и его семьи. Она включает купирование тягостных симптомов (боль, одышка), оказание психосоциальной и духовной поддержки и органично дополняет активное лечение. Оказание помощи часто осуществляется выездными патронажными бригадами.
Прогноз
Несмотря на современные достижения в области генной терапии и молекулярной биологии, МДД остаётся неизлечимым заболеванием. При естественном течении болезни средняя продолжительность жизни пациентов не превышает 25-30 лет. В 90 % случаев летальный исход связан с прогрессирующей дыхательной недостаточностью вследствие слабости дыхательной мускулатуры и развитием вторичных респираторных инфекций[1].
Диспансерное наблюдение
Основным принципом диспансерного наблюдения при МДД является мультидисциплинарное ведение пациентов с привлечением широкого круга специалистов: неврологов, кардиологов, пульмонологов, ортопедов, эндокринологов, реабилитологов, диетологов и психологов. Объём и частота контрольных обследований определяются индивидуально[6].
Профилактика
Профилактика вторичных осложнений при МДД основана на комплексном мультидисциплинарном подходе. Профилактика сердечно-сосудистых и дыхательных осложнений включает обязательные консультации профильных специалистов перед операциями и регулярную вакцинацию. Нутритивная поддержка направлена на коррекцию питания при начале терапии глюкокортикостероидами или выявлении дисфагии. Для сохранения мышечной функции и предотвращения контрактур применяется физическая терапия и дозированная активность. Важным направлением является профилактика остеопороза путём регулярного мониторинга состояния костной ткани и коррекции дефицита витамина D[10].
Примечания
- ↑ 1 2 Подклетнова Т. В., Кондакова О. Б., Увакина Е. В. и др. Клинический случай тяжёлого течения мышечной дистрофии Дюшенна, обусловленной нонсенс-мутацией в гене DMD, у девочки // Неврологический журнал имени Л.О. Бадаляна. — 2021. — Т. 2, № 4. — С. 227—232. — doi:10.46563/2686-8997-2021-2-4-227-232.
- ↑ 1 2 3 Ткачук Е. А., Барыкова Д. М., Семинский И. Ж. и др. Клинический случай миодистрофии Дюшенна // Байкальский медицинский журнал. — 2023. — Т. 2, № 2. — С. 45—52. — doi:10.57256/2949-0715-2023-2-45-52.
- ↑ Kamdar F., Garry D. Dystrophin-Deficient Cardiomyopathy (англ.) // Journal of the American College of Cardiology. — 2016. — Vol. 67, no. 21. — P. 2533—2546. — doi:10.1016/j.jacc.2016.02.081.
- ↑ Шумилова М. М. Мышечная дистрофия Дюшенна-Беккера (рус.). Генокарта - генетическая энциклопедия. (9 января 2020). Дата обращения: 21 декабря 2025.
- ↑ Okubo, M. Molecular genetics of dystrophinopathy (англ.) // Journal of Human Genetics. — 2025. — doi:10.1038/s10038-025-01357-7.
- ↑ 1 2 3 4 5 6 7 8 9 10 11 12 Анисимова И. В., Артемьева С. Б., Белоусова Е. Д., и др. Мышечная дистрофия Дюшенна: современные подходы к ведению и лечению пациентов // Педиатрическая фармакология. — 2023. — Т. 20, № 5. — С. 427—453. — doi:10.15690/pf.v20i5.2615.
- ↑ 1 2 Bez Batti Angulski A., Hosny N., Cohen H., и др. Duchenne muscular dystrophy: disease mechanism and therapeutic strategies (англ.) // Frontiers in Physiology. — 2023. — Vol. 14. — P. 1183101. — doi:10.3389/fphys.2023.1183101.
- ↑ 1 2 3 4 5 6 7 8 Do T. T. Muscular Dystrophy (англ.). Medscape (20 марта 2024). Дата обращения: 21 декабря 2025.
- ↑ 1 2 Venugopal V., Pavlakis S. Duchenne Muscular Dystrophy (англ.). Statpearls (10 июля 2023). Дата обращения: 21 декабря 2025.
- ↑ Darras B. T., Urion D. K., Ghosh P. S. Dystrophinopathies (англ.). GeneReviews (20 января 2022). Дата обращения: 21 декабря 2025.
Литература
- Bez Batti Angulski A., Hosny N., Cohen H. et al. Duchenne muscular dystrophy: disease mechanism and therapeutic strategies (англ.) // Frontiers in Physiology. — 2023. — Vol. 14. — P. 1183101. — doi:10.3389/fphys.2023.1183101.
- Анисимова И. В., Артемьева С. Б., Белоусова Е. Д. и др. Мышечная дистрофия Дюшенна: современные подходы к ведению и лечению пациентов // Педиатрическая фармакология. — 2023. — Т. 20, № 5. — С. 427—453. — doi:10.15690/pf.v20i5.2615.
- Ткачук Е. А., Барыкова Д. М., Семинский И. Ж. и др. Клинический случай миодистрофии Дюшенна // Байкальский медицинский журнал. — 2023. — Т. 2, № 2. — С. 45—52. — doi:10.57256/2949-0715-2023-2-45-52.