Миопатия Броди
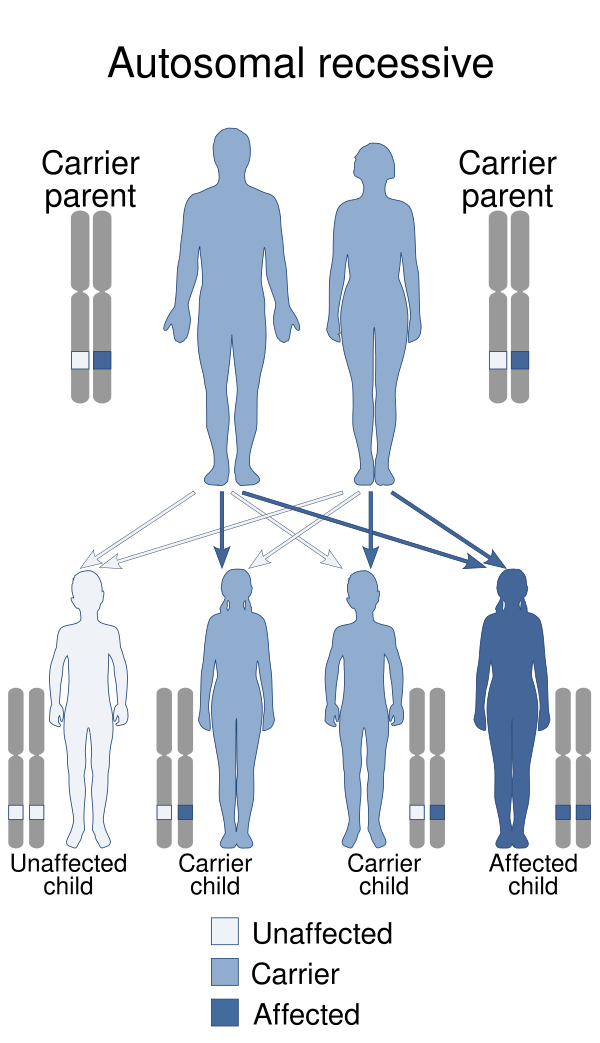
Миопати́я Бро́ди (МБ) — это редкое наследственное заболевание, передающееся по аутосомно-рецессивному типу, для которого характерны мышечные судороги и нарушение расслабления мышц после физической нагрузки, что проявляется в двигательной дисфункции. Патологический процесс затрагивает скелетную мускулатуру конечностей (рук и ног), а также мышцы, отвечающие за движение век. В основе заболевания лежат генетические дефекты, приводящие к нарушению кальциевого обмена в мышечных клетках. Ключевыми причинами являются мутации в гене ATP2A1, кодирующем белок кальциевую АТФазу-1 (SERCA1), либо нарушения в функции сарколипина — белка-регулятора активности этого же фермента[2].
Что важно знать
История
Первое клиническое описание выраженной мышечной скованности, возникающей при физической нагрузке и не сопровождающейся миотоническими разрядами на электромиографии, было представлено Броди в 1969 году. Патогенетическая основа этого фенотипа была установлена в 1986 году Карпати, обнаружившим дефицит белка SERCA1 в скелетных мышцах поражённых пациентов. Спустя десятилетие, в 1996 году, в двух независимых семьях был идентифицирован ответственный за заболевание ген ATP2A1[3].
Классификация
Этиология
МБ представляет собой редкую наследственную миопатию с аутосомно-рецессивным типом наследования. Этиология заболевания напрямую связана с мутациями в гене ATP2A1, который кодирует белок SERCA1 — кальциевую АТФазу 1-го типа саркоплазматического ретикулума. Данный генетический дефект приводит к нарушению функции этого транспортного белка, отвечающего за обратный захват ионов кальция в саркоплазматический ретикулум мышечных клеток после сокращения[3].
Патогенез
Патогенез заболевания обусловлен нарушением выведения ионов кальция из внутриклеточного пространства, что необходимо для расслабления мышцы. Белок SERCA играет ключевую роль в регуляции кальциевого гомеостаза в скелетных мышечных волокнах. После деполяризации сарколеммы дигидропиридиновый рецептор активирует рианодиновый рецептор 1-го типа. Это приводит к выбросу ионов кальция из саркоплазматического ретикулума в цитозоль, где они связываются с тропонином С, запуская каскад событий, ведущих к мышечному сокращению за счёт взаимодействия актина и миозина. Завершающим этапом цикла сокращения-расслабления является активный транспорт ионов кальция обратно в саркоплазматический ретикулум с помощью белка SERCA. Снижение цитоплазматической концентрации кальция вызывает расслабление мышцы[3][6].
При МБ мутации в гене ATP2A1 приводят к нарушению функции белка SERCA1. Это вызывает сбой в обратном захвате кальция, его задержку в цитозоле и, как следствие, стойкое напряжение и скованность мышц после их активности, что составляет суть патогенеза данного заболевания. Белок SERCA1, чья функция нарушена при МБ, экспрессируется исключительно в быстрых (тип II) мышечных волокнах. Именно поэтому характерная для заболевания мышечная скованность, провоцируемая физической нагрузкой, возникает преимущественно после фазовой активности — быстрых и интенсивных сокращений, выполняемых быстрыми волокнами. Напротив, тоническая активность, необходимая для поддержания позы и обеспечиваемая медленными волокнами, как правило, не вызывает подобных симптомов[3][6].
Эпидемиология
За все время в мировой литературе описано лишь около 33 семей с МБ, включающих 47 пациентов. Оценочная распространённость заболевания составляет примерно 1 случай на 10 миллионов человек, что подчёркивает его исключительную редкость[6].
Диагностика
Ключевым и обязательным симптомом заболевания является мышечная скованность (ригидность), провоцируемая физической нагрузкой. У большинства пациентов скованность возникает уже в начале выполнения упражнений. Наиболее часто в патологический процесс вовлекаются мышцы нижних конечностей, реже — верхних конечностей и век. Характерной особенностью является усиление симптомов при воздействии низких температур. Болевой синдром представлен мышечными судорогами (болезненными непроизвольными сокращениями) как во время нагрузки, так и в покое, а также миалгией, которая обычно носит распространённый характер. Субъективное ощущение мышечной слабости отмечает лишь часть пациентов[3].
При физикальном осмотре выявляется патогномоничный признак — замедленное расслабление мышц после их повторяющегося или длительного сокращения. Этот феномен чётко демонстрируется на веках. Мышечная атрофия для МБ не характерна. Напротив, у многих пациентов наблюдается атлетическое телосложение с развитой, иногда гипертрофированной мускулатурой. Перкуссионная миотония встречается редко, сухожильные рефлексы обычно сохранены. Несмотря на выраженную симптоматику, заболевание приводит в основном к лёгкой степени функциональных ограничений. Пациенты чаще всего испытывают затруднения при беге, быстром подъёме по лестнице и занятиях спортом[3].
При электромиографии характерным признаком является отсутствие миотонических разрядов на фоне наличия так называемых «немых контрактур»[3].
Исследование с повторной ритмической стимуляцией нерва выявляет характерный паттерн — так называемый псевдоинкремент, или признак Арзеля. Он проявляется увеличением амплитуды и одновременным уменьшением длительности вызванного моторного ответа (М-ответа) при сохранении стабильной площади под кривой. Этот феномен наиболее выражен и систематически наблюдается при стимуляции локтевого нерва с регистрацией ответа от мышцы, приводящей большой палец, а также от трапециевидной мышцы. Короткий и длинный нагрузочные тесты не вызывают значимых изменений вызванных моторных ответов[7].
Гистологическое исследование мышечной ткани выявляет характерный комплекс изменений. Наиболее частым и специфичным признаком является атрофия мышечных волокон второго типа, которая наблюдается у подавляющего большинства пациентов. При этом волокна первого типа, как правило, остаются сохранными. Отмечается значительное увеличение вариабельности размеров мышечных волокон. Ещё одним типичным гистологическим маркером является повышение количества внутренних ядер в мышечных волокнах. При длительном течении заболевания процент волокон с внутренними ядрами может нарастать, а сами ядра могут приобретать вытянутую форму. Дополнительным частым признаком служит изменение нормального распределения волокон. В большинстве биоптатов обнаруживается увеличение относительного процента быстрых волокон второго типа по сравнению с нормальными показателями для исследуемой мышцы. Признаки активного повреждения мышечной ткани, такие как некроз, дегенерация или регенерация волокон, наблюдаются редко и выражены минимально, что соответствует медленно прогрессирующему или стабильному характеру заболевания[3].
Иммуногистохимическое исследование позволяет визуализировать белок SERCA, причём в быстрых мышечных волокнах окрашивание преимущественно отражает содержание изоформы SERCA1. У половины пациентов отмечается выраженное снижение концентрации SERCA1 в мышечных волокнах второго типа при сохранной экспрессии в волокнах первого типа. В другой половине случаев иммуногистохимическое окрашивание на SERCA1 может оставаться нормальным. Содержание изоформы SERCA2 в большинстве исследованных биоптатов не изменено, лишь в единичных случаях наблюдается её компенсаторное увеличение. Иммуноблоттинг, направленный на количественную оценку содержания белка SERCA1, демонстрирует более однозначные результаты. Во всех случаях исследования выявляют значительное снижение или полное отсутствие этого белка в образцах мышечной ткани пациентов[3].
Молекулярно-генетический анализ методом секвенирования: позволяет выявить мутацию в гене ATP2A1. Среди выявленных мутаций преобладают миссенс-мутации, нонсенс-мутации, сдвиги рамки считывания, а также сплайсинг-мутации[3].
При МБ ключевым биохимическим дефектом является значительное снижение активности кальциевой АТФазы SERCA. При измерение АТФ-зависимого транспорта кальция в мембранных фракциях или Ca²⁺-зависимого гидролиза АТФ в гомогенатах мышц определяется выраженное падение активности фермента. Снижение активности составляет от 50 % до 80 % по сравнению с нормой[3].
Дифференциальная диагностика
Дифференциальная диагностика МБ проводится со следующими заболеваниями[3]:
- врождённые мышечные дистрофии;
- врождённые миастенические синдромы;
- глюкокортикоидная миопатия.
Осложнения
В редких случаях возможны серьёзные осложнения, связанные с нарушением кальциевого обмена: эпизоды рабдомиолиза после интенсивной нагрузки или общей анестезии, а также состояния, сходные с злокачественной гипертермией[3].
Лечение
Эффективного патогенетического лечения МБ не существует. Все применяемые терапевтические подходы носят исключительно симптоматический характер и имеют ограниченную эффективность. Для облегчения основных симптомов — мышечной скованности, судорог и миалгии — в клинической практике применяются различные препараты: верапамил, дантролен, мексилетин, карбамазепин, нифедипин, ацетазоламид, ибупрофен и миорелаксанты. Верапамил и дантролен, воздействующие на кальциевые каналы (дигидропиридиновые и рианодиновые рецепторы), теоретически являются наиболее эффективным, однако их применение часто ограничивается побочными эффектами. По имеющимся данным, лишь у единичных пациентов медикаментозная терапия приводила к значимому и долгосрочному улучшению состояния. Приблизительно половина пациентов не нуждается в постоянном лечении, что отражает вариабельную тяжесть симптомов и адаптацию пациентов к своему состоянию. Перспективы создания эффективной терапии связаны с изучением молекулярных механизмов болезни на животных моделях, которые являются ключевым инструментом для поиска новых потенциальных лекарственных мишеней[3][6].
Прогноз
Прогноз МБ в долгосрочной перспективе обычно благоприятный. У большинства пациентов состояние остаётся стабильным на протяжении многих лет. У части больных может отмечаться медленное прогрессирование с усилением скованности, болей и судорог, однако объективного нарастания мышечной слабости или развития атрофии, как правило, не происходит[3].
Диспансерное наблюдение
Профилактика
Не разработана.
Примечания
Литература
- Masingue M., Arzel M., Sternberg D. et al. Brody myopathy demonstrates a pseudo-increment on repetitive nerve stimulation (англ.) // Muscle and Nerve. — 2020. — April (vol. 61, no. 4). — P. 491—495. — doi:10.1002/mus.26809.
- Şahin A., Badakal E. Z. D., Kovancılar Koç M. et al. Case report: Revealing the rare-a Brody Disease patient from Turkey expanding the phenotype (англ.) // Frontiers in Genetics. — 2023. — 30 November (vol. 14). — P. 1289312. — doi:10.3389/fgene.2023.1289312.
- Molenaar J. P., Verhoeven J. I., Rodenburg R. J. et al. Clinical, morphological and genetic characterization of Brody disease: an international study of 40 patients (англ.) // Brain. — 2020. — 1 February (vol. 143, no. 2). — P. 452—466. — doi:10.1093/brain/awz410.
- Зырянова Т. Ю. Изучение молекулярных механизмов регуляции фенотипа скелетных мышечных волокон как теоретический подход к лечению миопатий // Вестник Санкт-Петербургского университета. Медицина. — 2014. — № 1.