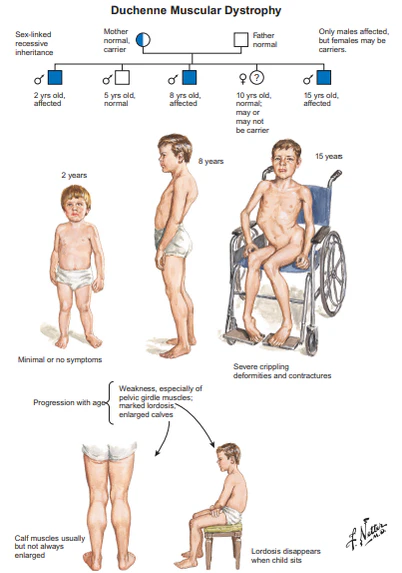
Дистрофинопатии
Дистрофинопати́и — это группа Х-сцепленных рецессивных нервно-мышечных заболеваний, вызванных патогенными мутациями в гене DMD и дефицитом белка дистрофина. Клинический континуум варьирует от лёгких форм (бессимптомная гиперферментемия, мышечные судороги) до тяжёлых прогрессирующих заболеваний. Классические формы включают мышечную дистрофию Дюшенна (раннее начало, быстрое прогрессирование, почти полное отсутствие дистрофина), мышечную дистрофию Беккера (более позднее начало, медленное течение, наличие частично функционального дистрофина) и ассоциированную с DMD дилатационную кардиомиопатию (первичное поражение сердца). Промежуточные по тяжести случаи классифицируются как интермединная мышечная дистрофия[1][2].
История
История изучения мышечной дистрофии Дюшенна начинается с первых детальных описаний болезни Мерьоном (1852) и Дюшенном (1868), который выявил жирово-фиброзное замещение мышц и чьим именем впоследствии была названа болезнь. В 1886 году Гауэрс описал характерный способ вставания с пола («приём Гауэрса»). Причина заболевания оставалась неизвестной более века, пока в 1986 году лаборатория Луи Кункела не идентифицировала ответственный ген DMD, а в 1987-м не доказала, что мутации в нём приводят к отсутствию белка дистрофина. Эти открытия заложили основу для современной диагностики, генетического тестирования и создания моделей заболевания, значительно ускорив понимание МДД за последние 30 лет[3].
Классификация
В понятие дистрофинопатий входят мышечная дистрофия Дюшенна, мышечная дистрофия Беккера и DMD-ассоциированная дилатационная кардиомиопатия[2].
Этиология
Этиология заболевания заключается в патогенных вариантах гена DMD, расположенного на Х-хромосоме. Этот ген, один из крупнейших в геноме человека, охватывает около 2.2 млн пар нуклеотидов и содержит 79 экзонов. Мутации в нём приводят к нарушению синтеза или функции белка дистрофина. Спектр патогенных вариантов чрезвычайно широк и включает крупные делеции одного или нескольких экзонов (60–70 % случаев), дупликации (5–10 %), а также точечные варианты — однонуклеотидные замены, малые делеции и инсерции и мутации сайтов сплайсинга. Ключевым фактором, определяющим тяжесть фенотипа, является сохранение рамки считывания: делеции или дупликации, приводящие к её сдвигу и образованию преждевременного стоп-кодона, обычно ассоциированы с тяжёлой формой мышечной дистрофии Дюшенна (почти полным отсутствием белка), тогда как мутации, сохраняющие рамку считывания, приводят к синтезу частично функционального дистрофина и более мягкому фенотипу мышечной дистрофии Беккера. Мутации преимущественно сгруппированы в двух основных «горячих точках» рекомбинации в гене: проксимальной (экзоны 2–20) и дистальной (экзоны 44–53). Нонсенс-мутации чаще встречаются при мышечной дистрофии Дюшенна[1].
Патогенез
Патогенез заболевания обусловлен дефицитом или структурными аномалиями белка дистрофина, который играет ключевую структурную роль в мышечной клетке. Дистрофин, расположенный под сарколеммой, выполняет функцию молекулярного «амортизатора» и связующего звена: его N-конец связывается с внутриклеточными актиновыми филаментами, а C-конец через цистеин-богатый домен соединяется с трансмембранным белковым комплексом (дистрогликановым и саркогликановым комплексами), который, в свою очередь, заякорен во внеклеточном матриксе (в основном на ламинине). Эта дистрофин-ассоциированная гликопротеиновая система обеспечивает механическую стабильность сарколеммы во время сокращения мышцы[4][5].
При мутациях в гене DMD, нарушающих рамку считывания (нонсенс-мутации, делеции или дупликации со сдвигом рамки), синтезируется сильно укороченный нефункциональный белок или белок вообще отсутствует. Это приводит к полному распаду всего дистрофин-гликопротеинового комплекса. В результате сарколемма становится хрупкой и подверженной механическим повреждениям при сокращении. Повреждение мембраны вызывает аномальный приток ионов кальция внутрь клетки, что активирует кальций-зависимые протеазы и фосфолипазы, запускает оксидативный стресс и в конечном итоге приводит к некрозу миоцита. Организм пытается компенсировать гибель мышечных волокон за счёт регенерации из сателлитных клеток, однако с течением времени регенеративный потенциал истощается. Повторяющиеся циклы некроза и частичной регенерации постепенно приводят к потере мышечной ткани и её замещению жировой и соединительной тканью (фиброзно-жировая дистрофия). Внешне это может проявляться псевдогипертрофией (увеличением объёма мышц, особенно икр, за счёт разрастания жировой и фиброзной ткани), тогда как функционально мышечная масса и сила прогрессивно снижаются[4].
На микроскопическом уровне патогенез проявляется характерными изменениями. На ранних стадиях заболевания наблюдается распространённый некроз мышечных волокон с их расщеплением. Среди погибающих миоцитов визуализируются «клетки-призраки» — остатки мембран ранее здоровых волокон. В зонах активного процесса отмечается инфильтрация некротизированных волокон воспалительными клетками. Сохранившиеся мышечные волокна демонстрируют значительный разброс в размерах и часто содержат смещённые в центр ядра. По мере прогрессирования заболевания макрофаги очищают область от погибших клеток, а мышечная ткань постепенно замещается жировыми клетками и элементами соединительной ткани. Этот процесс придаёт мышцам обманчиво увеличенный объём, что особенно заметно в области икр и предплечий[4].
Эпидемиология
Мышечная дистрофия Дюшенна является наиболее распространённой формой мышечной дистрофией с дебютом в детском возрасте, её распространённость составляет около 63 случаев на 1 млн населения. Мышечная дистрофия Беккера встречается реже, с распространённостью около 24 случаев на 1 млн. Примерно одна треть случаев возникает вследствие спонтанных мутаций, остальные наследуются по Х-сцепленному рецессивному типу. Дистрофинопатии почти исключительно поражают лиц мужского пола в силу Х-сцепленного типа наследования. В редких случаях у женщин-носительниц мутации может развиваться клиническая картина болезни из-за неравномерной инактивации здоровой Х-хромосомы. Также фенотип мышечной дистрофии Дюшенна может проявляться у женщин с синдромом Тёрнера, унипарентальной дисомией или транслокациями между Х-хромосомой и аутосомами[4].
Диагностика
Слабость при дистрофинопатиях носит симметричный и прогрессирующий характер с чёткой закономерностью: в первую очередь и в большей степени страдают проксимальные мышцы, особенно нижних конечностей (тазовый пояс, мышцы бёдра), а также разгибатели шеи, разгибатели запястья, квадрицепсы, передние большеберцовые мышцы, бицепсы и трицепсы. Мышцы-антогонисты (разгибатели шеи, сгибатели запястья, дельтовидные, мышцы задней поверхности бёдра, икроножные и камбаловидные) поражаются позже и в меньшей степени. Сухожильные рефлексы постепенно угасают параллельно потере мышечных волокон. Ключевыми симптомами являются[4]:
- псевдогипертрофия икр — классический, но обманчивый признак, обусловленный не истинным ростом мышц, а замещением мышечной ткани жировой и фиброзной. Она может также наблюдаться в области предплечий и языка. Отчасти увеличение объёма икр может быть компенсаторным из-за ранней слабости передних большеберцовых мышц;
- контрактуры развиваются закономерно: к 10 годам у 70 % пациентов формируются контрактуры подвздошно-большеберцового тракта, сгибателей бёдра и ахилловых сухожилий. Потеря способности к ходьбе и иммобилизация образуют порочный круг, усугубляющий развитие контрактур;
- сколиоз, который является следствием асимметричной слабости паравертебральных;
- дыхательные нарушения, которые связаны со слабостью дыхательной мускулатуры. Невозможность совершить эффективный кашлевой толчок ведёт к ателектазам и рецидивирующим пневмониям.
При мышечной дистрофии Беккера слабость развивается медленнее (дебют часто в 10–20 лет) и прогрессирует мягче. Псевдогипертрофия икр и контрактуры не являются обязательными признаками. Ключевое отличие — сохранение способности к самостоятельной ходьбе: если большинство больных мышечной дистрофией Дюшенна большинство к 10-12 годам нуждаются в инвалидном кресле, то при мышечной дистрофии Беккера многие ходят самостоятельно до 4–го десятилетия жизни, а некоторые — до 6–7-го[4].
Течение дистрофинопатий характеризуется прогрессирующей этапностью[4]:
- стадия 1 — пресмптоматическая: протекает без явных клинических признаков;
- стадия 2 — ранняя амбулаторная (возраст 2–6 лет): манифестация болезни проявляется «утиной» (раскачивающаяся) походкой вследствие слабости мышц тазового пояса. Прогрессирует слабость проксимальной мускулатуры ног. Характерен симптом Говерса — ребёнок «взбирается по себе», опираясь на бёдра, чтобы встать с пола. Возможна ходьба на носках. Способность ходить и подниматься по лестнице сохранена;
- стадия 3 — поздняя амбулаторная (примерно с 8 лет): нарастают трудности при ходьбе, подъём по лестнице становится невозможным, ребёнок не может встать с пола. Начинается медленное, но неуклонное снижение силы дыхательных мышц и жизненной ёмкости лёгких, что может проявляться симптомами ночной гипоксемии (вялость, утренние головные боли).
- стадия 4 — ранняя неамбулаторная: пациент теряет способность к самостоятельной ходьбе, но может какое-то время самостоятельно передвигать инвалидную коляску и удерживать осанку. Начинает формироваться сколиоз.
- стадия 5 — поздняя неамбулаторная: прогрессирует сколиоз и дыхательная недостаточность. Формируются контрактуры суставов. На первый план выходят кардиальные осложнения (дилатационная кардиомиопатия, сердечная недостаточность) и терминальная дыхательная недостаточность.
Иные проявления дистрофинопатий включают когнитивные и поведенческие расстройства встречаются у значительной части пациентов (до 30 %). Средние показатели IQ примерно на 1 стандартное отклонение ниже популяционной нормы. Типичны задержка речевого развития, трудности обучения, синдром дефицита внимания и гиперактивности, расстройства аутистического спектра. Особенно страдают вербальные навыки и обработка сложной речевой информации[4].
Рентгенография применяется для выявления характерных костно-мышечных и респираторных осложнений дистрофинопатий[4]:
- позвоночник: метод позволяет оценить прогрессирующий сколиоз;
- кости: могут обнаруживаться признаки остеопороза и остеопении, а также последствия патологической хрупкости костей — компрессионные переломы тел позвонков и переломы длинных трубчатых костей (часто бедренных);
- органы грудной клетки: при развитии дыхательной недостаточности на снимках могут визуализироваться признаки рестриктивного поражения лёгких (высокое стояние куполов диафрагмы, узкие межреберья), ателектазы и инфильтративные изменения при рецидивирующих пневмониях.
Электромиография: характерными изменениями являются короткие по продолжительности, часто полифазные потенциалы двигательных единиц с вариабельной (от нормальной до сниженной) амплитудой и ранний их рекрутимент при минимальном усилии. В активной фазе болезни, вследствие некроза регистрируется спонтанная активность в виде фибрилляций и положительных острых волн, свидетельствующих о денервации мышечных волокон. При тяжёлой потере мышечной массы картина может имитировать нейрогенное поражение, однако отличающаяся сниженной амплитудой и площадью одиночных потенциалов[4].
Электрокардиография: метод позволяет выявить характерные изменения, такие как глубокие зубцы Q (чаще в отведениях I, aVL, V5-V6) и увеличенная амплитуда зубцов R в правых грудных отведениях (V1-V2), что может свидетельствовать о гипертрофии миокарда левого желудочка и фиброзе заднебазальных сегментов. Также метод позволяет диагностировать нарушения ритма[4].
Эхокардиография: типичными находками являются дилатационная кардиомиопатия с расширением полостей (преимущественно левого желудочка), снижение фракции выброса, а также нарушения диастолической функции (замедленная релаксация) даже при сохранной систолической функции на ранних стадиях. Часто выявляются зоны гипокинеза[4].
Холтеровское мониторирование: используется для выявления пароксизмальных нарушений ритма сердца, которые могут не регистрироваться на стандартной электрокардиографии[4].
Магнитно-резонансная томография сердца: используется для выявления и количественной оценки фиброза миокарда[4].
Биохимический анализ крови: характерно повышение активности кретинкиназы[6].
Иммунногистохимический анализ мышечных биоптатов: при мышечной дистрофии Дюшенна иммунореактивность к дистрофину резко ослаблена или полностью отсутствует у подавляющего большинства мышечных волокон; при мышечной дистрофии Беккера картина более вариабельна — обычно наблюдается непрерывное, но часто ослабленное и неравномерное окрашивание сарколеммы, что соответствует наличию структурно изменённого, но частично функционального белка. У бессимптомных носительниц мутации может выявляться мозаичная картина, где часть волокон окрашивается нормально, а часть — снижено или отсутствует. Верификацию и уточнение молекулярной массы белка проводят с помощью иммуноблоттинга, который при мышечной дистрофии Дюшенна обычно выявляет отсутствие полноразмерного дистрофина, а при мышечной дистрофии Беккера — наличие белка с аномальной молекулярной массой[6].
Молекулярно-генетический анализ[6]:
- мультиплексная амплификация лигированных зондов — широко применяемый метод для детекции делеций или дупликаций одного или нескольких экзонов, которые составляют до 70 % всех патогенных вариантов. Он позволяет анализировать все 79 экзонов гена, но не определяет точечные мутации;
- выявление точечных мутаций: используются различные методы анализа полиморфизма конформации одноцепочечной или двуцепочечной ДНК, денатурирующий градиентный гель-электрофорез. При обнаружении аномальной подвижности ПЦР-продукта его направляют на прямое секвенирование по Сэнгеру для идентификации конкретного нуклеотидного изменения;
- секвенирование нового поколения: позволяет одновременно выявить как крупные экзонные делеции и дупликации, так и точечные мутации во всём гене, включая интронные участки, важные для сплайсинга. Комбинация мультиплексной амплификации лигированных зондов и секвенирования нового поколения считается эффективным подходом для полного анализа гена DMD.
Дифференциальная диагностика
Дифференциальная диагностика дистрофинопатий проводится со следующими заболеваниями[1]:
- поясно-конечностные мышечные дистрофии представляют собой группу аутосомно-рецессивных и аутосомно-доминантных заболеваний, клинически сходных с дистрофинопатиями, но поражающих лиц обоего пола. Причина — мутации в генах, кодирующих саркогликаны и другие белки сарколеммы, взаимодействующие с дистрофином;
- мышечная дистрофия Эмери — Дрейфуса характеризуется классической триадой: контрактуры суставов (возникают в детстве), медленно прогрессирующая мышечная слабость (начинается с плече-перонеальной мускулатуры, затем распространяется на поясные мышцы) и вовлечение сердца (аритмии, сердечная недостаточность). Возраст начала и тяжесть варьируются. Контрактуры развиваются в первые два десятилетия, за ними следует мышечная слабость. Кардиальные проявления обычно появляются после 20 лет. Заболевание может наследоваться Х-сцепленно (гены EMD, FHL1) или аутосомно-доминантно/рецессивно (ген LMNA).
- спинальная мышечная атрофия проявляется мышечной гипотонией и слабостью при сохранности мимической и глазодвигательной мускулатуры. Характерны признаки поражения мотонейронов передних рогов спинного мозга: фасцикуляции языка и отсутствие сухожильных рефлексов. Слабость симметричная, проксимальная, прогрессирующая. Типичны задержка роста, рестриктивные нарушения дыхания, сколиоз и контрактуры. Болезнь наследуется аутосомно-рецессивно и вызывается патогенными вариантами в гене SMN1.
- дилатационная кардиомиопатия может быть как семейной, так и ненаследственной. Семейные формы чаще наследуются аутосомно-доминантно (80-90 % случаев), реже — Х-сцепленно или аутосомно-рецессивно;
- синдром Барта — это Х-сцепленное заболевание, обусловленное мутацией в гене TAFAZZIN. У поражённых мальчиков характерна триада: кардиомиопатия (чаще дилатационная или с некомпактным миокардом, манифестирует до 5 лет), нейтропения и скелетная миопатия. Также отмечаются задержка роста в препубертате (с последующей «компенсаторной» скачкообразной прибавкой), характерные черты лица.
Осложнения
К возможным осложнениям дистрофинопатий относятся кардиомиопатия и респираторные осложнения (рестриктивная дыхательная недостаточность, неэффективный кашель с риском ателектазов и пневмоний, ночная гиповентиляция с гипоксемией)[1]
Лечение
Основные направления терапии дистрофинопатий включают как стандартную патогенетическую и симптоматическую терапию, так и инновационные генетические и клеточные подходы[7]:
- глюкокортикостероиды (преднизолон, дефлазакорт, ваморолон) остаются стандартом лечения. Они эффективно замедляя потерю мышечной силы и двигательных функций, отсрочивая утрату ходьбы на 1-3 года и оказывая положительное влияние на дыхательную и сердечную-сосудистую системы;
- среди нестероидных противовоспалительных препаратов применяется ингибитор гистондеацетилазы (гивиностат), замедляющий фиброз и прогрессирование болезни. Также исследуются перспективные препараты, такие как миозин-ингибитор севасемтен (для снижения гиперконтрактильности мышц) и модулятор сателлитных клеток SAT-3247 (для восстановления регенерации мышечной ткани);
- генетическая модуляция представлена двумя основными стратегиями: терапия пропуска экзона с использованием антисмысловых олигонуклеотидов (этеплирсен, голодирсен, вилтоларсен, казимерсен) восстаналивает рамку считывания мРНК у пациентов с определёнными делециями, приводя к синтезу частично функционального дистрофина;
- прорывным направлением является генная терапия, заключающаяся во внутривенном введении с помощью аденоассоциированного вирусного вектора гена, кодирующего усечённый дистрофин (микродистрофин). Первый одобренный препарат, деландистроген моксепарвовек, демонстрирует умеренное замедление прогрессирования. Однако его применение ограничивают иммунные реакции, риск серьёзных побочных эффектов (миокардит, гепатотоксичность), неполное распределение гена в тканях и недоказанность долгосрочного эффекта на сердце;
- технология редактирования генома (CRISPR-Cas9), теоретически способная к полному излечению путём коррекции мутации в ДНК, пока находится на доклинической стадии. Первое клиническое испытание было остановлено после тяжёлой иммунной реакции и летального исхода у пациента;
- важнейшим компонентом комплексного лечения является кардиопротекторная терапия: для лечения и профилактики жизнеугрожающей кардиомиопатии применяются ингибиторы АПФ или блокаторы рецептора ангиотензина и антагонисты альдостерона (эплеренон, спиронолактон), которые замедляют развитие фиброза миокарда.
Прогноз
Прогноз при дистрофинопатиях определяется не только поражением скелетной мускулатуры, но и вовлечением других систем, где экспрессируется дистрофин: сердца, головного мозга и гладкой мускулатуры[4]:
- при мышечной дистрофии Дюшенна прогноз неблагоприятный, заболевание остаётся инкурабельным со 100 % летальностью. Ключевые причины смертности — кардиореспираторные осложнения. Прогрессирующий фиброз миокарда приводит к дилатационной кардиомиопатии, сердечной недостаточности, а также жизнеугрожающим аритмиям. Слабость дыхательных мышц, усугубляемая сколиозом, вызывает рецидивирующие пневмонии и терминальную дыхательную недостаточность. Дисфункция гладкой мускулатуры желудочно-кишечного тракта на фоне отсутствия дистрофина и гиподинамии приводит к нарушению моторики, запорам, диарее и нарушениям нутритивного статуса.
- при мышечной дистрофии Беккера прогноз вариабелен и в целом значительно лучше. Фенотипический спектр широк: некоторые пациенты теряют способность к ходьбе уже к 20 годам, другие сохраняют её до 70 лет. Возраст манифестации двигательных нарушений обычно наступает как минимум на десятилетие позже. После перехода на коляску пациенты также подвержены риску типичных осложнений иммобилизации: сколиоза, контрактур, пролежней и ухудшения функции лёгких. Кардиомиопатия является частым и серьёзным осложнением, причём клиническую картину могут определять нарушения проводимости, требующие медикаментозной терапии, имплантации кардиовертера-дефибриллятора или даже рассмотрения вопроса о трансплантации сердца. При наиболее лёгких формах заболевания пациенты могут иметь почти нормальную продолжительность жизни.
Диспансерное наблюдение
Диспансерное наблюдение дистрофинопатий требеют комплексного междисциплинарного подхода, включающего регулярный мониторинг и лечение осложнений со стороны различных систем органов[7]:
- сердечно-сосудистая система: регулярный кардиологический скрининг (эхокардиография, магнитно-резонансная томография сердца) для раннего выявления и лечения кардиомиопатии;
- дыхательная система: спирометрия используется для своевременного начала респираторной поддержки;
- опорно-двигательный аппарата: наблюдение за развитием сколиоза и контрактур. Оценка плотности костей (денситометрия) и концентрации витамина D, особенно на фоне терапии глюкокортикостероидами;
- эндокринная система: мониторинг задержки роста и полового созревания, связанных с болезнью и лечением глюкокортикостероидами;
- нервная система: оценка когнитивных функций, поведения для психолого-педагогической поддержки.
Профилактика
Профилактика вторичных осложнений дистрофинопатий требует комплексного подхода, направленного на кардиореспираторную систему, нутритивный статус и опорно-двигательный аппарат[1]:
- кардиореспираторная профилактика включает обязательную консультацию пульмонолога и кардиолога перед любыми хирургическими вмешательствами, а также регулярную вакцинацию против пневмококковой инфекции и гриппа для снижения риска тяжёлых респираторных инфекций;
- нутритивная поддержка необходима при планировании начала терапии кортикостероидами, наличии дисфагии, хронических запоров, планировании обширной операции или при выявлении признаков недостаточного питания. Оценка проводится диетологом;
- поддержка мышечной функции и подвижности осуществляется с помощью физической терапии для сохранения объёма движений и предотвращения контрактур. Пациентам находящимся на ранней неамбулаторной стадии рекомендуется регулярная щадящая физическая активность, такая как плавание и рекреационные упражнения, для профилактики атрофии мышц;
- профилактика остеопороза и переломов включает регулярный мониторинг костного здоровья. Лабораторная оценка включает определение уровня кальция, фосфора, щелочной фосфатазы и 25-гидроксивитамина D в сыворотке крови, а также клинический анализ мочи. Инструментальная диагностика состоит из проведения денситометрии исходно (с 3 лет или при начале приёма кортикостероидов) и далее ежегодно у пациентов группы риска (приём глюкокортикостероидов, переломы в анамнезе).
Примечания
Литература
- Keselman D. J., Brandsema J. F. Update on Treatment of Dystrophicopathy (англ.) // Current Treatment Options in Neurology. — 2025. — Vol. 27. — P. 27. — doi:10.1007/s11940-025-00841-x.
- Angelini C., Saad F. A., Siciliano G. Advances in Dystrophinopathy Diagnosis and Therapy (англ.) // Biomolecules. — 2023. — Vol. 13, no. 9. — P. 1319. — doi:10.3390/biom13091319.
- Доронин В.Б., Доронина О.Б. Наследственные мышечные дистрофии // Бюллетень сибирской медицины. — 2009. — № 3—2.