Мышечная дистрофия
Мы́шечная дистрофи́я (от др.-греч. μῦς — «мышца» и δυστροφία — «расстройство питания, истощение») — группа наследственных прогрессирующих заболеваний, характеризующихся первичным поражением скелетной мускулатуры, проявляющимся постепенной мышечной слабостью, атрофией и дегенерацией мышечных волокон при сохранности чувствительности и интеллекта[1]. Заболевания этой группы различаются по возрасту начала, темпам прогрессирования и степени вовлечения различных мышечных групп[1]. В отдельных формах могут наблюдаться нарушения со стороны сердца, дыхательной и эндокринной систем[2][3].
Общие сведения
| Мышечная дистрофия | |
|---|---|
| Специальность | Педиатрия, медицинская генетика |
| Симптомы | Резкая слабость, разрушение скелетной мышечной ткани, затруднения при ходьбе[1][2] |
| Продолжительность | Длительное время[1] |
| Типы | более 30, включая дистрофию Дюшенна, мышечную дистрофию Беккера, фациоскапуло-гуморальную мышечную дистрофию, поясно-конечностную мышечную дистрофию, миотоническую дистрофию[1][2] |
| Причины | Генетическое (X-сцепленное рецессивное наследование заболеваний, аутосомно-рецессивное или аутосомно-доминантное)[2] |
| Метод диагностики | Анализы крови, генетический анализ[2] |
| Лечение | Физиотерапия, ортопедические браслеты, коррекционная хирургия, вспомогательная вентиляция[1][2] |
| Прогноз | Зависит от вида[1] |
История
Впервые мышечная дистрофия была описана в 1830 году Чарлзом Беллем[2]. В 1860-х годах в медицинских журналах начали появляться описания случаев, когда мальчики постепенно теряли силы, не могли ходить и умирали в раннем возрасте. В следующем десятилетии французский невролог Гийом Дюшен опубликовал подробный отчёт о наиболее распространённой и тяжёлой форме этого заболевания, которое впоследствии было названо в его честь[1].
В 1966 году в США и Канаде Джерри Льюис и Ассоциация по борьбе с мышечной дистрофией начали ежегодную телепередачу, посвящённую Дню труда, «Телемарафон Джерри Льюиса», который сыграл важную роль в повышении осведомлённости о мышечной дистрофии в Северной Америке. Некоторые защитники прав инвалидов раскритиковали телемарафон за то, что он изобразил жертв этого заболевания как заслуживающих жалости, а не уважения[4].
18 декабря 2001 года в Соединённых Штатах был подписан Закон о медицинском обслуживании. Этот закон вносит поправки в Закон о службе общественного здравоохранения для проведения исследований по различным видам мышечной дистрофии и учреждает Координационный комитет по мышечной дистрофии, который помогает сосредоточить исследовательские усилия на согласованной исследовательской стратегии[5][6].
Классификация
В группу мышечных заболеваний входят тридцать различных генетических нарушений, которые обычно делят на девять основных категорий и видов[1][2]. Самый распространённый вид заболевания — мышечная дистрофия Дюшенна, которая в основном поражает ткани у мужского пола, начиная с четырёхлетнего возраста[1]. В другие виды заболеваний входят: мышечная дистрофия Беккера, фациоскапуло-гуморальная мышечная дистрофия, поясно-конечностная мышечная дистрофия и миотоническая дистрофия[1]. Они вызваны мутациями в генах, которые участвуют в производстве мышечных белков[2]. Это может произойти либо из-за наследственных заболеваний от родителей, либо из-за мутации, возникшей во время развития раннего возраста[2]. Заболевания могут быть вызваны Х-сцепленным рецессивным, аутосомно-рецессивным или аутосомно-доминантным типом наследования[2][3].
| Название заболевания | Phenotype MIM-номер | Ген | Тип наследования | Возраст начала | Поражаемые мышцы | Клиническая характеристика |
|---|---|---|---|---|---|---|
| Мышечная дистрофия Беккера | 300376 | DMD | Х-сцепленный рецессивный | Детский | Дистальные отделы конечностей с последующим генерализованным поражением | Более лёгкая форма по сравнению с дистрофией Дюшенна, преимущественно у мальчиков. Характеризуется медленным прогрессированием мышечной слабости |
| Врождённая мышечная дистрофия | Множественные | Множественные | Аутосомно-рецессивный /
Аутосомно-доминантный |
С рождения | Генерализованная слабость | Проявляется генерализованной мышечной слабостью, возможны контрактуры суставов. Прогрессирование медленное, продолжительность жизни снижена. Различные формы заболевания могут сопровождаться поражением головного мозга (лизэнцефалия, гидроцефалия) и других органов. Дефекты часто связаны с нарушением структуры белков, взаимодействующих с дистрофин-гликопротеиновым комплексом |
| Мышечная дистрофия Дюшенна | 310200 | DMD | Х-сцепленный рецессивный | Детский | Дистальные мышцы с прогрессирующим вовлечением дыхательной мускулатуры | Мышечная дистрофия Дюшенна — это заболевание, составляющее около половины случаев мышечной дистрофии, поражающее при рождении одного из 5000 мальчиков[2]. Наиболее частая форма мышечной дистрофии у детей, преимущественно у мальчиков. Характеризуется прогрессирующей мышечной атрофией, появлением симптомов при начале ходьбы. К 10 годам требуется ортопедическая поддержка, к 12 — утрата способности к самостоятельной ходьбе. Продолжительность жизни — 15—45 лет. Часто возникают спорадические мутации |
| Дистальная мышечная дистрофия | 254130 | DYSF | Аутосомно-рецессивный /
Аутосомно-доминантный |
20-60 лет | Дистальные мышцы кистей, предплечий и голеней | Медленно прогрессирующее заболевание, не угрожающее жизни. Миопатия Миёси — форма дистальной дистрофии с начальной слабостью икроножных мышц, связана с дефектами того же гена, что и одна из форм поясно-конечностной дистрофии |
| Мышечная дистрофия Эмери — Дрейфуса | Множественные | Множественные | Х-сцепленный, Аутосомно-рецессивный /
Аутосомно-доминантный |
Детство или подростковый возраст | Дистальные мышцы, мышцы плечевого и тазового пояса, сердечная мускулатура | Проявляется слабостью и атрофией мышц, начиная с дистальных отделов конечностей и распространяющейся на мышцы пояса. Часто сопровождается нарушениями сердечной проводимости и аритмиями |
| Фациоскапулогумеральная (лицево-лопаточно-плечевая) мышечная дистрофия | 158900 | DUX4 | Аутосомно-доминантный | Подростковый | Мышцы лица, плечевого пояса и верхних конечностей | Прогрессирующая слабость, вначале — лицевые и плечевые мышцы, затем — другие группы. У 20 % больных к 50 годам развивается выраженная инвалидизация с необходимостью коляски. До 30 % случаев — спорадические мутации. У женщин течение обычно мягче |
| Поясно-конечностная мышечная дистрофия | Множественные | Множественные | Аутосомно-рецессивный /
Аутосомно-доминантный |
Любой | Мышцы плечевого и тазового пояса | Характеризуется слабостью проксимальных мышц. Большинство пациентов сохраняют возможность самостоятельного передвижения, однако возможны редкие кардиопульмональные осложнения. |
| Миотоническая дистрофия | 160900, 602668 | DMPK, CNBP | Аутосомно-доминантный | Взрослый | Скелетные, сердечные и другие группы мышц | Проявляется миотонией (замедленным расслаблением мышц), мышечной атрофией и слабостью. Характерно системное поражение — сердечно-сосудистой, эндокринной и зрительной систем. Тяжесть и клинические проявления варьируют. |
| Окулофарингеальная мышечная дистрофия | 164300 | PABPN1 | Аутосомно-доминантный и реже аутосомно-рецессивный | 40—50 лет | Мышцы глаз, лица, глотки, плечевого пояса | Проявляется слабостью мышц глаз, лица и глотки, затруднением глотания и поднятия век. Возможна медленная прогрессия с вовлечением тазового пояса |
Этиология и патогенез
В большинстве случаев мышечная дистрофия имеет наследственную природу. Различные типы этого заболевания передаются по-разному: некоторые из них связаны с Х-хромосомой, другие — с аутосомно-рецессивным или аутосомно-доминантным наследованием. Однако у небольшого числа пациентов причиной болезни может стать новая, спонтанная мутация[7][8].
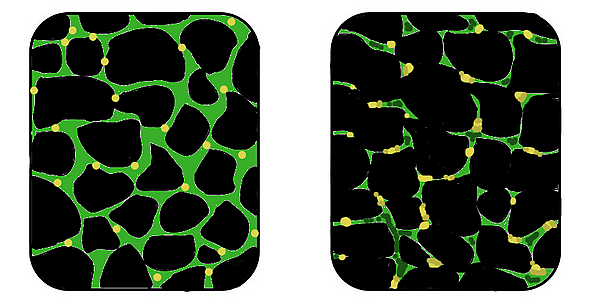
Гены представляют собой участки ДНК, расположенные в хромосомах. При мутациях в гене синтезируемый белок может становиться дефектным или вовсе не образовываться. В мышечной ткани это приводит к нарушению работы мышечных клеток, что проявляется клиникой мышечной дистрофии — прогрессирующей слабостью и утомляемостью. Мышца по своей структуре состоит из пучков мышечных волокон, представляющих собой специализированные клетки. Группы белков, расположенные вдоль мембран, окружающих каждое волокно, и вне клеток, помогают поддерживать нормальное функционирование мышечных клеток. Если один из этих белков утрачивается или повреждается (из-за мутации в гене, который его кодирует), это может стать причиной развития одной из форм мышечной дистрофии[3][8].
Различные формы врождённой мышечной дистрофии возникают из-за дефектов в белках, которые находятся либо в самой мембране мышечных клеток, либо за её пределами (фукутин и интегрин), либо во внеклеточном матриксе, который прилегает к мембране (мерозин или ламинин-альфа-2). Дисферлин — ещё один мембранный белок, связанный с дистальной формой мышечной дистрофии. Отсутствие определённых протеинов, функционирующих в клеточном ядре, приводит к развитию мышечной дистрофии Эмери — Дрейфуса (эмерин, ламина А, ламина С) или окулофарингеальной мышечной дистрофии (PABPN1)[9][10].
Ребёнок может унаследовать от своих родителей по одной копии дефектного гена, что может привести к развитию заболевания. В случае доминантного наследования достаточно одной копии дефектного гена, чтобы проявилось заболевание. При Х-сцепленном наследовании болезнь передаётся от матери к сыну. Мышечная дистрофия может быть как наследственной, так и возникать вследствие воспалительных и других патологий. Важно уметь различать различные формы дистрофий. С помощью генетических тестов, проводимых с использованием образца крови, можно проанализировать гены пациента на наличие специфических дефектов, характерных для редких мышечных дистрофий. Это позволяет прогнозировать течение заболевания и помогает семьям оценить риск передачи болезни будущим поколениям[3][11].
Человек может быть носителем дефектного гена, но не иметь симптомов заболевания. Если заболевание доминантное, то для его проявления достаточно одной копии повреждённого гена. Носитель дефектного гена может передать заболевание своим детям. Если заболевание связано с полом, то оно передаётся от матери к сыну, а дочери могут быть носительницами, но, как правило, не болеют. В ряде случаев мышечные дистрофии проявляются внезапно, несмотря на то что оба родителя могут являться носителями дефектного гена. В отдельных случаях мышечные дистрофии могут возникать без видимых причин, если во время развития эмбриона происходит спонтанная мутация, при этом родители не являются носителями повреждённого гена. Это явление называется спонтанной мутацией и может передаваться последующим поколениям[11]. Для выявления причины мышечной слабости применяется специальное исследование, известное как электромиография
Таким образом, потомкам передаётся ген, который может стать причиной развития определённой формы мышечной дистрофии. Вероятность передачи различных форм мышечной дистрофии зависит от множества факторов, включая конкретный тип заболевания[3][12].
Диагностика
При мышечной дистрофии прогрессирующее поражение мышечных волокон приводит к выраженной слабости, и в тяжёлых стадиях пациент утрачивает способность к самостоятельному движению. Некоторые формы мышечной дистрофии могут сопровождаться контрактурами — тугоподвижными суставами, а также сколиозом — искривлением позвоночника. В большинстве случаев при мышечной дистрофии истощение мышц в поражённых областях становится визуально заметным (мышцы уменьшаются в размерах), и руки, ноги или туловище могут выглядеть искажёнными[14]. Если мышечная дистрофия затрагивает глотательные мышцы, то могут потребоваться дополнительные меры предосторожности, чтобы еда и питьё не попадали в лёгкие. Хотя при большинстве мышечных дистрофий мозг не поражается, некоторые из них всё же связаны с изменениями в мозге, что приводит к ухудшению когнитивных функций. Уровень этих изменений может быть как незначительным, так и весьма значительным. Наконец, некоторые формы мышечной дистрофии затрагивают сердце, что требует постоянного контроля за его работой. Каждое заболевание имеет свои уникальные особенности и проблемы[15].
- прогрессирующее истощение мышц;
- нарушение равновесия;
- сколиоз (аномальное искривление позвоночника);
- мышечные контрактуры, приводящие к ограничению подвижности суставов[7];
- неспособность ходить;
- походка «вразвалочку»;
- синдром Гауэрса, наблюдаемый при мышечной дистрофии Дюшенна[7];
- деформация голени, наблюдаемая при дистрофии Дюшенна;
- дыхательная недостаточность[8];
- кардиомиопатия[16].
Диагностика различных форм мышечной дистрофии начинается с тщательного анализа анамнеза пациента и его семьи, а также с проведения тщательного осмотра. На раннем этапе диагностики часто назначается анализ крови для определения уровня креатинфосфокиназы — фермента, который высвобождается из повреждённых мышц. Повышенный уровень креатинфосфокиназы в крови обычно указывает на то, что мышцы разрушаются в результате патологического процесса, такого как мышечная дистрофия или воспаление[3][16]. Однако высокий уровень креатинфосфокиназы может свидетельствовать о том, что мышечная слабость вызвана патологическими процессами в самих мышцах, но не позволяет точно определить конкретное заболевание. Дополнительно оценивают уровень ЛДГ, АСТ и АЛТ, которые также могут быть повышены вследствие мышечного цитолиза[3].
В диагностически сложных случаях применяют молекулярно-генетическое тестирование, позволяющее подтвердить конкретный тип дистрофии, выявить делеции, дупликации или точковые мутации в соответствующих генах. Генетическое исследование является «золотым стандартом» верификации диагноза и позволяет определить носительство и провести медико-генетическое консультирование семье, путём гистологического исследования биоптата мышцы, которое позволяет определить конкретное заболевание[16].
Магнитно-резонансная томография применяется для оценки состояния белого вещества и выявления изменений, связанных с дефицитом мерозина у детей мужского пола. Недостаток мерозина приводит к выраженному неврологическому дефициту и характерным изменениям структуры белого вещества[17].
Дифференциальная диагностика
Дифференциальная диагностика мышечных дистрофий проводится с рядом заболеваний, сопровождающихся мышечной слабостью и атрофией, но имеющих иную этиологию. Прежде всего исключаются воспалительные миопатии (дерматомиозит, полимиозит), эндокринные миопатии (при гипотиреозе, гипертиреозе, синдроме Кушинга), токсические и метаболические поражения мышц (например, при длительном приёме глюкокортикоидов или алкоголя), а также нейрогенные заболевания — спинальная амиотрофия, боковой амиотрофический склероз, периферические нейропатии. Для уточнения диагноза используют электромиографию, исследование уровня креатинфосфокиназы в сыворотке крови, молекулярно-генетический анализ и морфологическое исследование биоптата мышцы с иммуногистохимическим и электронно-микроскопическим контролем[3][18].
Лечение
К методам лечения относятся[3][19][20]:
- Физиотерапия — комплекс упражнений, направленных на укрепление мышц и улучшение их функций.
- Трудотерапия — занятия, направленные на адаптацию повседневных действий и создание более удобных условий для жизни.
- Ортопедические вмешательства при мышечных дистрофиях включают коррекцию контрактур (удлинение сухожилий, релиз мягких тканей), стабилизацию позвоночника при прогрессирующем сколиозе (спондилодез), а также операции по выравниванию деформаций стоп и нижних конечностей для улучшения опоры и снижения болевого синдрома
- Логопедия — коррекция речевых нарушений, связанных с мышечной дистрофией.
- Респираторная терапия — упражнения, направленные на улучшение дыхания и увеличение объёма лёгких[21].
В некоторых случаях для улучшения качества жизни могут потребоваться дополнительные меры, такие как:
- Ортезы — ортопедические приспособления, предназначенные для поддержки и коррекции[2].
- Корригирующие ортопедические операции — хирургические вмешательства, направленные на исправление деформации суставов и костей[22].
Проблемы с сердцем, связанные с мышечной дистрофией Эмери — Дрейфуса (EDMD) и миотонической мышечной дистрофией, могут потребовать установки кардиостимулятора[23].
Миотонию — замедленное расслабление мышцы после сильного сокращения, которая часто встречается при миотонической мышечной дистрофии, можно лечить с помощью таких препаратов, как хинин[24].
В ходе 24-недельного исследования было установлено, что низкоинтенсивные вспомогательные упражнения, динамические тренировки и велотренировки рук и ног на специальном велосипеде способны значительно замедлить потерю функциональности при мышечной дистрофии. Эти методы лечения являются безопасными и доступными даже для детей, которые только начинают ходить. Однако важно избегать эксцентричных или интенсивных упражнений, которые могут вызывать болезненность, так как они могут привести к дальнейшему повреждению[25].
Трудотерапия способствует тому, чтобы пациент мог вести привычный образ жизни, включая самостоятельное питание и уход за собой. Это достигается с помощью адаптивного оборудования и методов энергосбережения[26]. Трудотерапия может внести изменения в окружающую среду человека как дома, так и на работе, чтобы повысить её функциональность и доступность[27].
Прогноз
Прогноз развития заболевания зависит от конкретной формы мышечной дистрофии. Большинство форм мышечной дистрофии имеют прогрессирующее течение и со временем неуклонно ухудшаются. Однако возраст начала и скорость прогрессирования могут значительно различаться в зависимости от формы заболевания. Некоторые из этих болезней могут серьёзно повлиять на продолжительность жизни. Некоторые виды дистрофий характеризуются прогрессирующей мышечной слабостью и утратой функций, что может привести к тяжёлой физической инвалидности и даже к нарушению работы дыхательных мышц и сердца, представляя угрозу для жизни. В то же время другие формы заболевания не оказывают влияния на продолжительность жизни и вызывают лишь незначительные нарушения[2].
Диспансерное наблюдение
Диспансерное наблюдение при мышечных дистрофиях — ключевой элемент комплексной терапии, направленный на своевременное выявление осложнений и оптимизацию междисциплинарного ухода. Согласно российским клиническим рекомендациям 2023 года по мышечной дистрофии Дюшенна и Беккера, пациенты должны регулярно проходить кардиореспираторное мониторирование с оценкой функции дыхания, сатурации и ЭКГ, особенно при признаках гипоксемии или сниженной жизненной ёмкости лёгких (ЖЕЛ). Важной составляющей диспансерного плана также является мультидисциплинарный подход: регулярные визиты к кардиологу, пульмонологу, физиотерапевту, а также психологу и другим специалистам, исходя из тяжести и формы заболевания[3]
Профилактика
Специфической профилактики мышечных дистрофий не существует в связи с их генетической природой. Основное значение имеет медико-генетическое консультирование семей, в которых выявлены случаи заболевания, а также проведение пренатальной и преимплантационной диагностики при известных мутациях. Вторичная профилактика направлена на замедление прогрессирования заболевания и предупреждение осложнений — контрактур, дыхательной недостаточности, кардиомиопатии. Для этого применяются программы дозированной физической активности, физиотерапии, ортопедической коррекции, регулярного кардиологического и пульмонологического наблюдения[28].
Примечания
Литература
- М. Р. Шаймурзин, И. С. Луцкий, О. С. Евтушенко, М. В. Ефименко. Возможности мануальной терапии в коррекции сколиоза у детей со спинальными мышечными атрофиями// Университетская клиника.— 2020-12-01.— Вып. 4(37).— С. 20.— ISSN 1819-0464.— doi:10.26435/uc.v0i4(37).517.
- De Los Angeles Beytía, Maria; Vry, Julia; Kirschner, Janbernd (2012). “Drug treatment of Duchenne musculardystrophy: available evidence and perspectives”. Acta Myologica. 31 (1): 4—8. PMC 3440798. PMID 22655510.
- Bertini, Enrico; D'Amico, Adele; Gualandi, Francesca; Petrini, Stefania (December 2011). “Congenital Muscular Dystrophies: A Brief Review”. Seminars in Pediatric Neurology. 18 (4): 277—288. DOI:10.1016/j.spen.2011.10.010. PMC 3332154. PMID 22172424.