Мышечная дистрофия Беккера
Мы́шечная дистрофи́я Бе́ккера (МДБ; миодистрофи́я Бе́ккера) — это наследственное Х-сцепленное рецессивное нервно-мышечное заболевание, вызываемое мутациями в гене дистрофина (DMD), приводящими к выработке аномального, частично функционального белка дистрофина. Основным клиническим проявлением болезни является прогрессирующая мышечная слабость, гипотония, атрофия и повышенная утомляемость, которые первоначально локализуются в мышцах тазового пояса, бёдер и голеней. По сравнению с более тяжёлой формой — мышечной дистрофией Дюшенна — течение МДБ является более мягким и вариабельным, с более поздним началом симптомов и более медленным прогрессированием. По мере развития заболевания у пациентов почти в 100 % случаев развивается дилатационная кардиомиопатия, характеризующаяся фиброзом миокарда, что приводит к сердечной недостаточности и создаёт высокий риск возникновения жизнеугрожающих аритмий. Ведение пациентов с МДБ является поддерживающим и многопрофильным, ключевую роль в котором играет комплексная реабилитация, направленная на максимально долгое сохранение двигательной функции и качества жизни. Средняя продолжительность жизни больных составляет около 40-50 лет, а наиболее частой причиной летального исхода является прогрессирующая кардиомиопатия и её осложнения[1][2].
Что важно знать
История
МДБ впервые была описана Беккером и Кинером в 1955 году[3].
Классификация
МДБ входит в группы дистрофинопатий[4].
Этиология
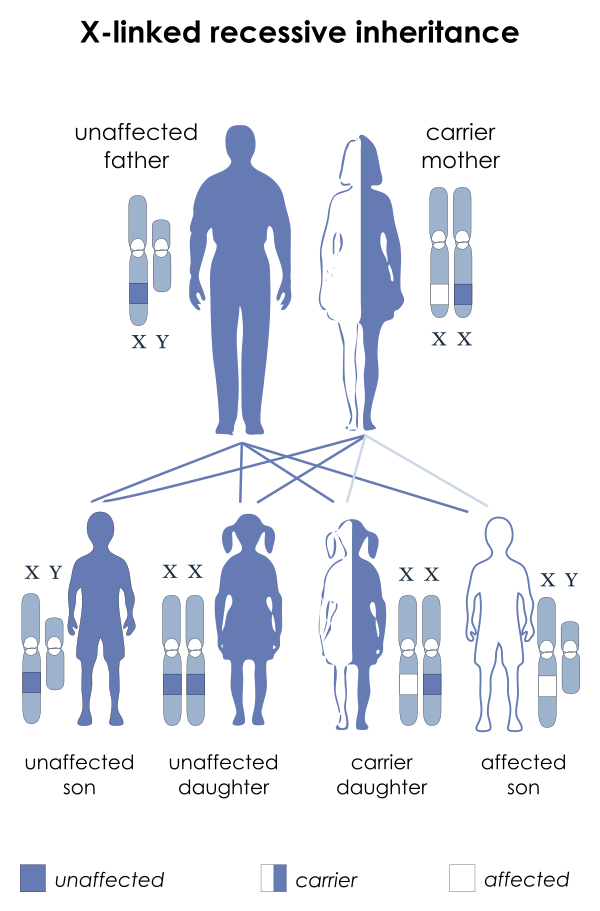
МДБ возникает в результате мутации в гене, кодирующем субсарколеммальный белок дистрофин. Дефектный ген расположен в локусе Xp21.2 на Х-хромосоме, и наследование происходит по Х-сцепленному рецессивному типу. У пациентов без чёткой Х-сцепленной наследственной истории дефект может быть связан не с самим дистрофином, а с мутациями в генах, кодирующих ассоциированные с дистрофином гликопротеины. Ген дистрофина состоит из 79 экзонов в регионе Xp21 и охватывает более 2200 килобаз. Высокая вероятность мутаций в этом гене связана с его огромным размером — около 2 миллионов пар оснований, что делает его особенно уязвимым во время мейоза. Также, хотя и реже, встречаются другие типы мутаций, такие как небольшие делеции, инсерции и точечные варианты последовательности[2].
Существует ключевое различие в типах мутаций, вызывающих мышечную дистрофию Дюшенна (МДД) и МДБ. МДД преимущественно является следствием сдвига рамки считывания (out-of-frame мутации) открытой рамки считывания гена дистрофина, что приводит к полному отсутствию функционального белка. В отличие от этого, МДБ обычно возникает из-за мутаций, сохраняющих рамку считывания (in-frame мутации), в результате чего производится усечённый или структурно изменённый, но частично функциональный дистрофин. Это фундаментальное различие лежит в основе более широкого спектра фенотипических проявлений и более мягкого течения болезни при МДБ по сравнению с МДД[2].
Патогенез
Патогенез МДБ неразрывно связан с нарушением структуры и функции белка дистрофина, являющегося ключевым элементом для стабильности мышечного волокна. Дистрофин, кодируемый самым крупным из известных генов, расположенным в локусе Xp21, выполняет роль молекулярной пружины, связывающей внутриклеточный актиновый цитоскелет с внеклеточным матриксом через комплекс дистрогликанов. Этот белок, состоящий из более чем 3600 аминокислот, организован в четыре основных домена: N-концевой актин-связывающий домен, центральный стержневой домен, богатый цистеином домен и C-концевой домен. Такая структура позволяет ему с одной стороны крепиться к саркомерному актину, а с другой — через комплекс гликопротеинов, включая β-дистрогликан и саркогликаны, соединяться с ламинином базальной мембраны, обеспечивая механическую стабильность сарколеммы во время мышечных сокращений[5].
В основе МДБ лежат, как правило, протяжённые делеции или дупликации (реже точковые мутации) в гене дистрофина, которые, в отличие от мутаций при МДД, сохраняют рамку считывания. Это приводит к синтезу усечённого или структурно изменённого, но частично функционального дистрофина. Степень сохранения функции зависит от локализации и размера мутации: изменения в N-концевой или центральной областях могут вызывать менее тяжёлые последствия, если не нарушают критических точек связывания. Однако даже частичная дисфункция дистрофина запускает каскад патологических процессов[2][5]:
- нарушение целостности дистрофин-гликопротеинового комплекса делает сарколемму уязвимой для механических повреждений. Это приводит к её нестабильности, повышенной проницаемости и нарушению ионного гомеостаза, в первую очередь — к аномальному притоку ионов кальция в миоцит. Внутриклеточный кальциевый дисбаланс усугубляется опосредованной воспалением гиперэкспрессией синтазы оксида азота. Продуцируемый в избытке оксид азота нитрозилирует рианодиновые рецепторы саркоплазматического ретикулума, вызывая дополнительную утечку кальция в цитозоль;
- повышенная концентрация кальция активирует протеолитические ферменты, в частности кальпаины, которые запускают деградацию внутриклеточных белков. Мышцы подвергаются повторяющимся циклам микроповреждений, некроза и регенерации. Со временем регенеративный потенциал сателлитных клеток истощается, и мышечная ткань замещается жировой и соединительной, приводя к атрофии. Особенностью патогенеза МДБ является также нарушение рекрутирования нейрональной синтазы оксида азота в сарколемму при нагрузке, что ведёт к дефициту локального сосудорасширяющего сигнала, нарушению перфузии работающей мышцы и усугублению утомляемости.
- конечным итогом этого многокомпонентного патологического каскада являются системные осложнения: дилатационная кардиомиопатия вследствие поражения кардиомиоцитов, прогрессирующая дыхательная недостаточность из-за слабости дыхательной мускулатуры и контрактуры суставов.
Эпидемиология
МДБ является редким заболеванием, которое поражает почти исключительно лиц мужского пола вследствие Х-сцепленного рецессивного типа наследования. Согласно исследованию, проведённому в США в 2010 году, распространённость МДБ во всех возрастных группах составила 0,26 случая на 10 000 мужчин. Также было отмечено, что это состояние встречается чаще среди белых лиц по сравнению с чернокожими лицами. Региональные исследования демонстрируют вариабельность показателей: так, распространённость МДБ в Южной Африке оценивается в 0,01 случая, в азиатских странах — от 0,1 до 0,2 случая, а в странах Европы — от 0,1 до 0,7 случая на 10 000 мужчин. Согласно отдельным данным, МДБ встречается примерно в 3 раза реже, чем МДД[2].
Диагностика
У детей заболевание может манифестировать проксимальной мышечной слабостью, которая предшествует слабости в дистальных отделах конечностей. Часто сообщается о мышечных судорогах при интенсивной нагрузке и задержке в достижении основных моторных вех. Рост может замедляться, приводя к низкорослости. У части пациентов наблюдается отставание в когнитивном развитии: коэффициент интеллекта менее 70 отмечается у 20-25 % больных. Некоторые пациенты сталкиваются с поздним началом заболевания и сохраняют способность к самостоятельной ходьбе до взрослого возраста. По мере прогрессирования состояния могут наблюдаться такие проявления, как патологические переломы, кардиомиопатия, затруднение дыхания, контрактуры суставов и ходьба на носках. Кардиомиопатия обусловлена фиброзом стенки левого желудочка и является причиной развития жизнеугрожающих аритмий[2].
Женщины-носительницы мутации могут иметь клинические проявления, наиболее часто — изолированную кардиомиопатию, хотя у некоторых также возможна лёгкая слабость скелетных мышц. Симптоматическими становятся примерно 22 % носительниц, причём степень выраженности симптомов широко варьирует[2].
При физикальном обследовании могут выявляться следующие признаки[2]:
- атрофия мышц в сочетании с псевдогипертрофией икроножных мышц;
- гипотония и гипорефлексия квадрицепсов, возможны фасцикуляции;
- симптом Говерса — характерный приём «взбирания по себе» при вставании из положения сидя или лёжа;
- усиленный поясничный лордоз;
- укорочение ахиллова сухожилия;
- контрактуры коленных, локтевых или тазобедренных суставов;
- макроглоссия;
- увеличение мышц предплечий;
- сколиоз, развивающийся вследствие прогрессирующей слабости мышц грудной клетки;
- признаки сердечной недостаточности: набухание шейных вен, смещение верхушечного толчка, периферические отёки, ритм галопа, шумы митральной или трикуспидальной регургитации;
- признаки дыхательной недостаточности в далеко зашедших случаях: крепитация, цианоз.
При проведении игольчатой электромиографии у пациентов с МДБ регистрируется характерный миопатический паттерн изменений, который проявляется уменьшением средней длительности и снижением амплитуды потенциалов двигательных единиц[2][6].
Ультразвуковое исследование мышц: визуализирует структурные изменения скелетной мускулатуры, характерные для прогрессирующего заболевания. Основным признаком является замещение нормальной мышечной ткани гиперэхогенными жировой и фиброзной тканями. Это проявляется повышенной и неоднородной эхогенностью мышц, уменьшением их объёма и исчезновением чёткой фибриллярной структуры[6][7].
Электрокардиография: типичными находками являются различные формы аритмий (тахикардия, фибрилляция предсердий, экстрасистолия) и нарушения проводимости (блокады ножек пучка Гиса, в особенности правой). Также могут регистрироваться признаки гипертрофии миокарда желудочков и патологические изменения зубца Q, имитирующие инфаркт[2][6].
Эхокардиография: наиболее характерными и ранними признаками являются систолическая дисфункция (снижение фракции выброса левого желудочка) и дилатация полости левого желудочка. По мере прогрессирования развиваются гипертрофия миокарда и нарушение функции клапанов, чаще всего митральная регургитация, возникающая из-за дилатации фиброзного кольца и дисфункции папиллярных мышц[7].
Магнитно-резонансная томография мышц: характерно жировое замещение мышечной ткани (гиперинтенсивный сигнал на T1), отёк, указывающий на активное повреждение (гиперинтенсивный сигнал на STIR/T2-FS), и атрофия[7].
Биохимический анализ крови: характерно повышение активности креатинфосфокиназы[7].
Гистологическое исследование биоптата мышечной ткани выявляет характерные, но неспецифичные для МДБ изменения. Патогномоничным гистологическим признаком заболевания при микроскопическом исследовании является картина продолжающегося некроза и регенерации миофибрилл. У молодых пациентов более выражены активный некроз мышечных волокон и скопления базофильных регенерирующих волокон, в то время как у пациентов старшего возраста чаще обнаруживаются расщепление мышечных волокон с некрозом, увеличение числа внутренних ядер, гипертрофия волокон, жировое замещение и эндомизиальный фиброз[2].
Молекулярно-генетический анализ методом секвенирования: характерно выявление мутации в гене DMD[2].
Дифференциальная диагностика
Дифференциальная диагностика МДБ проводится со следующими заболеваниями:
- мышечная дистрофия Дюшенна;
- полимиозит;
- спинальная мышечная атрофия;
- поясно-конечностная мышечная дистрофия;
- дилатационная кардиомиопатия;
- мышечная дистрофия Эмери — Дрейфуса;
- миастения;
- метаболические миопатии.
Осложнения
Потенциальными осложнениями МДБ являются[2]:
- потеря способности к самостоятельному передвижению;
- когнитивные нарушения;
- задержка роста;
- патологические переломы;
- кардиомиопатия;
- контрактуры суставов;
- сколиоз;
- послеоперационные инфекции грудной клетки;
- прогрессирующая печёночная и дыхательная недостаточность;
- почечная недостаточность вследствие рабдомиолиза и миоглобинурии;
- надпочечниковая недостаточность и иммуносупрессия, связанные с длительным применением глюкокортикостероидов.
Лечение
Специфической терапии МДБ не существует. Общий подход к ведению пациентов часто аналогичен таковому при более лёгких формах МДД и носит симптоматический и поддерживающий характер.
1. Фармакотерапия:
- глюкокортикостероиды (преднизолон или дефлазакорт) остаются основой терапии при наличии значительной мышечной слабости. Их рекомендуется начинать до развития выраженной физической недееспособности и продолжать даже после потери способности к самостоятельному передвижению. Доказано, что терапия глюкокортикоидами способствует увеличению продолжительности жизни за счёт отсрочки развития кардиомиопатии, улучшения функции лёгких, замедления прогрессирования сколиоза;
- кардиопротекторная терапия: поскольку дилатационная кардиомиопатия с сердечной недостаточностью — ведущая причина смертности, жизненно важны ранняя диагностика и лечение. Основой кардиопротекции являются ингибиторы ангиотензин-превращающего фермента, часто в комбинации с бета-адреноблокаторами;
- прочие препараты: для улучшения мышечной микроциркуляции может назначаться донор оксида азота.
2. Немедикаментозное лечение и реабилитация:
- ключевую роль играет физическая реабилитация, направленная на максимально долгое сохранение подвижности и силы. Программа включает кинезиотерапию, дыхательную гимнастику, ортезирование (например, для голеностопных суставов) и эрготерапию.
3. Хирургическое вмешательство:
- при быстром прогрессировании симптомов может рассматриваться хирургическая коррекция:
- для удлинения сохранной фазы ходьбы выполняют операции на сухожилиях (например, релиз ахиллова сухожилия);
- при прогрессирующем сколиозе, угрожающем функции лёгких и сердца, проводят спинальную стабилизацию (спондилодез);
- в некоторых случаях применяются мышечные транспозиции.
Прогноз
Течение МДБ, как правило, значительно мягче, чем при МДД. Однако с прогрессированием заболевания шансы на выживание снижаются, и пациенты становятся зависимыми от поддерживающих медицинских вмешательств, направленных на продление жизни. Средняя ожидаемая продолжительность жизни пациентов с МДБ составляет около 40-50 лет. Наиболее частой и непосредственной причиной летального исхода является дилатационная кардиомиопатия с развитием сердечной недостаточности или жизнеугрожающих аритмий[2].
Диспансерное наблюдение
План диспансерного наблюдения у пациентов с МДБ включает регулярные консультации кардиолога для мониторинга и раннего лечения кардиомиопатии, осмотры пульмонолога для оценки дыхательной функции и своевременного начала респираторной поддержки, а также наблюдение у ортопеда для профилактики и хирургической коррекции сколиоза и контрактур суставов. Необходимость и частота консультаций определяются индивидуально в зависимости от темпов прогрессирования заболевания и текущего состояния пациента[3].
Профилактика
Консультирование относительно носительства мутации матерью и сиблингами пациента является важнейшим аспектом профилактики МДБ. Необходимо обсуждать риск передачи заболевания потомству. Выявление мозаицизма у матери или отца, а также определение риска такой передачи — ещё одна ключевая тема для рассмотрения в семьях, где нет явных гетерозиготных носителей, или в случаях спорадического (изолированного) заболевания[3].
Примечания
Литература
- Chunkayeva D., Jaxybayeva A. A review of diagnosis of Duchenne and Becker muscular dystrophy (англ.) // Journal of Clinical Medicine of Kazakhstan. — 2021. — Vol. 18, no. 5. — P. 6—10. — doi:10.23950/jcmk/11222.
- Царькова С. А., Ушакова Р. А., Громада Н. Е. и др. Прогрессирующая мышечная дистрофия Дюшенна-Беккера. Трудности диагностики // Доктор.Ру. — 2020. — № 10. — С. 61—65. — doi:10.31550/1727-2378-2020-19-10-61-65.
- Okubo M. Molecular genetics of dystrophinopathy (англ.) // Journal of Human Genetics. — 2025. — doi:10.1038/s10038-025-01357-7.