Врожденные мышечные дистрофии
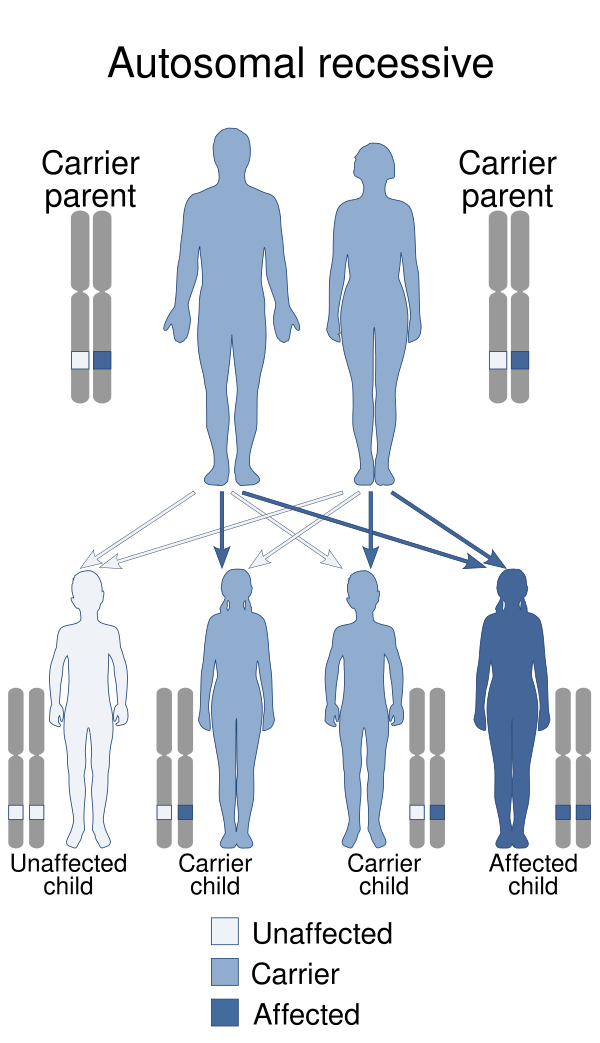
Врождённые мы́шечные дистрофи́и (ВМД) это клинически и генетически разнородная группа наследственных заболеваний нервно-мышечной системы, наследуемых преимущественно по аутосомно-рецессивному типу. Ключевыми клиническими проявлениями, возникающими с рождения или в раннем детском возрасте, являются мышечная гипотония, слабость и контрактуры суставов. Прогноз при данной патологии является вариабельным и зависит от конкретного типа ВМД[2].
Что важно знать
История
ВМД были впервые описаны в начале XX века, однако долгое время оставались слабо дифференцированной группой заболеваний. Баттен в 1903—1904 годах выделил признаки тяжёлой врождённой миопатии, а сам термин «врождённая мышечная дистрофия» был предложен Ховардом в 1908 году. В последующие десятилетия на основе клинических или этнических особенностей стали выделять отдельные формы ВМД. В период с 1930 по 1990 годы были описаны: врождённая склерозирующая атоническая мышечная дистрофия Ульриха (1930), врождённая мышечная дистрофия Фукуямы (1960), синдром ригидного позвоночника Дюбуовица (1970), болезнь мышц, глаз и мозга (болезнь MEB) Сантавуори (1977) и, наконец, синдром Уокера — Варбурга (1986). В 1993 году была идентифицирована «западная форма врождённой мышечной дистрофии», имевшая сходные с ВМД Фукуямы проявления, но в другом географическом регионе[3].
После 1993 года внедрение методов молекулярной диагностики произвело революцию в диагностике ВМД. В 1994 году с помощью генетического сцепления и анализа мутаций была выявлена мерозин-негативная, или мерозин-дефицитная ВМД, связанная с мутацией гена LAMA2. В 1998 году были открыты гены, ответственные за ВМД Фукуямы и ВМД с ригидным позвоночником. В 2001 году установлена генотип-фенотипическая корреляция при ВМД Ульриха, а в 2003 году описана новая форма ВМД с тяжёлым поражением центральной нервной системы, ассоциированная с мутацией гена LARGE. В 2005 году была установлена связь синдрома Уокера — Варбурга с мутацией в гене POMT2[3].
Классификация
В зависимости от этиологии выделяются следующие виды ВМД[3]:
- Нарушения в структурных белках базальной мембраны или внеклеточного матрикса мышечных волокон:
- ВМД, связанная с мутацией LAMA2;
- ВМД, связанная с дефектом коллагена VI (ВМД Ульриха, миопатия Бетлема);
- ВМД с дефицитом интегрина α7.
- Дефекты гликозилирования альфа-дистрогликана (дистрогликанопатии):
- спектр заболеваний варьирует от наиболее тяжёлых форм (мышечная дистрофия-дистрогликанопатия типа А1) — синдром Уокера — Варбурга, болезнь MEB, ВМД Фукуямы — до умеренных (тип B1) и относительно лёгких (тип C1), клинически сходных с поясно-конечностной мышечной дистрофией.
- Дефекты белков эндоплазматического ретикулума:
- селенопротеин-N-ассоциированная миопатия (связанная с геном SEPN1).
- Дефекты белков ядерной оболочки:
- ламин A/C-ассоциированная ВМД.
- Нарушения белков, участвующих в транспорте из эндоплазматического ретикулума в аппарат Гольджи:
- ВМД с жировой дистрофией печени и инфантильной катарактой.
- Прочие формы ВМД:
- митохондриальная ВМД;
- ВМД с поражением мозжечка;
- ВМД с экстрапирамидными симптомами;
- ВМД с катарактой и интеллектуальными нарушениями;
- синдром Маринеску — Шегрена;
- муколипидоз IV типа.
- синдром мышечной дистрофии, потери слуха и яичниковой недостаточности.
Согласно международной классификации болезней 10-го пересмотра ВМД относится к первичным поражениям мышц (G71)[4].
Согласно международной классификации болезней 11-го пересмотра ВМД относится к врождённым миодистрофиям (8C70.6)[5].
Этиология
Этиология ВМД является генетически гетерогенной. Известно около 30 ключевых генов, мутации в которых приводят к развитию различных форм заболевания. К ним относятся, в частности: COL6A1, COL6A2, COL6A3, COL12A1, ITGA7, LAMA2, LMNA, CHKB, RYR1, POMT1, POMT2, POMGNT1, FKTN, FKRP, LARGE, ISPD, POMGNT2, DAG1, TMEM5, B3GLNT2, POMK, B4GAT1, GMPPB, DPM1-3, DOLK, SEPN1, TRIP4. Ряд исследователей также включают в этот перечень такие гены, как SYNE1, TCAP, DNM2, PLEC1, GFPT1, MICU1, TTN и INPP5K, что подчёркивает сложность и многообразие молекулярных основ ВМД. В основе заболевания лежат дефекты белков, отвечающих за структурную целостность мышечного волокна, клеточной адгезии, гликозилирования, функционирования эндоплазматического ретикулума и ядерной оболочки. Подавляющее большинство форм ВМД наследуется по аутосомно-рецессивному типу, однако некоторые, например, связанные с мутациями в генах LMNA и COL6, могут иметь и аутосомно-доминантный тип наследования[2][3].
Патогенез
Патофизиологические механизмы ВМД различны и определяются тем, в каком звене цепи, обеспечивающей структурную целостность и функцию мышечного волокна, произошёл сбой. Однако, патогенез некоторых форм остаётся до конца не изученным. Основные патогенетические механизмы включают[3]:
- коллагенопатия: коллаген VI, являясь ключевым компонентом внеклеточного матрикса, обеспечивает структурную поддержку и адгезию мышечных клеток. Его недостаток или аномалия нарушает стабильность базальной мембраны, делая мышечные волокна уязвимыми к механическому стрессу, что приводит к прогрессирующей дистрофии;
- при LAMA2-ассоциированной ВМД (мерозин-дефицитная ВМД 1А типа) патогенез связан с мутацией в гене LAMA2, кодирующем α2-цепь ламинина. Этот белок критически важен для связи базальной мембраны с внутриклеточным цитоскелетом через комплекс дистрогликанов. Дефицит ламинина разрушает архитектонику базальной мембраны, повышает проницаемость гематоэнцефалического барьера (что объясняет характерные изменения белого вещества) и приводит к тяжёлой мышечной дегенерации, часто сопровождающейся демиелинизирующей нейропатией;
- тяжёлые формы ВМД с поражением мозга и глаз (синдром Уокера — Варбурга, болезнь MEB, ВМД Фукуямы) относятся к группе дистрогликанопатий. Их патогенез связан с нарушением процесса гликозилирования белка альфа-дистрогликана, который служит основным рецептором для ламинина во внеклеточном матриксе. Дефектное гликозилирование, вызванное мутациями в генах, таких как POMT1, POMT2, FKTN, FKRP и других, нарушает связывание с ламинином. Это ослабляет связь цитоскелета с базальной мембраной и дополнительно нарушает процессы нейрональной миграции и развития коры головного мозга, что приводит к комплексным аномалиям скелетной мускулатуры, глаз и центральной нервной системы;
- отдельную группу составляет селенопротеин-N-ассоциированная миопатия, обусловленная мутациями в гене SEPN1. Патогенез связан с дисфункцией белка эндоплазматического ретикулума, который участвует в гомеостазе кальция и защите клетки от окислительного стресса. Это приводит к избирательному поражению определённых групп мышц (осевой мускулатуры, диафрагмы) с развитием характерного синдрома ригидного позвоночника и ранней дыхательной недостаточности при относительно сохранной силе в конечностях;
- патогенез LMNA-ассоциированной ВМД обусловлен мутациями в гене LMNA, кодирующем ламины А/С — структурные белки ядерной оболочки. Дефектные ламины нарушают архитектонику и стабильность ядра мышечного волокна, делая его чувствительным к механическим нагрузкам, что клинически проявляется тяжёлой мышечной слабостью, особенно в разгибателях шеи («синдром свисающей головы»), и ранним вовлечением дыхательной мускулатуры.
Эпидемиология
Эпидемиология ВМД остаётся недостаточно изученной. Существующие данные, вероятно, занижены из-за исторически ограниченных возможностей диагностики. В среднем распространённость заболевания в мире оценивается приблизительно в 1 случай на 100 000 новорождённых, однако этот показатель варьирует в зависимости от региона и популяции. Так, по имеющимся сведениям, общая распространённость ВМД в Италии составляет около 0,56 случая на 100 000 населения, в северной Англии — около 0,89 на 100 000. Данные по Китаю демонстрируют ещё более значительные региональные различия: от 0,017 на 100 000 в Северо-Западном регионе до 0,083 на 100 000 в Пекине. Хотя спектр основных форм ВМД в большинстве исследованных популяций схож, их удельный вес и распространённость конкретных генетических вариантов могут существенно различаться[2].
Диагностика
Основу клинической картины ВМД составляют симптомы, общие для большинства форм заболевания, однако их выраженность и возраст дебюта широко варьируют даже в пределах одной семьи. Ключевые общие проявления включают генерализованную мышечную гипотонию (синдром «вялого ребёнка») и диффузную мышечную слабость, которые возникают с рождения или в первые месяцы жизни. Это приводит к задержке моторного развития: дети поздно начинают держать голову, переворачиваться, сидеть и ходить. Часто наблюдаются множественные контрактуры крупных суставов (тазобедренных, коленных, локтевых), сочетающиеся в некоторых случаях с гиперподвижностью дистальных суставов. Поражение дыхательной мускулатуры, особенно диафрагмы, ведёт к прогрессирующей дыхательной недостаточности. Прогрессирующий кифосколиоз является частым проявлением, усугубляющим дыхательную недостаточность[6].
Наряду с общими чертами, различные генетические формы ВМД имеют отличительные клинические особенности, позволяющие заподозрить конкретный диагноз[6].
- поражение центральной нервной системы и глаз является отличительной чертой тяжёлых дистрогликанопатий (синдром Уокера — Варбурга, болезнь MEB, ВМД Фукуямы). Для них характерны структурные аномалии мозга (лиссэнцефалия, гипоплазия мозжечка, гидроцефалия), тяжёлая умственная отсталость, судороги, а также комплексные пороки развития глаз (врождённая катаракта, микрофтальмия, глаукома, отслойка сетчатки). При LAMA2-ассоциированной ВМД часто наблюдается демиелинизирующая невропатия, в то время как интеллект обычно сохранён;
- преимущественное поражение осевой мускулатуры и ранняя дыхательная недостаточность при относительно сохранной силе в конечностях типичны для SEPN1-связанной миопатии. Основным признаком служит ранняя ригидность позвоночника с быстрым развитием сколиоза, при этом большинство пациентов сохраняют способность к ходьбе;
- сочетание проксимальных контрактур с дистальной гиперподвижностью (гиперлабильностью суставов кистей и стоп) считается патогномоничным признаком коллагенопатий (ВМД Ульриха). Также для этой формы характерны фолликулярный гиперкератоз («гусиная кожа») и необычно мягкая кожа ладоней и стоп;
- синдром «свисающей головы» (выраженная слабость разгибателей шеи) является ярким и ранним признаком тяжёлой LMNA-ассоциированной ВМД, которая также часто сопровождается быстрым развитием контрактур и кардиомиопатии.
Магнитно-резонансная томография головного мозга: наиболее выраженные и специфичные изменения выявляются при тяжёлых дистрогликанопатиях (синдром Уокера — Варбурга, болезнь MEB, ВМД Фукуямы). Для них характерны грубые структурные аномалии: лиссэнцефалия, гипоплазия мозжечка и ствола мозга, вентрикуломегалия, агенезия мозолистого тела и кистозные изменения[6][7].
Электронейромиография: характерна регистрация коротких, полифазных двигательных единиц с низкой амплитудой, что указывает на миопатический паттерн активности[8].
Эхокардиография: возможно выявление дилатационной кардиомиопатии[6].
Электрокардиография: возможны явления перегрузки правого желудочка, высокие зубцы R, глубокие зубцы Q и инверсия зубцов Т[8].
Офтальмологическое обследование включает визометрию, офтальмоскопию, офтальмотонометрию, биомикроскопию, оптическую когерентную томографию и другие методы[9][10].
Гистологическое исследование биоптата мышечной ткани позволяет выявить типичный дистрофический миопатический паттерн. Он характеризуется значительным варьированием размеров мышечных волокон, пролиферацией эндомизия и перимизия, признаками дегенерации и регенерации волокон, а также увеличением доли жировой ткани и фиброзом. Гистологическая картина может варьировать в зависимости от конкретной стадии заболевания, степени его тяжести или от обоих факторов одновременно. Так, на ранних этапах болезни может определяться миопатический паттерн без выраженных дистрофических изменений, что сходно с картиной при врождённой миопатии, метаболической миопатии или нейрогенном расстройстве[3].
Биохимический анализ крови: возможно повышение активности креатинфосфокиназы, аспартатаминотрансферазы и аланинаминотрансферазы[8].
Молекулярно-генетический анализ методом секвенирования позволяет выявить мутации в генах, ответственных за развитие ВМД[10].
Дифференциальная диагностика
Осложнения
К возможным осложнениями ВМД относятся[10]:
- хроническая дыхательная недостаточность, вторичная по отношению к мышечной слабости, часто приводит к ателектазам, аспирации и пневмониям, связанным с проведением искусственной вентиляции лёгких;
- кардиомиопатия может быть частым сопутствующим состоянием, что ведёт к развитию хронической сердечной недостаточности, требующей медикаментозной терапии;
- у пациентов может развиваться сколиоз вследствие обездвиженности, остеопения и повышенный риск переломов. Также могут формироваться пролежни и контрактуры суставов, даже несмотря на активную физиотерапию;
- надпочечниковая недостаточность;
- у части пациентов могут возникать судороги. Кроме того, у пациентов с хроническим заболеванием высок уровень психологических расстройств, таких как депрессия и тревожность.
Лечение
Специфической терапии, направленной на причину заболевания, при ВМД не существует. Поэтому лечение носит в основном симптоматический и поддерживающий характер и направлено на улучшение качества жизни и увеличение продолжительности жизни пациентов. Стандартная помощь пациентам с ВМД представляет собой комплексный, мультидисциплинарный подход и включает следующие ключевые направления[3]:
- физическая терапия для регулярной профилактики и коррекции контрактур суставов, костных деформаций и сколиоза;
- респираторная поддержка, подразумевающая применение методов неинвазивной вентиляции лёгких для предупреждения и лечения дыхательной недостаточности;
- кардиотропная терапия, направленная на контроль функции сердца и терапию сердечной недостаточности при развитии кардиомиопатии;
- нутритивная поддержка, включающая коррекцию рациона питания и лечение гастроэзофагеального рефлюкса для обеспечения адекватного энергетического баланса, роста и развития;
- лечение инфекций, в первую очередь своевременная терапия респираторных заболеваний;
- а также ортопедическая помощь, которая заключается в использовании ортезов и корсетов, а при необходимости — в проведении хирургической коррекции деформаций опорно-двигательного аппарата.
Активно ведутся исследования по разработке патогенетических методов лечения. На различных стадиях клинических испытаний находятся подходы, основанные на модуляции генетического дефекта, включая регуляцию экспрессии генов и генную терапию. Изучается потенциал препаратов, воздействующих на ключевые звенья патогенеза: антифибротические, антиапоптотические, противовоспалительные средства, а также модуляторы метаболизма и антиоксиданты. Генная терапия с использованием аденоассоциированных вирусов рассматривается как перспективное направление, особенно для таких форм, как LAMA2-ассоциированная ВМД, где решается задача доставки укороченной версии крупного гена[3].
Прогноз
Учитывая, что лечение большинства форм ВМД является поддерживающим, долгосрочный прогноз неблагоприятный. Продолжительность жизни зависит от корреляции между лежащим в основе генетическим дефектом и фенотипом, обусловленным синтезом аномального белка. Наиболее частой причиной заболеваемости и смертности при этих расстройствах являются вторичные дыхательные или сердечные осложнения, развивающиеся вследствие мышечной слабости[10].
Диспансерное наблюдение
Пациенты с ВМД нуждаются в диспансерном наблюдении невролога, ортопеда и кардиолога. Объём и частота диспансерных наблюдений определяется индивидуально[10].
Профилактика
Консультация генетика необходима для профилактики ВМД. Специалист проводит медико-генетическое консультирование семей с отягощённой наследственностью, определяет риск повторения заболевания и информирует о возможностях пренатальной диагностики при планировании беременности[7].
Примечание
Литература
- Topaloğlu H., Poorshiri B. The congenital muscular dystrophies (англ.) // Annals of the Child Neurology Society. — 2024. — Vol. 2. — P. 27—39. — doi:10.1002/cns3.20050.
- Чаусова П. А., Рыжкова О. П., Поляков А. В. Клинико-генетическая характеристика врождённых мышечных дистрофий (часть 1) // Нервно-мышечные болезни. — 2020. — Т. 10, № 1. — С. 10—21. — doi:10.17650/2222-8721-2020-10-1-10-21.