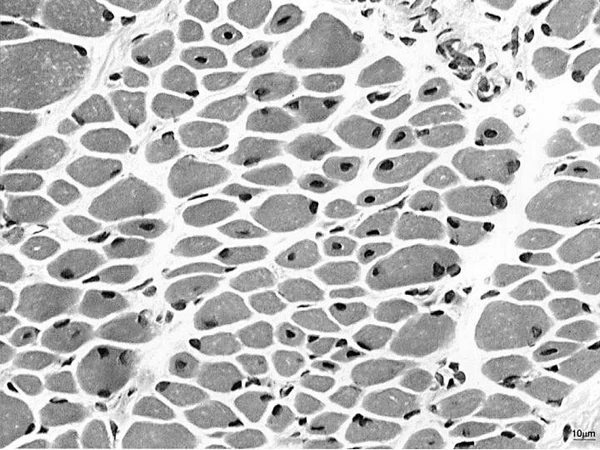
Центронуклеарные миопатии
Центронуклеа́рные миопати́и (ЦНМ) — это генетически гетерогенная группа наследственных нервно-мышечных заболеваний, ключевым диагностическим признаком которых является наличие центрально расположенных ядер в большинстве мышечных волокон. В зависимости от типа наследования и ответственного гена выделяют три основные формы. Х-сцепленная рецессивная форма, или миотубулярная миопатия, обусловлена мутациями в гене MTM1 и протекает наиболее тяжело, преимущественно у мальчиков. Аутосомно-доминантная форма, часто связанная с мутациями в гене DNM2 и проявляющаяся дистальной слабостью, составляет большинство случаев у взрослых. Аутосомно-рецессивная форма, ассоциированная с мутациями в генах BIN1, RYR1, TTN и других, характеризуется умеренным или тяжёлым течением[1][2].
Что важно знать
История
Термин «миотубулярная миопатия» был предложен в 1966 году исследователями во главе со Спиро. Позднее, учёные, обратив внимание на ключевой микроскопический признак — смещение множества ядер в центр мышечного волокна, — предложили использовать термин «центронуклеарная миопатия». В 1985 году на основании анализа всех известных случаев было предложено разделение центронуклеарной миопатии на три генетические формы: аутосомно-доминантную, аутосомно-рецессивную и Х-сцепленную. Последнюю, наиболее тяжёлую форму с ранним началом, дыхательной недостаточностью и неблагоприятным прогнозом, стали называть Х-сцепленной миотубулярной миопатией[3].
Классификация
Согласно международной классификации болезней 11-го пересмотра ЦНМ относится к врождённым миопатиям со структурными аномалиями (8C72.01)[4].
Согласно международной классификации болезней 10-го пересмотра ЦНМ относится к врождённым миопатиям (G71.2)[5].
ЦНМ в зависимости от типа наследования классифицируются следующим образом[1]:
- Х-сцепленная рецессивная форма (миотубулярная миопатия), которая связана с мутациями в гене MTM1;
- аутосомно-доминантная форма, связанная с мутациями в гене DNM2;
- аутосомно-рецессивная форма, ассоциированная с мутациями в генах BIN1, RYR1, TTN и других.
Этиология
ЦНМ характеризуются значительной генетической гетерогенностью и в основном связываются с мутациями в следующих генах[6]:
- X-сцепленные рецессивные мутации в гене MTM1, кодирующем миотубуларин 1;
- аутосомно-доминантные мутации в гене DNM2, кодирующем динамин-2;
- аутосомно-доминантные или рецессивные мутации в гене BIN1, кодирующем белок BIN1;
- аутосомно-рецессивные мутации в гене RYR1, кодирующем рианодиновый рецептор скелетных мышц, и в гене TTN, кодирующем титин.
Также имеются данные об особых фенотипах ЦНМ, связанных с аутосомно-рецессивными мутациями в гене SPEG, кодирующем предпочтительно экспрессируемую в поперечнополосатых мышцах протеинкиназу, и с мутациями в гене CCDC78, кодирующем белок, содержащий спирально-спиральный домен 78[6].
Патогенез
Особенности патогенеза каждой формы ЦНМ связаны с мутациями, вызывающими развитие заболевания[2]:
- патогенез миотубулярной миопатии связан с мутациями в гене MTM1, кодирующими белок миотубуларин. Миотубуларин является фосфоинозитид-фосфатазой, дефосфорилирующей внутриклеточные сигнальные липиды — фосфатидилинозитол-3-фосфат и фосфатидилинозитол-3,5-бисфосфат, ключевые для мембранного транспорта и аутофагии. Дефицит миотубуларина приводит к накоплению этих липидов, что нарушает процессы эндоцитоза, созревания эндолизосом и регуляции аутофагии. В скелетных мышцах это вызывает вторичные структурные аномалии Т-трубочек, саркоплазматического ретикулума и триад, критических для связи возбуждения с сокращением;
- патогенез DNM2-связанной формы: динамин-2 — ГТФазный белок, играющий центральную роль в отщеплении мембранных везикул при эндоцитозе. Мутации нарушают его функцию в мембранном ремоделировании, что приводит к дефектам формирования и функционирования Т-трубочек и саркоплазматического ретикулума, аналогичным наблюдаемым при дефиците миотубуларина. Кроме того, доказаны нарушения в процессе аутофагии, такие как задержка созревания аутофагосом;
- патогенез BIN1-связанной формы: белок амфифизин-2 содержит BAR-домен, ответственный за изгиб мембран, и критически важен для формирования Т-трубочек в мышцах. Мутации, особенно в BAR-домене, нарушают способность белка к тубуляции мембран. Это вызывает структурные аномалии Т-трубочек и неправильную сборку триад, что приводит к нарушению высвобождения кальция из саркоплазматического ретикулума и дефекту связи возбуждения с сокращением;
- патогенез RYR1-связанной формы: в отличие от доминантных мутаций, рецессивные мутации в гене рианодинового рецептора обычно приводят к снижению экспрессии белка RyR1 и вторичному снижению экспресии дигидропиридинового рецептора. Это вызывает первичный дефект связи возбуждения с сокращением. Патогенез характерных гистологических изменений (центральные ядра, атрофия) при этой форме полностью не ясен и, вероятно, не связан напрямую с дефектами мембранного трафика или аутофагии, характерными для других форм, хотя нарушения кальциевого гомеостаза могут косвенно влиять на внутриклеточные пути метаболизма белков;
- патогенез TTN-связанной формы связан с нарушением функций гигантского саркомерного белка титина. Дефект может затрагивать пути, связанные с организацией мембранных структур и внутриклеточной деградацией. Мутации часто вызывают усечение С-концевой части титина, расположенной в М-диске саркомера. Это нарушает несколько критических взаимодействий:
- связь саркомера с саркоплазматическим ретикулумом через белок обскурин, что может влиять на организацию триад;
- сигнальные функции М-диска, включая киназный домен титина, связанный с регуляцией аутофагии и функционирования белков.
- описаны единичные случаи ЦНМ, связанные с другими генами:
- мутации в гене MTMR14, ещё одном члене семейства миотубуларинов, могут способствовать проявлению ЦНМ, иногда в дигенном наследовании с мутацией в DNM2. Патогенез данной формы не определён;
- мутации в гене CCDC78 описаны в одной семье с аутосомно-доминантным наследованием. Патогенез, возможно, связан с триадами, но его точная роль в патогенезе ЦНМ пока не ясна.
Эпидемиология
Точная распространённость ЦНМ неизвестна. Для X-сцепленной формы распространённость оценивается примерно в 1 случай на 50 000 новорождённых мальчиков[6].
Диагностика
Спектр клинических проявлений ЦНМ широк, варьируется в зависимости от генетической формы, но имеет общие характерные черты. Помимо классических симптомов миопатии, часто наблюдаются системные проявления. Возраст начала болезни различен: у пациентов Х-сцепленной формы дебют всегда врождённый, при RYR1 и DNM2 мутациях симптомы чаще всего появляются в детском возрасте, а начало заболевания у пациентов с BIN1 мутацией может сильно варьировать[7].
Нарушения двигательных функций являются центральными для всех форм. К ним относятся задержка развития крупной моторики, мышечная слабость, атрофия мышц и гипотония. Практически все пациенты испытывают эти симптомы. Способность к самостоятельной ходьбе сильно различается: например, пациенты мужского пола с MTM1 мутацией, как правило, не могут ходить самостоятельно, в то время как среди пациентов с BIN1 мутацией не отмечена полная зависимость от помощи или инвалидной коляски[7].
Помимо основной мышечной слабости, пациенты часто страдают от неспецифических симптомов, таких как выраженная утомляемость, непереносимость физической нагрузки, миалгии и судороги. Эти проявления особенно характерны для пациентов с BIN1 мутацией и для женщин-носительниц мутации в гене MTM1. Поражение лицевой и бульбарной мускулатуры (слабость лицевых мышц, птоз, нарушения движений глаз, дисфагия, дизартрия) часто наблюдается у пациентов с RYR1, DNM2 и MTM1 мутациями, причём бульбарные симптомы наиболее выражены при RYR1 мутации[7].
Дыхательная недостаточность наиболее характерна и выражена у пациентов мужского пола с MTM1 мутацией, но также встречается и при других генетических вариантах, за исключением мутации BIN1, где она не описана. Сердечная недостаточность отмечается в небольшом проценте случаев. Другими частыми проявлениями являются ограничение подвижности суставов, часто вследствие контрактур, и сколиоз, который может возникать при любой генетической форме. Также нередки снижение сухожильных рефлексов. Редко определяются различные нарушения мочеиспускания[7].
При гистологическом исследовании мышечных биоптатов наиболее частой находкой являются многочисленные внутренние и центрально расположенные ядра. Также обычными признаками служат повышенная вариабельность размеров мышечных волокон и преобладание волокон первого типа, хотя последний признак не наблюдался у женщин-носительниц мутации в гене MTM1. Увеличение доли жировой или соединительной ткани отмечается в части биоптатов, но не было описано у пациентов с BIN1-формой. Скопления ядер (ядерные клампы) регистрировались только у пациентов с DNM2- и BIN1-мутациями, а также у женщин-носительниц MTM1 мутации. Характерным, хотя и не абсолютно специфичным признаком для DNM2-ассоциированной формы является частое наличие радиальных саркоплазматических тяжей, окружающих центральные ядра. Эти структуры лишь изредка встречаются при других формах ЦНМ и у носительниц мутации MTM1. Ядроподобные структуры наблюдались преимущественно у пациентов с мутациями в гене RYR1. Иногда у женщин-носительниц мутации MTM1 могут быть обнаружены так называемые «ожерельные» волокна[7].
Биохимический анализ крови: характерно повышение активности креатинфосфокиназы[7].
Молекулярно-генетический анализ методом секвенирования позволяет выявить конкретные мутации в зависимости от типа наследования[7].
Электрокардиография и эхокардиография позволяют выявить нарушения проводимости и структурные изменения сердца при вовлечении миокарда[8].
Дифференциальная диагностика
Дифференциальная диагностика проводится с другими формами врождённых миопатий (например, немалиновая миопатия, миопатия Бетлема), а также с иными нервно-мышечными патологиями, протекающими с синдромом выраженной мышечной гипотонии[6].
Осложнения
Возможными осложнениями ЦНМ являются[8]:
- хроническая дыхательная недостаточность, ведущая к ателектазам и аспирационной пневмонии;
- кардиомиопатия и сердечная недостаточность;
- развитие сколиоза, остеопении, контрактур суставов и пролежней;
- судороги;
- высокий риск развития депрессии и тревожных расстройств.
Лечение
Лечение ЦНМ является симптоматическим и поддерживающим, направленным на устранение конкретных проявлений у каждого пациента. Основными направлениями терапии являются респираторная поддержка и коррекция питания. В зависимости от тяжести состояния пациентам может требоваться постоянная или периодическая (например, во время сна) респираторная поддержка с использованием инвазивных или неинвазивных методов вентиляции. При выраженных затруднениях глотания и питания может быть установлена гастростома. Важную роль играет физиотерапия для поддержания мышечной силы и предотвращения контрактур суставов. При развитии сколиоза рассматривается возможность хирургической коррекции. Особое внимание уделяется пациентам с мутациями в гене RYR1 из-за потенциального риска злокачественной гипертермии[9].
Ведутся исследования новых терапевтических подходов. Изучается применение ингибиторов ацетилхолинэстеразы, показавших улучшение мышечной силы. Также исследуется потенциальная польза сальбутамола при RYR1-ассоциированных миопатиях. Перспективным направлением является генная терапия, целью которой является замена дефектного гена функциональной копией для выработки нормального белка, однако этот метод пока находится на стадии разработки[9].
Прогноз
Прогноз при ЦНМ вариабелен и в значительной степени зависит от генетической формы заболевания. Наиболее тяжёлое течение характерно для X-сцепленной миотубулярной миопатии, которая зачастую приводит к летальному исходу в младенческом возрасте. Аутосомно-доминантные формы, связанные с мутациями в гене DNM2, а также ряд случаев аутосомно-рецессивной формы, вызванной мутациями в гене BIN1, как правило, имеют значительно более благоприятный прогноз. Для этих пациентов характерно более медленное прогрессирование заболевания, большая продолжительность жизни и сохранение двигательных функций по сравнению с X-сцепленной формой[6].
Диспансерное наблюдение
Пациенты с ЦНМ нуждаются в диспансерном наблюдении педиатра, пульмонолога, кардиолога, невролога и ортопеда. Объём и частота диспансерных наблюдений определяется индивидуально[9].
Профилактика
Генетическое консультирование является ключевой профилактической мерой для семей пациентов с ЦНМ. Оно позволяет определить тип наследования заболевания и оценить риск его повторного появления в семье[9].
Примечания
Литература
- Reumers S. F. I., Erasmus C. E., Bouman K. et al. Clinical, genetic, and histological features of centronuclear myopathy in the Netherlands (англ.) // Clinical Genetics. — 2021. — December (vol. 100, no. 6). — P. 692—702. — doi:10.1111/cge.14054.
- Новикова Л. Б., Акопян А. П., Шарапова К. М. и др. Миотубулярная Х-сцепленная миопатия // Российский неврологический журнал. — 2023. — Т. 28, № 3. — С. 44—49. — doi:10.30629/2658-7947-2023-28-3-44-49.