Врожденные миастенические синдромы
Врождённые миастени́ческие синдро́мы (ВМС) — это гетерогенная группа наследственных заболеваний, возникающих вследствие патогенных вариантов в генах зародышевой линии, которые экспрессируются в нервно-мышечном синапсе и приводят к нарушению передачи нервно-мышечного импульса. На сегодня известно около 40 генов, мутации в которых могут вызывать ВМС. Дебют заболевания чаще всего происходит в неонатальном периоде или на первых годах жизни, но в отдельных случаях первые симптомы могут проявиться в подростковом или взрослом возрасте, при этом у части пациентов возможен феномен временного ослабления симптомов после неонатального дебюта с последующим рецидивом позже. Клиническая картина отличается значительным разнообразием даже внутри одной семьи и может включать мышечную слабость, патологическую мышечную утомляемость, гипоплазию мышц, а также малые лицевые аномалии (например, низко посаженные уши, высокое готическое нёбо). Тяжесть и течение заболевания крайне вариабельны и определяются конкретным генетическим дефектом[1][2].
Что важно знать
| Врожденные миастенические синдромы | |
|---|---|
| МКБ-11 | 8C61 |
| МКБ-10 | G70.0, G70.2, G70.8, G70.9 |
| МКБ-10-КМ | G70.0, G70.2, G70.8, G70.9 |
| OMIM | 617143 619461 616224 616325 616326 616330 616720 617239 254190 254210 254300 601462 603034 605809 608930 608931 610542 614198 614750 615120 616040 616227 616228 616304 616313 616314 616321 616322 616323 616324 |
| MeSH | D020294 |
История
Самое раннее описание ВМС было сделано Ротбартом в 1937 году, в то время как сам термин «врождённая миастения» был введён Боуменом для описания младенца с нормальными родителями, чьи миастенические симптомы сохранялись в детском возрасте. ВМС были признаны самостоятельными клиническими единицами с 1970-х годов, после того как впервые были описаны аутоиммунные механизмы миастении гравис и синдрома Ламберта — Итона[3][4].
Классификация
| Классификация ВМС[5] | ||
|---|---|---|
| Основная категория ВМС | Подтип ВМС | Ген(ы) |
| Постсинаптические ВМС | Дефицит ацетилхолинового рецептора (АХР) | CHRNA1, CHRNB1, CHRND, CHRNE |
| Медленноканальный ВМС | CHRNA1, CHRNB1, CHRND, CHRNE | |
| Быстроканальный ВМС | CHRNA1, CHRNB1, CHRND, CHRNE | |
| Дефект пути кластеризации АХР | RAPSN | |
| DOK7 | ||
| LRP4 | ||
| MUSK | ||
| Дефицит плектина | PLEC | |
| Дефект потенциал-зависимого натриевого канала скелетных мышц | SCN4A | |
| Синаптические ВМС | Дефицит ацетилхолинэстеразы концевой пластинки | COLQ |
| COL13A1 | ||
| Дефекты пути кластеризации АХР | AGRN | |
| Пресинаптические ВМС | Дефект синтеза ацетилхолина | CHAT |
| Дефекты рециклинга ацетилхолина | SLC5A7 | |
| Дефекты рециклинга ацетилхолина | SLC18A3 | |
| Дефекты экзоцитоза синаптических везикул | SNAP25 | |
| VAMP1 | ||
| SYT2 | ||
| PREPL | ||
| Дефекты аксонального транспорта | MYO9A | |
| Дефект митохондриального переносчика цитрата | SLC25A1 | |
| Пре- и постсинаптические ВМС | Поясно-конечностные мышечные дистрофии с дефицитом гликозилирования | ALG2, ALG14 |
| DPAGT1, GFPT1, GMPPB | ||
Этиология
ВМС вызваны патогенными вариантами в генах зародышевой линии, которые экспрессируются в нервно-мышечном синапсе, и характеризуются нарушением нервно-мышечной передачи сигнала. На сегодняшний день патогенные варианты, приводящие к ВМС, идентифицированы в 40 генах. Все формы ВМС, за исключением пяти, обусловлены вариантами с потерей функции и наследуются по аутосомно-рецессивному типу. Аутосомно-доминантный тип наследования или гемиаллельные de novo варианты наблюдаются при медленноканальном ВМС, а также при ВМС, ассоциированных с генами PURA, PTPN11, SNAP25 и у части пациентов с вариантами в гене SYT2[2].
Патогенез
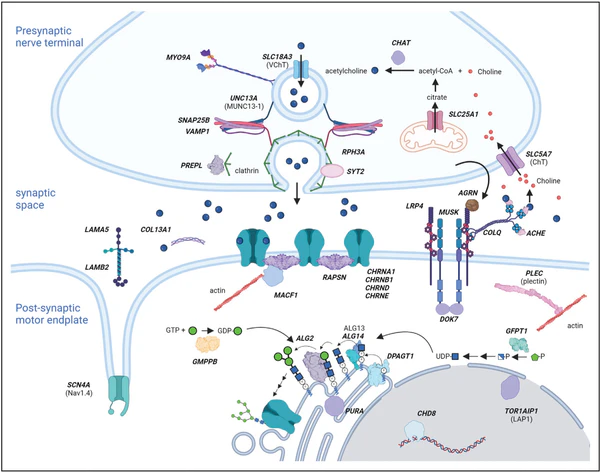
В основе всех ВМС лежит единый патофизиологический итог: стойкое нарушение передачи сигнала с нерва на мышцу в синапсе. Ключевым звеном является недостаточность концевой пластиночки — снижение амплитуды её потенциала до уровня, который не может запустить потенциал действия в мышечном волокне. Эта недостаточность формируется через несколько взаимосвязанных механизмов, которые являются следствием мутаций в генах, отвечающих за нормальную работу синапса. Патологические варианты затрагивают белки, необходимые на всех этапах синаптической передачи[6]:
- На пресинаптической стороне (нервное окончание): нарушается синтез нейромедиатора ацетилхолина (АХ), его упаковка в синаптические пузырьки или процесс высвобождения в синаптическую щель. Это приводит к уменьшению количества молекул АХ в каждом сигнальном «кванте» или снижает вероятность его выброса.
- На постсинаптической стороне (мышечное волокно): нарушается количество или функция ацетилхолиновых рецепторов. Рецепторов может быть слишком мало на мембране, либо их ионные каналы работают неправильно — открываются слишком кратко (не успевая создать сигнал) или, наоборот, слишком долго (вызывая чрезмерную деполяризацию и «усталость» синапса — десенситизацию).
- В синаптической щели и структуре синапса: страдают белки, ответственные за архитектуру и стабильность нервно-мышечного соединения, что вторично нарушает как высвобождение медиатора, так и работу рецепторов.
Таким образом, несмотря на генетическое разнообразие (мутации в более чем 40 генах), конечный путь сводится к одному — мышечное волокно перестаёт получать достаточно сильный электрический сигнал от нерва. Конкретный поражённый ген и тип мутации определяют вариабельность заболевания: возраст начала, тяжесть симптомов, вовлечение определённых групп мышц и ответ на терапию[6].
Эпидемиология
Распространённость ВМС составляет в среднем 2,2 случая на один миллион человек в общей популяции. Данная оценка получена на основе эпидемиологических исследований, проведённых в ряде стран: в Бразилии и Испании этот показатель равен 1,8 на миллион, в Австрии — 3,1 на миллион, а в Бельгии — 3,2 на миллион. Среди детского и подросткового населения (в возрасте до 18 лет) распространённость значительно выше. В Великобритании она составляет 9,2 случая на миллион, в Словении — 22,2 на миллион, а в Австрии — 10,5 на миллион. Средневзвешенное значение для этой возрастной группы достигает 9,7 случаев на миллион человек[2].
Диагностика
Классическим проявлением ВМС является патологическая утомляемость и слабость скелетных мышц, которая ограничивает работу глазодвигательных, бульбарных мышц и мускулатуры конечностей. Дебют заболевания обычно происходит при рождении, в неонатальном периоде или в раннем детстве, чаще всего в первые два года жизни, хотя в редких случаях первые симптомы могут появиться во втором-третьем десятилетии. В своей классической форме ВМС затрагивает исключительно поперечнополосатую мускулатуру, не вовлекая сердечную и гладкую мускулатуру; при этом когнитивные функции, координация, чувствительность и сухожильные рефлексы остаются в норме. Однако при некоторых подтипах миастения является лишь одним из элементов более тяжёлого и комплексного клинического спектра[5].
При неонатальном дебюте симптомы могут проявляться уже при рождении. У новорождённых частыми признаками являются дыхательная недостаточность, внезапные эпизоды апноэ и цианоза, а также множественные контрактуры суставов (артрогрипоз), возникающие из-за недостаточной подвижности плода в утробе матери. Другими значимыми находками в неонатальном периоде могут быть трудности с кормлением, слабый сосательный рефлекс и крик, попёрхивание, птоз век, а также слабость лицевой, бульбарной и скелетной мускулатуры. Стридор в младенчестве может служить важным диагностическим ключом. У некоторых пациентов также отмечаются характерные черты лица: удлинённая форма, узкая челюсть и высокое готическое нёбо[5].
При дебюте в детском возрасте у пациентов наблюдается аномальная мышечная утомляемость, которая выражается в трудностях при беге или подъёме по лестнице, может отмечаться задержка моторного развития. Типичными являются флюктуирующий или фиксированный птоз одного или обоих век, слабость глазодвигательных мышц. Также возможны слабость лицевой и бульбарной мускулатуры с гнусавостью голоса, нарушениями кашлевого рефлекса и глотания. Со временем могут развиться деформации позвоночника и атрофия мышц[5].
Отдельной клинической формой является поясно-конечностная миастения, для которой характерен специфический паттерн слабости с преимущественным поражением мышц плечевого и тазового пояса, утиной походкой и птозом, но обычно без нарушений движений глаз[5].
Тяжесть и течение болезни сильно варьируются: от незначительных симптомов до прогрессирующей инвалидизирующей слабости. Для определённых подтипов ВМС характерны относительно лёгкие миастенические симптомы, но при этом возможны внезапные, резкие обострения слабости или даже эпизоды дыхательной недостаточности, спровоцированные лихорадкой, инфекциями или эмоциональным возбуждением[5].
Ритмическая стимуляция нерва: стандартный диагностический критерий — снижение амплитуды суммарного мышечного потенциала действия (СМПД) на 10 % и более при стимуляции частотой 2-3 Гц, что служит прямым признаком нарушения нервно-мышечной передачи. Для отдельных подтипов ВМС характерны особые электрофизиологические паттерны. Так, при некоторых формах (медленноканальный ВМС, а также COLQ- и PURA-ассоциированные ВМС) одиночный стимул может вызывать повторяющийся СМПД, однако этот феномен быстро исчезает после короткой серии стимулов или произвольного мышечного сокращения. Диагностический поиск также требует анализа специфических ответов на стимуляцию. При SCN4A-ВМС характерный декремент часто выявляется только при использовании высокочастотной стимуляции. Для ВМС, обусловленных нарушением рециклинга ацетилхолина (CHAT, SLC18A3, SLC5A7, PREPL), паттерн ответа может быть вариабельным: у одних пациентов декремент на низких частотах регистрируется в покое, а у других — только после предварительной физической нагрузки или высокочастотной стимуляции. Особый и важный для дифференциальной диагностики паттерн наблюдается при ВМС, клинически напоминающих синдром Ламберта — Итона (SYT2, VAMP1, UNC13A, RPH3A, LAMA5). Для этих форм характерно сочетание декрементного ответа на низкочастотную стимуляцию с инкрементным ответом (то есть нарастанием амплитуды СМПД) на высокочастотную стимуляцию[6].
Магнитно-резонансная томография: характерен фиброз и жировая инфильтрация скелетных мышц[6].
Гистологическое исследование биоптата мышечной ткани: определяются характерные структурные изменения при некоторых генетических подтипах врождённых миастенических синдромов, связанных с дефектами гликозилирования. В частности, при ВМС, ассоциированных с мутациями в генах GFPT1, DPAGT1 и ALG2, в мышечной ткани могут обнаруживаться тубулярные агрегаты или вакуоли с ободком. Однако эти патологические находки непостоянны и не наблюдаются при всех подтипах: они отсутствуют при ВМС, вызванных мутациями в ALG14 или GMPPB. При медленноканальном ВМС развивается концевая миопатия, которая при световой микроскопии может проявляться как тубулярные агрегаты, а при электронной микроскопии — как включения, напоминающие тельца при миозите с включениями[6].
Биохимический анализ крови: возможно повышение концентрации креатинфосфокиназы[6].
Молекулярно-генетический анализ методом секвенирования позволяет выявить мутацию в конкретном гене в зависимости от типа ВМС[5].
Дифференциальная диагностика
Дифференциальная диагностика ВМС проводится со следующими заболеваниями[5]:
- миастения;
- спинальная мышечная атрофия;
- врождённые мышечные дистрофии;
- врождённые миопатии;
- митохондриальные миопатии;
- врождённые нарушения гликозилирования;
- синдром Мёбиуса;
- аномалии ствола мозга;
- болезни двигательного нейрона;
- поясно-конечностные мышечные дистрофии;
- лице-лопаточно-плечевая мышечная дистрофия;
- митохондриальная миопатия и хроническая прогрессирующая наружная офтальмоплегия;
- аутосомно-доминантная прогрессирующая наружная офтальмоплегия.
Лечение
Лечение ВМС основано на применении ряда препаратов, направленных на улучшение передачи сигнала в нервно-мышечном синапсе. Ключевыми лекарственными средствами являются[6]:
- ингибиторы холинэстеразы эффективны при многих формах, особенно при дефиците ацетилхолиновых рецепторов, однако они, как правило, не помогают при медленноканальном ВМС и DOK7-ВМС. Более того, их применение противопоказано при COLQ-ВМС и LAMB2-ВМС из-за риска тяжёлых побочных эффектов, включая остановку дыхания. В ряде случаев эти препараты могут ухудшать состояние пациентов с DOK7-, MUSK- и LRP4-ассоциированными синдромами;
- эфедрин и сальбутамол оказывают положительный эффект при широком спектре ВМС. Их действие, вероятно, связано со стимуляцией симпатической иннервации синапса. Они также могут приносить пользу отдельным пациентам с медленноканальным и COLQ-ВМС, компенсируя вторичный дефицит рецепторов;
- амифампридин блокирует калиевые каналы нервного окончания, усиливая выброс ацетилхолина. Это препарат выбора для ВМС, напоминающих синдром Ламберта — Итона, а также эффективен при многих других формах, за исключением медленноканального ВМС, AGRN-, SLC5A7- и SLC25A1-ВМС. Отмечена его польза и при некоторых случаях COLQ-ВМС;
- для лечения специфической формы — медленноканального ВМС — применяются хинидин и флуоксетин, которые укорачивают патологически длинное открытие рецепторов. Действие флуоксетина, однако, неоднозначно: он может ухудшать состояние при RAPSN-ВМС, но в одном случае помог при COLQ-ВМС;
- ацетазоламид показал эффективность у части пациентов с SCN4A-ВМС.
Прогноз
Тяжесть и течение ВМС крайне вариабельны и напрямую зависят от лежащего в основе генетического дефекта. Клинический спектр простирается от незначительных симптомов, таких как лёгкая непереносимость физической нагрузки, до прогрессирующей инвалидизирующей мышечной слабости. Важно отметить, что даже на фоне слабовыраженных миастенических проявлений у пациентов могут возникать внезапные эпизоды резкого ухудшения состояния или дыхательной недостаточности. Такие кризы часто провоцируются лихорадкой, инфекциями или эмоциональным возбуждением[5].
Диспансерное наблюдение
Для пациентов с ВМС рекомендуется регулярное наблюдение, включающее оценку мышечной силы и функции внешнего дыхания. Периодичность такого мониторинга обычно составляет не реже одного раза в шесть месяцев для детей и не реже одного раза в двенадцать месяцев для взрослых. Особое внимание следует уделять контролю дыхательной функции, поскольку у части пациентов, в особенности с патогенными вариантами в генах COLQ и DOK7, с возрастом может развиваться медленно прогрессирующая дыхательная недостаточность. В рамках наблюдения необходимо активно выявлять симптомы ночной гиповентиляции, такие как беспокойный сон, дневная сонливость, утренние головные боли или чувство удушья ночью[5].
Профилактика
Не разработана.
Примечания
Литература
- Ohno K., Ohkawara B., Shen X.-M., et al. Clinical and Pathologic Features of Congenital Myasthenic Syndromes Caused by 35 Genes—A Comprehensive Review (англ.) // International Journal of Molecular Sciences. — 2023. — Vol. 24, no. 4. — P. 3730. — doi:10.3390/ijms24043730.
- Engel A. G., Shen X. M., Selcen D., Sine S. M. Congenital myasthenic syndromes: pathogenesis, diagnosis, and treatment (англ.) // Lancet Neurology. — 2015. — April (vol. 14, no. 4). — P. 420—434. — doi:10.1016/S1474-4422(14)70201-7.
- Ohno K., Ito M., Ohkawara B. Review of 40 genes causing congenital myasthenic syndromes (англ.) // Journal of Human Genetics. — 2025. — doi:10.1038/s10038-025-01355-9.