Т-клеточный лейкоз из больших гранулярных лимфоцитов
Т-кле́точный лейко́з из больши́х грануля́рных лимфоци́тов (ТКЛ) — это редкое клональное заболевание, характеризующееся пролиферацией больших гранулярных лимфоцитов. Это приводит к инфильтрации костного мозга лимфоцитами, что вызывает цитопению, наиболее выраженную в виде нейтропении. Большие гранулярные лимфоциты представляют собой особый подтип лимфоидных клеток, которые крупнее обычных циркулирующих лимфоцитов и обладают характерными азурофильными гранулами, содержащими кислые гидролазы. В норме они составляют 10-15 % от общего количества мононуклеарных клеток периферической крови. Большинство пациентов с этим лейкозом клинически бессимптомны, и заболевание имеет тенденцию к хроническому течению. Хотя в конечном итоге многим пациентам требуется лечение из-за тяжёлой или симптоматической нейтропении, анемии или лимфопении. Лечение основывается на иммуносупрессивной терапии[2].
Общие сведения
История
ТКЛ был впервые описан в 1975-77 годах как хронический лимфоцитарный лейкоз Т-клеточного происхождения, ассоциированный с нейтропенией и спленомегалией. Впоследствии, в 1989 году, он был переименован в лейкоз из больших гранулярных лимфоцитов в связи с тем, что в его основе лежит клональная пролиферация этих клеток. Таким образом, данный лейкоз сформировался как редкое гетерогенное клональное лимфопролиферативное заболевание зрелых посттимических Т-клеток или натуральных киллеров[3][4].
Этиология
Точная причина клональной пролиферации больших гранулярных лимфоцитов неизвестна. Считается, что в основе развития лейкоза лежит дисрегуляция путей, отвечающих за гибель клеток, индуцированную активацией. В результате аномальной клональной пролиферации происходит выживание и накопление зрелых больших гранулярных лимфоцитов, которые, будучи первоначально активированы антигеном, смогли избежать запрограммированной клеточной гибели. Эти лейкемические клетки продолжают функционировать как клетки-киллеры и эффекторные Т-клетки памяти[3].
ТКЛ часто ассоциирован с аутоиммунными заболеваниями, например, ревматоидный артрит и синдром Шегрена, хотя также сообщается о связи с системной красной волчанкой и тиреоидитом Хашимото[2].
Патогенез
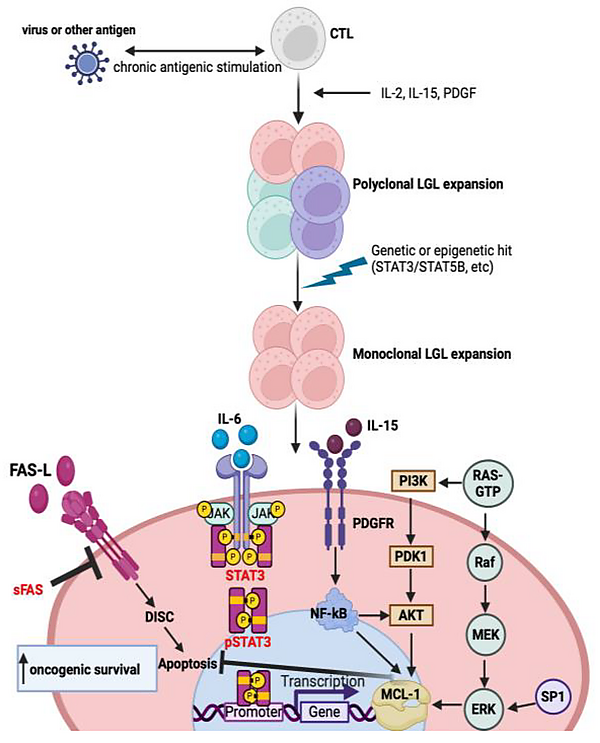
Патогенез ТКЛ связан с хронической антигенной стимуляцией и нарушением механизмов запрограммированной клеточной гибели (апоптоза), что приводит к выживанию и клональной экспансии больших гранулярных лимфоцитов. Основными механизмами в патогенезе заболевания являются[3][5]:
- антиген-индуцированная активация: пусковым механизмом может служить хроническая вирусная инфекция. Установлена связь заболевания с вирусами, например, Т-лимфотропный вирус человека 1-го типа, вирус гепатита С, вирус Эпштейна — Барр и цитомегаловирус;
- роль цитокинов: ключевую роль в активации и выживании больших гранулярных лимфоцитов играют цитокины, в частности интерлейкины и тромбоцитарный фактор роста. Интерлейкин 15 активирует сигнальные пути JAK-STAT и MAPK, что подавляет апоптоз. Тромбоцитарный фактор роста через рецептор тирозинкиназы активирует пути PI3K-AKT и MAPK, способствуя длительному выживанию клеток;
Важным звеном патогенеза является нарушение функционирования молекулярных путей[3][5]:
- путь JAK-STAT3: это центральное звено патогенеза. Мутации в гене STAT3 встречаются у 30-40 % пациентов и приводят к постоянной активации пути, что способствует выживанию больших гранулярных лимфоцитов;
- FAS/FAS-L путь: в норме этот путь обеспечивает гибель активированных лимфоцитов после выполнения их функции (активационно-индуцированная клеточная смерть). Однако большие гранулярные лимфоциты устойчивы к этому механизму. Одновременно повышенный уровень Fas-лиганда может вызывать апоптоз предшественников нейтрофилов в костном мозге, что объясняет характерную для пациентов нейтропению;
- путь RAS-RAF-MEK-ERK: его сверхактивация способствует выживанию больших гранулярных лимфоцитов. Блокада этого пути может восстановить чувствительность лейкемических клеток к апоптозу через FAS;
- путь PI3K/AKT: его повышенная активность в больших гранулярных лимфоцитах напрямую связана с ингибированием апоптоза;
- путь NF-KB: активируясь, этот путь усиливает экспрессию антиапоптотических белков семейства Bcl-2, независимо от STAT3;
- сфинголипидный путь: в больших гранулярных лимфоцитах нарушен баланс между проапоптотическим метаболитом церамидом и сфингозин-1-фосфатом. Повышенная концентрация сфингозин-1-фосфата способствует выживанию клеток, а ингибирование фермента, превращающего церамид в сфингозин, может индуцировать апоптоз больших гранулярных лимфоцитов.
Эпидемиология
ТКЛ представляет собой редкое заболевание, на которое приходится от 2 до 5 % всех хронических лимфопролиферативных заболеваний в США и Европе и около 5-6 % случаев среди азиатской популяции. Средняя ежегодная заболеваемость оценивается в 0,2-0,72 случая на миллион человек. Заболевание с одинаковой частотой встречается у мужчин и женщин. Средний возраст пациентов на момент постановки диагноза составляет 55-60 лет, при этом у женщин диагноз обычно устанавливается в более молодом возрасте, чем у мужчин. Наиболее часто болезнь дебютирует в седьмом десятилетии жизни. ТКЛ редко встречается у детей. Согласно данным исследований, от 14 % до 26 % пациентов моложе 50 лет на момент диагностики[2][4].
Диагностика
Клиническая картина ТКЛ отличается вариабельностью, при этом около трети пациентов на момент диагностики не предъявляют жалоб. Наиболее характерным симптомом является усталость, которая наблюдается более чем у половины больных. Ключевые клинические проявления связаны с цитопениями: анемия вследствие парциальной красноклеточной аплазии костного мозга (чаще у пациентов азиатского происхождения) и рецидивирующие инфекции. Инфекции в типичных случаях поражают кожу, ротоглотку, придаточные пазухи и параректальную область, но могут так же быть в виде тяжёлых пневмоний или сепсиса. В-симптомы (лихорадка, ночная потливость, потеря веса) нетипичны[3].
При агрессивном течении, которое чаще встречается у молодых пациентов азиатского происхождения, наблюдается более тяжёлая клиническая картина с гепатомегалией, лимфаденопатией, кожными поражениями, серозными выпотами. Заболевание может осложняться коагулопатией, гемофагоцитарным синдромом и полиорганной недостаточностью[3].
Клинический анализ крови: могут быть явления лимфоцитоза, нейтропении, анемии и тромбоцитопении. Патогномоничным является обнаружение больших гранулях лимфоцитов в количестве более 0,5 × 109/л[3].
Иммуноферментный анализ: возможно повышение концентрации ревматоидного фактора, антинейтрофильных антител, бета-2-микроглобулина, Fas-лиганда, повышения активности лактатдегидрогеназы, гипергаммаглобулинемия[3].
Микроскопия мазка крови: большие гранулярные лимфоциты имеют большой размер, обильную цитоплазму с типичными азурофильными гранулами и почковидное или круглое ядро со зрелым хроматином[5].
Гистологическое исследование биоптата костого мозга: наблюдается преимущественно интерстициальная и интрасинусоидальная инфильтрация CD8+ T-лимфоцитами, которая сочетается с наличием реактивной (незлокачественной) лимфоидной популяции, состоящей из поликлональных B- и T-клеток. Клетки миелоидного ряда могут демонстрировать признаки блокады созревания. Клетки эритроидного ряда обычно увеличены в количестве[3].
Иммуногистохимический исследование биоптата костного мозга: ТКЛ зрелым посттимическим фенотипом. В подавляющем большинстве случаев эти опухолевые клетки имеют фенотип CD3+, TCR αβ+, CD4-, CD5dim, CD8+, CD16+, CD27-, CD28-, CD45R0-, CD45RA+ и CD57+, что соответствует фенотипу конститутивно активированной Т-клетки. Вариация Т-клеточного лейкоза с фенотипом CD3+/CD56+ может ассоциироваться с более агрессивным течением заболевания и мутациями в гене STAT5B[5].
Дифференциальная диагностика
Дифференциальная диагностика проводится со следующими заболеваниями[2][3]:
- реактивная пролиферация больших гранулярных лимфоцитов;
- Т-клеточная лимфома;
- синдром Шегрена;
- парциальная красноклеточная аплазия;
- гепатоспленальная Т-клеточная лимфома;
- аутоиммунная гемолитическая анемия.
Лечение
Стандартной терапии первой линии для ТКЛ из-за отсутствия масштабных клинических исследований не существует. Основным подходом к лечению является длительная иммуносупрессивная терапия, направленная против цитотоксических лимфоцитов. Лечение обычно назначается при наличии тяжёлых цитопений или сопутствующих аутоиммунных заболеваний. К терапии первой линии относятся такие препараты, как метотрексат, циклофосфамид и циклоспорин. Метотрексат часто является предпочтительным выбором при нейтропении и сопутствующем ревматоидном артрите, в то время как циклофосфамид может быть более эффективен при сопутствующей парциальной красноклеточной аплазии. Циклоспорин может применяться как самостоятельно, так и в комбинации с метотрексатом. Ответ на лечение оценивается не ранее чем через несколько месяцев, а общие показатели ответа на терапию первой линии варьируются в широких пределах[2].
При рефрактерном или резистентном заболевании применяется терапия второй линии. К ней относятся сиролимус и алемтузумаб. Также могут использоваться антитимоцитарный иммуноглобулин, ритуксимаб и режимы на основе флударабина. В отдельных случаях может рассматриваться спленэктомия, особенно при симптоматической спленомегалии, или трансплантация гемопоэтических стволовых клеток[2].
Перспективным направлением является разработка таргетной терапии. Изучаются ингибиторы JAK-киназ (руксолитиниб, тофацитиниб), антагонисты интерлейкина-6 и ингибиторы протеасом. Также в разработке находятся моноклональные антитела, нацеленные на различные мишени на поверхности лимфоцитов или блокирующие ключевые цитокины. Особый интерес представляют препараты, направленные на подавление сигнальных путей STAT3 и STAT5, которые играют ключевую роль в выживании злокачественных клеток при этом заболевании[2].
Прогноз
Пациенты с ТКЛ обычно имеют благоприятный прогноз и вялотекущее течение болезни. На начальном этапе большинство из них не нуждаются в активном лечении и находятся под динамическим наблюдением. Терапия требуется лишь при появлении симптомов. Причиной смерти в этих случаях обычно являются не прогрессирование самого лейкоза, а тяжёлые инфекции, развивающиеся на фоне нейтропении. Согласно данным, лишь около 2 % пациентов умирают непосредственно от прогрессирования заболевания, в то время как около 4 % — от тяжёлых инфекционных осложнений. Общая пятилетняя выживаемость составляет примерно 75 %[3].
Примечания
Литература
- Ullah F., Markouli M., Orland M., Ogbue O., Dima D., Omar N., Mustafa Ali M.K. Large Granular Lymphocytic Leukemia: Clinical Features, Molecular Pathogenesis, Diagnosis and Treatment (англ.) // Cancers. — 2024. — Vol. 16, no. 7. — P. 1307. — doi:10.3390/cancers16071307.
- Rahul E., Ningombam A., Acharya S., Tanwar P., Ranjan A., Chopra A. Large granular lymphocytic leukemia: a brief review (англ.) // American Journal of Blood Research. — 2022. — 15 February (vol. 12, no. 1). — P. 17—32. — PMID 35291253.
- Федулова М.В., Куприянов Д.Д. Судебно-гистологическая диагностика редкого Т-клеточного лейкоза при производстве повторной экспертизы // Судебно-медицинская экспертиза. — 2023. — Т. 66, № 3. — С. 56—58. — doi:10.17116/sudmed20236603156.
- Чернова Н.Г., Сидорова Ю.В., Захарько Е.И. и др. Проточная цитометрия и ПЦР-исследование Т-клеточной клональности в разграничении опухолевой и реактивной пролиферации больших гранулярных лимфоцитов // Гематология и трансфузиология. — 2018. — № 2.