Инсулиноподобный фактор роста 1
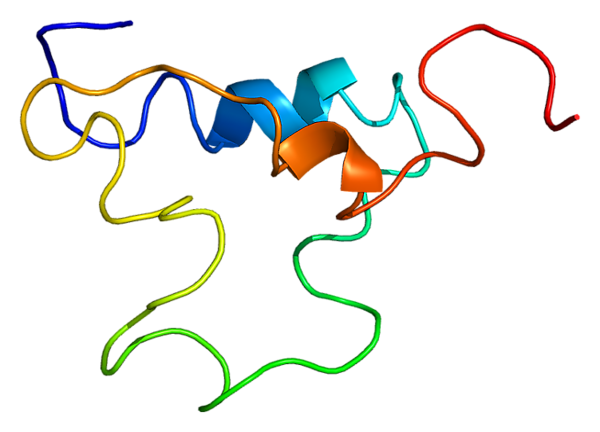
Инсулиноподобный фактор роста 1 (ИФР-1, соматомедин С, англ. insulin-like growth factor 1, IGF1) — белок из семейства инсулиноподобных факторов роста, по структуре и функциям похожий на инсулин. Он участвует в эндокринной, аутокринной и паракринной регуляции процессов роста, развития и дифференцировки клеток и тканей организма. ИФР-1 состоит из одной полипептидной цепи длиной 70 аминокислотных остатков с тремя внутримолекулярными дисульфидными мостиками. Молекулярная масса ИФР-1 7,6 кДа[5]. Считается, что этот белок играет активную роль в процессах старения организма: мутации гена ИФР-1 приводили к увеличению продолжительности жизни у лабораторных животных[6].
Инсулиноподобный фактор роста 1 у человека кодируется геном IGF1[7][8].
ИФР-1 является важнейшим эндокринным посредником действия соматотропного гормона, поэтому называется также соматомедином С. ИФР-1 производится гепатоцитами печени в ответ на стимуляцию их соматотропиновых рецепторов. В периферических тканях именно ИФР-1 обеспечивает практически все физиологические эффекты соматотропного гормона. Его последствия были названы «неуправляемой инсулиноподобной деятельностью».
Общие сведения
Действие
ИФР-1 также обеспечивает обратную связь с гипоталамусом и гипофизом по соматотропной оси: от уровня ИФР-1 в крови зависит секреция соматотропин-рилизинг-гормона и соматотропного гормона. При низком уровне ИФР-1 в крови секреция соматотропин-рилизинг-гормона и соматотропина возрастает, при высоком — снижается. Также ИФР-1 регулирует секрецию соматостатина: высокий уровень ИФР-1 приводит к возрастанию секреции соматостатина, низкий — к её снижению. Этот механизм является ещё одним способом регуляции уровня соматотропного гормона в крови. Но действие может быть заторможено недостаточным питанием, нечувствительностью гормона роста, отсутствием реакции рецепторов, или неудачным, ниже необходимого минимума сигнального пути, сообщением рецепторов. В экспериментах на крысах было показано, что концентрация иммунореактивного ИФР-1 в плазме была выше у крыс на казеиновой диете, чем у крыс на диете из соевых бобов или безпротеиновой диете[9]. Также было установлено, что при недостатке ИФР-1 в крови он может продуцироваться в самих мышцах.
Уровень ИФР-1 в крови зависит от действия на печень не только соматотропного гормона, но и половых стероидов и тиреоидных гормонов, глюкокортикоидов, инсулина. При этом инсулин, андрогены, эстрогены повышают секрецию ИФР-1 печенью, а глюкокортикоиды её снижают. Это является одной из причин синергизма инсулина, соматотропина, половых и тиреоидных гормонов в отношении процессов роста и развития организма, роста и дифференцировки тканей, и одной из причин характерного тормозящего действия глюкокортикоидов на процессы линейного роста, полового созревания и пр. ИФР-1 воздействует на развитие всю жизнь, но его уровень в крови не постоянный: наиболее низкий уровень ИФР-1 производства в детстве и в старости, а самый высокий — во время подросткового периода жизни.
История
ИФР-1 как таковой был открыт в 1978 году и спустя 10 лет он стал использоваться спортсменами как элемент подготовки. Он обрел огромную популярность благодаря тому, что совершенно не нуждается в дополнительных подпитках (курсы стероидов, инсулин и т.п.). Но недавно были выведены и побочные эффекты: увеличение печени, селезёнки, количества злокачественных клеток.
ИФР1 каскад
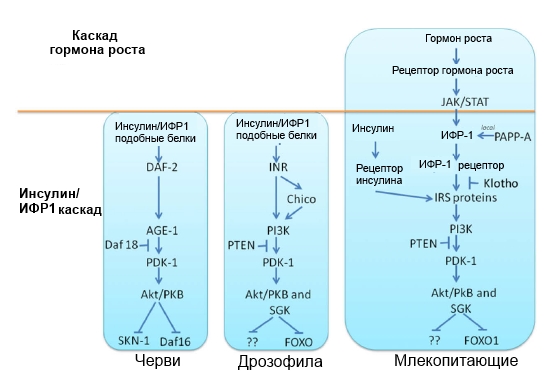
ГР/ИФР1 каскад сильно консервативен у различных групп животных (позвоночных и беспозвоночных). В общих чертах он заключается в том, что ИФР1 через свой рецептор запускает каскад реакций, приводящих к ингибированию факторов транскрипции (DAF-16 у C.elegans или FOXO1 у мышей). Вероятно, эти факторы транскрипции регулируют экспрессию генов, которые увеличивают продолжительность жизни[10].
Если у беспозвоночных животных insulin/ИФР1 — путь один, у высших позвоночных, в том числе, млекопитающих, этот путь подразделяется на два. Эти два пути имеют перекрывающиеся функции, но инсулин главным образом участвует в регуляции метаболизма, а ГР/ИФР1 путь играет важную роль в процессах роста, развития и, возможно длительности жизни[11].
Именно гены ИФР-каскада стали первыми открытыми «генами старения» — то есть генами, повреждение которых привело к увеличению продолжительности жизни[12].
Роль каскада в старении различных животных
Различные животные (позвоночные и беспозвоночные) являются удобными моделями для изучения старения, в связи с их относительно недолгой продолжительностью жизни, возможностью генетических манипуляций и изучением длин их жизни.
Каскад, который регулирует как увеличение продолжительности жизни, так и диапаузу[13], был впервые исследован для нематоды Caenorhabditis elegans. В ответ на неблагоприятные внешние условия этот червь переходит в ювенильную форму, которая называется дауэровской («спящей»). В этой форме Caenorhabditis elegans не происходит развития, размножения. Эта форма становится устойчивой к окислительному стрессу[14]. В организме накапливается жир для запасания энергии. Когда условия среды восстанавливаются, нематода возвращается в состояние фертильных взрослых особей. В dauer — форму может перейти только молодая особь, которая не достигла половой зрелости.
Восстановление условий окружающей среды стимулирует активацию инсулин/ИФР-1 сигнального пути. Если мутировать рецептор инсулина/ИФР-1, daf-2 (или более поздние компоненты каскада, PI3-kinase/PDK/Akt), то Caenorhabditis elegans переходит в dauer-форму даже в удовлетворительных условиях окружающей среды. Инсулин/ИФР-1 каскад направлен на ингибирование белка DAF-16, который является фактором транскрипции блока генов, стимулирующих переход в dauer-форму[13]. Мутации пути, которые приводят к увеличению продолжительности жизни, должны быть слабыми. При сильных мутациях и недостаточной активности инсулин/ИФР1 каскада молодая особь может «застрять» в dauer-форме.
Было показано, что помимо продолжительности жизни, описываемый каскад реакций влияет также на фертильность и движение особей. Некоторые мутанты по daf-2 переходили в ювенильную форму, теряли способность к движению. Однако такие проявления нельзя связывать с продолжительностью жизни, так как существуют долгоживущие мутанты по daf-2, чья подвижность и фертильность нормальна (по сравнению с диким типом). Инсулин/ИФР1 путь может регулировать гормональную сигнализацию организма. У организмов, имеющих мутации гена daf-2 только в определенных линиях, наблюдалась увеличенная продолжительность жизни всего организма[14][15].
Drosophila (плодовая мушка) имеет ряд преимуществ для изучения старения: это животное — хорошо изученный модельный организм с разработанными методами генной инженерии по работе с ним, а также хороший объект для генетического нокаута. Плодовые мушки имеют больше сходных черт с человеком (с млекопитающими), чем Caenorhabditis elegans (нематода), — у них есть головной мозг, сердце, гомологи почек. Также у Drosophila сложное поведение. Однако большинство биологических процессов изучено на эмбриотической стадии и до метаморфоза. Взрослая мушка, модельный объект геронтологии, изучена хуже, чем эмбриональная стадия. Несмотря на это, Drosophila является одним из основных модельных организмов в изучении старения.
Как и для Caenorhabditis elegans, для Drosophila мутации, снижающие эффективность ИФР1 каскада, приводят к увеличению продолжительности жизни. Это было показано путём уменьшения количества инсулин-подобных белков и нокаутом субстратов ИФР — рецептора (chico и Lnk)[6]. В то же время увеличение экспрессии гомолога DAF-16 FOXO(транскрипционного фактора, регулируемого ИФР-каскадом) тоже приводит к увеличению продолжительности жизни мушек. При уменьшении экспрессии другого обратного регулятора FOXO (14-3-3ε) продолжительность мушек также растет.
Нервная система и жировое тело дрозофил вовлечены в регуляцию продолжительности жизни. Так, нейросекреторными клетками вырабатываются некоторые инсулин-подобные белки (ИПБ). При стрессе активируется Jun-N-terminal kinase (киназа), что приводит к сокращению экспрессии некоторых таких белков (ИПБ2 и ИПБ5), и, как следствие, к уменьшению эффективности работы ИФР1-каскада. При активации этой киназы молекулярными методами наблюдается увеличение продолжительности жизни мушек.
В жировом теле (эквиваленты белой жировой ткани и печени у млекопитающих) произошла редукция ИФР1-каскада. Однако в 2004 году было показано, что увеличение экспрессии FOXO способно увеличить продолжительность жизни организма. Механизмы такого влияния требуют дальнейшего изучения[6].
Во всех случаях ингибирования ИФР1-каскада было отмечено, что увеличивается активность генов, участвующих в каскадах клеточной детоксикации.
В описанных ранее опытах было показано, что ингибирование ИФР1-каскада увеличивает продолжительность жизни, однако действительно ли это ингибирование замедляет процесс старения?
Уменьшение активности ИФР1-каскада приводит к снижению фертильности самок, что неудивительно, ведь этот каскад играет одну из ключевых ролей в регуляции роста, пролифирации и выживаемости стволовых клеток — предшественниц яйцеклеток. Однако при ограничении питания мушек дикого типа, что приводит, в том числе, в ограничении работы ИФР1-каскада, увеличивает количество половых клеток.
С другой стороны, при снижении эффективности работы каскада (в совокупности с редукцией TOR-сигнальной цепи) замедляется снижение функций сердца, реже наблюдается отрицательный геотаксис. Для мушек, служащих моделями для изучения болезни Альцгеймера, было показано, что редукция компонентов ИФР1-пути приводила к снижению прогрессии патологии. Аналогичные результаты были показаны для ряда других нейродегенеративных заболеваний (например, болезни Паркинсона)[6][16].
Доказательства влияния ИФР1 каскада на продолжительность жизни были показаны на различных моделях млекопитающих. Хорошим примером могут быть карликовые мутантные мыши, дефицитные по гормону роста.
Карликовые мыши Эймса живут на 50 %, 70 % дольше (самцы, самки), чем мыши "дикого" типа[12]. Эта модель — один из первых примеров способности единичного гена значительно продлевать жизнь у млекопитающих. Аутосомальные рецессивные мутации ведут к гипопитуитаризму, проявляющемуся в снижении синтеза и секреции гормона роста (ГР), пролактина и тиреоидстимулирующего гормона (ТСГ). У этих мышей снижен уровень инсулинподобного фактора роста 1 (IGF-1) и инсулина в крови, повышена чувствительность к инсулину и понижена температура тела. Как самцы, так и самки карликовых мышей бесплодны, у них выражена иммунодепрессия[12]. Показано, что у этих мышей в печени снижен уровень глутатиона и аскорбиновой кислоты и увеличена активность каталазы по сравнению с контролем, что проявляется большей устойчивостью к окислительному стрессу. Частота возникновения спонтанных опухолей у карликовых и нормальных мышей одинакова. Однако карликовые мыши живут значительно дольше, чем нормальные, и возможно, что опухоли развиваются у них позднее.
Карликовые мыши Снелл (Snell), у которых имеется мутация в гене Pit1 (гипофизарно-специфичный транскрипционный фактор 1), регулируемом геном Prop-1, также живут много дольше, чем нормальные мыши, что связывают с дефицитом у них продукции гормона роста. Дефицит гормона роста у карликовых мышей Снелл приводит к снижению секреции инсулина и IGF-1 и снижению передачи сигнала, опосредованного генами рецептора инсулина InR, IRS-1 или IRS-2 и Р13К, вовлеченными в контроль продолжительности жизни. Авторы полагают, что мутация Pit-1 приводит к такому состоянию физиологического гомеостаза, которое благоприятствует долголетию.
У гомозиготных мышей с выключенным геном рецептора гормона роста (GHR-/-) наблюдается некоторое замедление роста, пропорциональная карликовость, уменьшение длины костей и содержания костных минералов, отсутствие рецептора гормона роста и ГР-связывающего белка, значительное уменьшение содержания в крови IGF-1 и связывающего его белка-3 и увеличение в сыворотке крови концентрации ГР. Они живут значительно дольше, чем гетерозиготные (GHR+/-) животные или мыши дикого типа (GHR+/+)[17].
Также у грызунов, которых посадили на диету (ограниченное питание), наблюдалось снижение уровня инсулина и ИФР1. Снижалось количество запасаемого жира, стимулировалась иммунная система. Продолжительность жизни возрастала на 30—40 %[11]. Генетические модели также показали влияние ИФР1 каскада на продолжительность жизни.
Чтобы создать систему для изучения болезни Альцгеймера, в мышах был экспрессирован β-амилоид. У здорового человека идет экспрессия этого белка, и в норме этот белок не токсичен, однако β-амилоид может образовывать димеры и олигомеры, которые обладают нейротоксичностью и вызывают болезнь Альцгеймера. При редукции ИФР1-каскада у мышей наблюдалось агрегирование β-амилоид в более масштабные ансамбли, что уменьшало их токсичность и замедляло процесс развития болезни[18].
По аналогии с другими животными, у млекопитающих ИФР1-каскад негативно регулирует факторы трансляции генов FOXO. FOXO — это сильно консервативное у млекопитающих семейство генов, необходимых для выживания организма в стрессовых условиях. Более того, при редукции ИФР1 сигнала у мышей наблюдалась бОльшая устойчивость к оксидативному стрессу. Таким образом, на мышах, моделированных для изучения болезни Альцгеймера, было показано комплексное влияние ИФР1-каскада на защитные системы организма[18].
В 2009 году было проведено исследование на группе пожилых европеоидов. Исследовали 30 генов insulin/ИФР1-сигнального пути. В ходе этого исследования были найдены SNP, достоверно связанные с продолжительностью жизни. Один из этих SNP был найден в гене AKT1. И еще две SNP в гене FOXO3A были связаны с продолжительностью жизни у женщин.
AKT1 — это одна из тирозинкиназ, которая способна фосфорилировать FOXO3A. Фосфорилированный белок не может проникнуть в ядро и активировать гены семейства FOXO. FOXO3A — это один из трех человеческих гомологов фактору трансляции DAF-16 у Caenorhabditis elegans. Интересно, что SNP, влияющие на продолжительность жизни, были найдены в интронах, функции которых еще не известны[19].
Для человека важную роль играет соотношение ГР/ИФР1. При относительно большом количестве гормона роста (при недостатке ИФР1) могут развиться такие симптомы, как ожирение, умственная отсталость, непереносимость глюкозы (синдром Ларона)[11].
Исследования
Путь ИФР сигнализации имеет патогенную роль в развитии рака. Исследования показали, что при повышенном уровне ИФР усиливается рост раковых клеток[20][21]. Кроме того у людей с синдромом Ларона риск развития рака существенно меньше[22][23]. Изменения в диете, в частности, веганская диета, уменьшающие активность ИФР-1, могут быть связаны с уменьшением риска рака[24]. Однако, несмотря на значительные исследования, противораковые терапии, влияющие на ИФР-1, не показали впечатляющих результатов в клинических испытаниях[21][25][26][27].
Была показана эффективность ИФР-1 при инсульте у мышей в комбинации с эритропоэтином. Были зафиксированы поведенческие и клеточные улучшения[28].
Клинические испытания вещества ибутаморен, которое повышает уровень ИФР-1 у пациентов, не продемонстрировало улучшений симптомов болезни Альцгеймера[29]. Другое исследование продемонстрировало отсутствие замедления прогрессирования болезни у пациентов с БАС, однако другие исследования показали значительные улучшения при ИФР-1-заместительной терапии у пациентов с БАС[30], поэтому ИФР-1 имеет потенциал для лечения БАС[31]. Однако в целом исследования показали противоречивые результаты[32].
Фармакологическое использование
Пациенты с тяжелым первичным дефицитом ИФР-1 могут лечиться либо ИФР-1, либо ИФР-1 вместе с IGFBP3 (ИФР-связывающий белок типа 3)[33]. Мекасермин (выпускается под брендом Инкрелекс) — синтетический аналог ИФР-1, утверждённый для лечения нарушений роста[33]. ИФР-1 производится в промышленных масштабах с использованием дрожжей или E. coli.
Ссылки на источники
- https://www.ncbi.nlm.nih.gov/gene/3479
- Ageing in Drosophila: the role of the insulin/Igf and TOR signalling network, Partridge L, Alic N, Bjedov I, Piper MD, 2011
- Endocrine regulation of ageing, Russell SJ, Kahn CR, 2007
- Drosophila melanogaster in the Study of Human Neurodegeneration, Frank Hirth, 2010
- Reduced IGF-1 signaling delays age-associated proteotoxicity in mice, Cohen et al, 2009
- The insulin/IGF-1 signaling in mammals and its relevance to human longevity, Rincon M et al, 2005
- Association of common genetic variation in the insulin/IGF1 signaling pathway with human longevity, Pawlikowska L, 2009
- A Conserved Regulatory System for Aging, Cynthia Kenyon, 2001
- Genetic pathways that regulate ageing in model organisms Leonard Guarente & Cynthia Kenyon.
- Role of the GH/IGF-1 axis in lifespan and healthspan: lessons from animal models, Berryman DE, Christiansen JS, Johannsson G, Thorner MO, Kopchick JJ., 2008
- Dwarf mice and the ageing process, Brown-Borg HM, Borg KE, Meliska CJ, Bartke A. 1996
- В. Н. Анисимов «Молекулярные и физиологические механизмы старения» — Спб: Наука 2003 — ISBN 5020261998
Примечания
Литература
- Butler A.A., Yakar S., LeRoith D. Insulin-like growth factor-I: compartmentalization within the somatotropic axis? (англ.) // Physiology (journal) : journal. — 2002. — Vol. 17. — P. 82—5. — PMID 11909998.
- Maccario M., Tassone F., Grottoli S., Rossetto R., Gauna C., Ghigo E. Neuroendocrine and metabolic determinants of the adaptation of GH/IGF-I axis to obesity (англ.) // Ann. Endocrinol. (Paris) : journal. — 2002. — Vol. 63, no. 2 Pt 1. — P. 140—144. — PMID 11994678.
- Camacho-Hubner C., Woods K.A., Clark A.J., Savage M.O. Insulin-like growth factor (IGF)-I gene deletion (неопр.) // Reviews in endocrine & metabolic disorders. — 2003. — Т. 3, № 4. — С. 357—361. — doi:10.1023/A:1020957809082. — PMID 12424437.
- Dantzer B., Swanson E.M. Mediation of vertebrate life histories via insulin-like growth factor-1 (англ.) // Biological Reviews : journal. — 2012. — Vol. 87, no. 2. — P. 414—429. — doi:10.1111/j.1469-185X.2011.00204.x. — PMID 21981025.
- Trojan L.A., Kopinski P., Wei M.X., Ly A., Glogowska A., Czarny J., Shevelev A., Przewlocki R., Henin D., Trojan J. IGF-I: from diagnostic to triple-helix gene therapy of solid tumors (англ.) // Acta Biochim. Pol. : journal. — 2004. — Vol. 49, no. 4. — P. 979—990. — PMID 12545204.
- Winn N., Paul A., Musaro A., Rosenthal N. Insulin-like growth factor isoforms in skeletal muscle aging, regeneration, and disease (англ.) // Cold Spring Harb. Symp. Quant. Biol. : journal. — 2003. — Vol. 67. — P. 507—518. — doi:10.1101/sqb.2002.67.507. — PMID 12858577.
- Delafontaine P., Song Y.H., Li Y. Expression, regulation, and function of IGF-1, IGF-1R, and IGF-1 binding proteins in blood vessels (англ.) // Arteriosclerosis, Thrombosis, and Vascular Biology : journal. — 2005. — Vol. 24, no. 3. — P. 435—444. — doi:10.1161/01.ATV.0000105902.89459.09. — PMID 14604834.
- Trejo J.L., Carro E., Garcia-Galloway E., Torres-Aleman I. Role of insulin-like growth factor I signaling in neurodegenerative diseases (англ.) // Journal of Molecular Medicine : journal. — 2004. — Vol. 82, no. 3. — P. 156—162. — doi:10.1007/s00109-003-0499-7. — PMID 14647921.
- Rabinovsky E.D. The multifunctional role of IGF-1 in peripheral nerve regeneration (англ.) // Neurol. Res. : journal. — 2004. — Vol. 26, no. 2. — P. 204—210. — doi:10.1179/016164104225013851. — PMID 15072640.
- Rincon M., Muzumdar R., Atzmon G., Barzilai N. The paradox of the insulin/IGF-1 signaling pathway in longevity (англ.) // Mech. Ageing Dev. : journal. — 2005. — Vol. 125, no. 6. — P. 397—403. — doi:10.1016/j.mad.2004.03.006. — PMID 15272501.
- Conti E., Carrozza C., Capoluongo E., Volpe M., Crea F., Zuppi C., Andreotti F. Insulin-like growth factor-1 as a vascular protective factor (англ.) // Circulation (журнал) : journal. — Lippincott Williams & Wilkins, 2005. — Vol. 110, no. 15. — P. 2260—2265. — doi:10.1161/01.CIR.0000144309.87183.FB. — PMID 15477425.
- Wood A.W., Duan C., Bern H.A. Insulin-like growth factor signaling in fish (англ.) // International Review of Cell and Molecular Biology : journal. — 2005. — Vol. International Review of Cytology. — P. 215—285. — ISBN 9780123646477. — doi:10.1016/S0074-7696(05)43004-1. — PMID 15797461.
- Sandhu M.S. Insulin-like growth factor-I and risk of type 2 diabetes and coronary heart disease: molecular epidemiology (англ.) // Endocrine development : journal. — 2005. — Vol. Endocrine Development. — P. 44—54. — ISBN 3-8055-7926-8. — doi:10.1159/000085755. — PMID 15879687.
- Ye P., D'Ercole A.J. Insulin-like growth factor actions during development of neural stem cells and progenitors in the central nervous system (англ.) // Journal of Neuroscience Research : journal. — 2006. — Vol. 83, no. 1. — P. 1—6. — doi:10.1002/jnr.20688. — PMID 16294334.
- Gomez J.M. The role of insulin-like growth factor I components in the regulation of vitamin D (англ.) // Current pharmaceutical biotechnology : journal. — 2006. — Vol. 7, no. 2. — P. 125—132. — doi:10.2174/138920106776597621. — PMID 16724947.
- Federico G., Street M.E., Maghnie M., Caruso-Nicoletti M., Loche S., Bertelloni S., Cianfarani S. Assessment of serum IGF-I concentrations in the diagnosis of isolated childhood-onset GH deficiency: a proposal of the Italian Society for Pediatric Endocrinology and Diabetes (SIEDP/ISPED) (англ.) // Journal of Endocrinological Investigation : journal. — 2006. — Vol. 29, no. 8. — P. 732—737. — doi:10.1007/bf03344184. — PMID 17033263.
- Zakula Z., Koricanac G., Putnikovic B., Markovic L., Isenovic E.R. Regulation of the inducible nitric oxide synthase and sodium pump in type 1 diabetes (англ.) // Medical Hypotheses : journal. — 2007. — Vol. 69, no. 2. — P. 302—306. — doi:10.1016/j.mehy.2006.11.045. — PMID 17289286.
- Trojan J., Cloix J.F., Ardourel M.Y., Chatel M., Anthony D.D. Insulin-like growth factor type I biology and targeting in malignant gliomas (англ.) // Neuroscience (журнал) : journal. — Elsevier, 2007. — Vol. 145, no. 3. — P. 795—811. — doi:10.1016/j.neuroscience.2007.01.021. — PMID 17320297.
- Venkatasubramanian G., Chittiprol S., Neelakantachar N., Naveen M.N., Thirthall J., Gangadhar B.N., Shetty K.T. Insulin and insulin-like growth factor-1 abnormalities in antipsychotic-naive schizophrenia (англ.) // American Journal of Psychiatry : journal. — 2007. — October (vol. 164, no. 10). — P. 1557—1560. — doi:10.1176/appi.ajp.2007.07020233. — PMID 17898347.