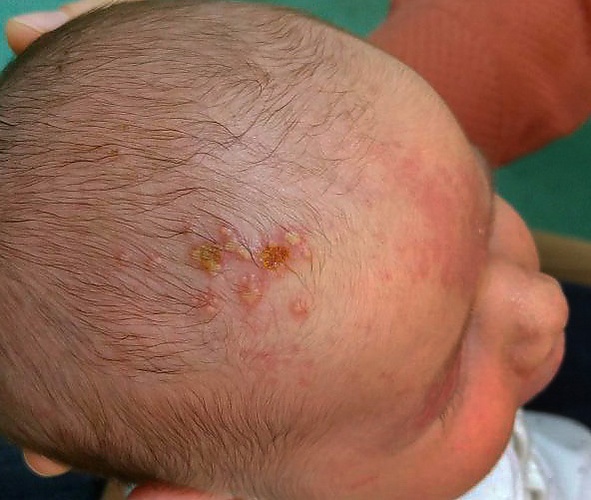
Неонатальный герпес
Неоната́льный ге́рпес (неона́тальная инфе́кция, вы́званная ви́русом просто́го ге́рпеса; врождённая инфе́кция, вы́званная ви́русом просто́го ге́рпеса; врождённая герпети́ческая инфе́кция; врождённый ви́рус просто́го ге́рпеса) — инфекционное заболевание плода и новорождённого, вызванное вирусом простого герпеса (ВПГ). Заболевание возникает в результате передачи возбудителя от матери к ребёнку во время беременности, родов или в послеродовом периоде[1]. Клинические проявления варьируют от ограниченных везикулёзных высыпаний до тяжёлого системного поражения с развитием дыхательной недостаточности, судорог, нарушений терморегуляции и признаков печёночной дисфункции[2]. Диагноз устанавливают на основании клинический картины и результатах лабораторных методов диагностики. Этиотропное лечение состоит в парентеральном введении высоких доз ацикловира[3].
Классификация
Выделяют три клинические формы неонатального герпеса[4]:
- локализованный герпес (кожи, глаз, слизистой оболочки рта);
- изолированное поражение центральной нервной системы (церебральная форма);
- диссеминированный герпес.
Этиология
Возбудителем неонатального герпеса является ВПГ, относящийся к семейству Herpesviridae, роду Simplexvirus. Различают два серотипа вируса: ВПГ-1 и ВПГ-2. Источником инфекции является человек, являющийся единственным природным резервуаром вируса. Передача ВПГ новорождённому происходит преимущественно интранатально (во время родов) при контакте с инфицированными выделениями из родовых путей матери. В большинстве случаев возбудителем выступает ВПГ-2, ассоциированный с генитальными формами герпетической инфекции, однако растёт доля случаев, вызванных ВПГ-1[2][3].
Возможна также антенатальная (трансплацентарная) передача вируса, приводящая к внутриутробному заражению плода, и постнатальное заражение — при тесном контакте с матерью или другими лицами, имеющими активную герпетическую инфекцию[2][3].
Риск инфицирования новорождённого зависит от характера герпетической инфекции у матери[2]:
- первичная генитальная инфекция в третьем триместре беременности сопровождается наибольшим риском вертикальной передачи.
- При рецидивирующей инфекции риск передачи значительно ниже, что связано с наличием у матери защитных антител.
Факторами, повышающими риск заражения, являются[2]:
- тип ВПГ-инфекции;
- серологический статус матери;
- типирование вируса;
- наличие активного ВПГ при родах;
- способ родоразрешения;
- длительный безводный промежуток;
- инвазивные процедуры, например, использование электродов на коже плода.
Патогенез
Заражение новорождённого ВПГ происходит преимущественно интранатально — при контакте кожи и слизистых ребёнка с инфицированными выделениями из родовых путей матери. Вирус проникает через слизистые оболочки или микроповреждения кожи, после чего начинает реплицироваться в эпителиальных клетках[2][5].
Размножение вируса в клетках приводит к их гибели и развитию воспалительной реакции. Вирус способен проникать в чувствительные нервные окончания, мигрировать по аксонам в нервные ганглии и формировать там латентную инфекцию. В дальнейшем возможна реактивация вируса с возобновлением репликации и выделением ВПГ, хотя у новорождённых чаще развивается именно первичное, а не рецидивное поражение[2].
Вирус обладает выраженной нейротропностью и может распространяться гематогенным или нейрогенным путём, вызывая поражение центральной нервной системы, печени, лёгких и других органов. В результате формируются три клинические формы неонатального герпеса — локализованная, энцефалитическая и диссеминированная[2][6].
В редких случаях ВПГ возможно антенатальное инфицирование, что приводит к внутриутробному инфицированию плода. Последствиями такого заражения могут быть врождённые аномалии развития, поражение нервной системы (микроцефалия, гидроцефалия, кальцификаты в мозге), микрофтальмия, задержка внутриутробного роста, мертворождённость и преждевременные роды[5].
Эпидемиология
Распространённость неонатального герпеса составляет от 1 случая на 3000 до 1 случая на 20 000 живорождённых[2]. Частота встречаемости в Англии — 1 случай на 40 000 родов, в США — 1 случай на 2500—10 000 родов[5]. Наиболее часто новорождённый заражается во время родов — в 75—85 % случаев, когда вирус передаётся при контакте с инфицированными половыми путями матери. В 5—8 % случаев инфекция передаётся трансплацентарно (через плаценту во время беременности), а в оставшихся случаях — постнатально, при контакте с родителями или лицами, осуществляющими уход[7].
При первичном эпизоде генитального герпеса во время беременности вероятность инфицирования новорождённого достигает 25—60 %[2], по некоторым данным — до 50 %[5]. Рецидив полового герпеса во время беременности с симптомами болезни приводит к заражению ребёнка всего в 3 % случаев, а без симптомов — в 0,05 % случаев[7].
Наличие у матери антител как к ВПГ-1, так и к ВПГ-2 существенно снижает риск передачи вируса — до 1—3 %, что объясняется трансплацентарной передачей защитных материнских антител, начинающейся примерно с седьмого месяца беременности[8][9].
Диагностика
Врождённая герпетическая инфекция характеризуется широким полиморфизмом и выявляется при рождении в первые 24—48 часов жизни новорождённого. Заболевание может протекать в локализованной, церебральной, диссеминированной формах, а также в виде латентной инфекции, манифестирующей позже. Инкубационный период варьирует от 2 до 30 дней, чаще всего клиническая манифестация наблюдается между первой и второй неделями жизни ребёнка[10].
Внутриутробная передача ВПГ может приводить к выкидышам, мертворождению, повреждению центральной нервной системы плода (вентрикуломегалия, микроцефалия, гидранэнцефалия, агенезия мозолистого тела, внутричерепные кальцификаты), преждевременным родам, внутриутробной задержке плода, внутриутробной гибели плода, формированию кожных рубцов, микрофтальмии, дисплазии сетчатки, атрофии зрительного нерва и хориоретинита[2][5].
Локализованная форма герпетической инфекции наблюдается у 20—40 % новорождённых. Она характеризуется поражением кожи, слизистых оболочек полости рта и глаз. На коже на 10—11 день появляются типичные единичные или сгруппированные везикулы на эритематозном фоне, чаще на лице и конечностях. Везикулы вскрываются, образуя эрозии, покрывающиеся корочками. Возможна пятнистая эритема[7][10]. У 10 % детей отмечается афтозный стоматит с везикулами на слизистой полости рта. У 40 % больных развивается поражение глаз в виде конъюнктивита, кератита или хориоретинита. Осложнения глазной формы — язва роговицы, атрофия зрительного нерва и слепота. Заболевание может сопровождаться повышением температуры тела, снижением аппетита, трудностями при сосании, нарушениями адаптации. Без терапии у 50—70 % новорождённых инфекция прогрессирует с вовлечением центральной нервной системы или генерализацией процесса. Часто отмечается рецидивирующее течение в течение первого года жизни и позднее[5].
Церебральная форма неонатального герпеса наблюдается у 30—35 % больных и развивается при интранатальном заражении. Манифестация заболевания происходит на 2—4-й неделе жизни[7]. Для церебральной формы характерны типичные признаки герпетического энцефалита. Заболевание начинается с повышения температуры тела, нарушений поведения и сознания: отмечаются угнетение вплоть до ступора или комы либо, напротив, гипервозбудимость, беспокойство, высокочастотный крик. У большинства детей (60—80 %) развиваются судороги, преимущественно генерализованные[5]. Нередко наблюдаются трудности при кормлении, раздражительность, набухание большого родничка, эпизоды апноэ. В клинической картине нередко присутствуют кожные проявления герпетической инфекции. У 60—70 % новорождённых с поражением центральной нервной системы на каком-либо этапе заболевания отмечаются везикулярные высыпания на коже и слизистых либо кератоконъюнктивит, что помогает установить герпетическую природу поражения[2][11].
Без своевременной противовирусной терапии заболевание быстро прогрессирует и нередко заканчивается летально. Даже при проведении специфического лечения выживаемость достигает около 80 %, однако у большинства детей остаются стойкие неврологические последствия. К ним относятся эпилепсия, парезы, задержка психического и интеллектуального развития, формирование микроцефалии, гидроцефалии, участков энцефаломаляции и внутричерепных кальцификатов[2][7].
Диссеминированный неонатальный герпес развивается преимущественно при интранатальном заражении и является одной из самых тяжёлых форм заболевания. Он составляет 25—50 % всех случаев герпеса новорождённых. Симптомы появляются, как правило, на 4—10-й день жизни и достигают максимума к 9—11-му дню. Заболевание характеризуется поражением многих органов — головного мозга (энцефалит), печени (гепатит), лёгких (интерстициальная пневмония), сердца (миокардит), селезёнки, надпочечников. Клиническая картина напоминает бактериальный сепсис и сопровождается развитием ДВС-синдрома. Отмечаются лихорадка или, наоборот, гипотермия, повышенная возбудимость, крик, генерализованные судороги, сменяющиеся угнетением сознания, вялостью и гипотонией. Нередко наблюдаются дыхательная недостаточность, апноэ, гепатомегалия, желтуха, кровоточивость, признаки печёночной недостаточности, гипогликемия, тромбоцитопения, коагулопатия и шок. Также наблюдаются герпетические везикулярные высыпания на коже и слизистых оболочках, которые могут отсутствовать у 20—30 % больных[5][7].
Другие симптомы, которые могут возникать как изолированно, так и в комбинации, включают нестабильность температуры, вялость, гипотонию, дыхательную недостаточность, апноэ и судороги[3].
- Выявление ДНК ВПГ методом полимеразной цепной реакции в мазках со слизистых полости рта, носоглотки, конъюнктивы и прямой кишки, при наличии поражений центральной нервной системы — в ликворе, при диссеминированных формах заболевания — дополнительно в крови, а при наличии элементов сыпи — в содержимом везикул[5].
- Вирусологическое исследование — культивирование ВПГ из содержимого везикул, слизистых оболочек или ликвора. Цитопатогенные изменения в культуре клеток наблюдаются через 1—3 дня после заражения. Положительные результаты посева, полученные более чем через 12—24 часа после рождения, свидетельствуют о репликации вируса у новорождённого[2].
- Исследование спинномозговой жидкости (при церебральной форме неонатального герпеса) — повышенная концентрация белка, плеоцитоз[2][5]
- Проба Тцанка поражённых участков — могут наблюдаться характерные многоядерные гигантские клетки и внутриядерные включения[3]
- Иммуноферментный анализ — определение IgM и IgG к ВПГ в сыворотке крови новорождённого. IgM свидетельствуют об активной инфекции, однако могут отсутствовать при врождённой форме. Диагностическим критерием служит нарастание титра специфических IgG или отсутствие их снижения в динамике заболевания[5]. Для дополнительного подтверждения может использоваться сравнительное определение антител (IgG и IgM) в сыворотке крови и ликворе. Наличие интратекальных антител к ВПГ или повышенное соотношение титров между ликвором и сывороткой является достоверным признаком вовлечения центральной нервной системы. Следует помнить, что в норме антитела к вирусу могут присутствовать в крови, но в ликворе они отсутствуют, и их появление свидетельствует о герпетическом энцефалите[2][10].
- Электроэнцефалография — проводится у младенцев, у которых наблюдаются судороги. Могут выявляться периодические эпилептиформные разряды[2].
- Компьютерная томография или магнитно-резонансная томография головного мозга — выявляются очаги пониженной плотности (некрозы) преимущественно в лобных и височных долях мозга, реже в теменных, затылочных долях головного мозга, стволе и мозжечке[5].
- Офтальмологическое обследование — проводится всем новорождённым с герпетической инфекцией для исключения кератоконъюнктивита, хориоретинита и других поражений органов зрения[2].
Дифференциальная диагностика
Включает:
- неонатальный сепсис;
- токсическая эритема новорождённых;
- транзиторный пустулёзный меланоз новорождённых;
- акне новорождённых;
- потница;
- вирусный конъюнктивит, вызванный аденовирусом или энтеровирусом;
- бактериальный конъюнктивит, вызванный Chlamydia trachomatis, Neisseria gonorrhoeae;
- бактериальный менингит;
- вирусный менингоэнцефалит, вызванный энтеровирусом или парэховирусом;
- врождённые нарушения обмена веществ;
- аденовирусная инфекция;
- энтеровирусная инфекция;
- парвовирусная инфекция;
- вирусный гепатит;
- лекарственный гепатит;
- цитомегаловирусная инфекция;
- токсоплазмоз;
- сифилис;
- краснуха[2];
- опоясывающий герпес;
- ветряная оспа;
- герпетическая ангина;
- грибковый стоматит[12].
Осложнения
Включают:
- ухудшение зрения,
- слепота,
- образование рубцов,
- полиорганная недостаточность,
- микрофтальмия,
- дисплазия сетчатки,
- энцефалит[2],
- язва роговицы,
- атрофия зрительного нерва,
- вентрикуломегалия,
- микроцефалия
- гидранэнцефалия,
- агенезия мозолистого тела,
- внутричерепные кальцификаты[5],
- эпилепсия,
- парезы,
- задержка психического и интеллектуального развития,
- летальный исход[7],
- инфекционно-токсический шок,
- ДВС-синдром,
- массивный некроз печени[12].
Лечение
Стандартом терапии врождённой инфекции, вызванной ВПГ, является парентеральное введение ацикловира. Лечение назначают всем новорождённым с подтверждённой или предполагаемой ВПГ-инфекцией, независимо от клинических проявлений. Продолжительность терапии зависит от формы заболевания: при поражении кожи, слизистых оболочек или глаз лечение проводят в течение 14 дней, при поражении центральной нервной системы или диссеминированной форме — не менее 21 дня[2][5].
Ближе к завершению курса терапии поражения центральной нервной системы рекомендуется повторное исследование спинномозговой жидкости методом полимеразной цепной реакции для подтверждения отсутствия вирусной ДНК[2].
После завершения курса внутривенной терапии, младенцам с любой формой заболевания, вызванного ВПГ, назначают пероральный ацикловир на 6 месяцев; этот долгосрочный режим улучшает неврологическое развитие в возрасте 1 года, однакр может вызывать нейтропению[3].
При герпетическом поражении глаз проводится комбинированное лечение с применением местных офтальмологических противовирусных препаратов (трифлуридин, йододезоксиуридин или ганцикловир), в сочетании с системным ацикловиром. Терапия проводится под контролем офтальмолога[2][3].
В тяжёлых и генерализованных формах заболевания в состав комплексной терапии могут включаться иммуноглобулины для внутривенного введения. При наличии неврологических симптомов в программу лечения рекомендуется включить последовательно следующие препараты: полипептиды коры головного мозга скота, гидролизат головного мозга крупного рогатого скота, пиритинол[13].
Поддерживающая терапия включает коррекцию водно-электролитного баланса, нутритивную поддержку, респираторную помощь при необходимости, а также контроль судорог и коррекцию нарушений свёртываемости крови[3].
Прогноз
Прогноз при врождённой инфекции, вызванной ВПГ, зависит от формы заболевания, времени инфицирования плода, степени поражения органов и своевременности начала терапии. У новорождённых с локализованной формой заболевания прогноз относительно благоприятный, особенно при раннем начале противовирусного лечения.. Однако без терапии заболевание нередко прогрессирует, переходя в диссеминированную форму или поражение центральной нервной системы. При диссеминированной форме и герпетическом энцефалите прогноз существенно хуже. Без лечения смертность при диссеминированной инфекции достигает до 85 %, а при поражении центральной нервной системы — около 50 %. Даже при адекватном лечении неврологические последствия сохраняются примерно у 13 % детей с диссеминированной формой и у 40—70 % детей с поражением центральной нервной системы[3].
Раннее начало противовирусного лечения и последующая супрессивная терапия улучшают исход заболевания и снижают риск осложнений[2].
Диспансерное наблюдение
Индивидуальное наблюдение у врача-педиатра, врача-офтальмолога и врача-невролога.
Профилактика
Профилактика неонатальной герпетической инфекции направлена на предотвращение заражения плода и новорождённого вирусом простого герпеса (ВПГ) и включает меры до, во время и после родов. Основное значение имеет снижение частоты и активности генитального герпеса у беременных. Женщинам с анамнезом ВПГ-инфекции рекомендуется проведение противовирусной терапии до наступления беременности и супрессивной терапии ацикловиром или валацикловиром, начиная с 36-й недели гестации, что снижает частоту рецидивов и риск инфицирования новорождённого[2][11].
При наличии активных герпетических высыпаний или продромальных симптомов в родах показано проведение кесарева сечения, особенно при первичном инфицировании в третьем триместре. Вагинальные роды допустимы только при отсутствии поражений в области гениталий[2][11].
После родов при выявлении у матери герпетической инфекции новорождённый подлежит обследованию на наличие ВПГ и при необходимости — профилактическому назначению ацикловира. Больные новорождённые должны быть изолированы для предотвращения внутрибольничного распространения инфекции[11].