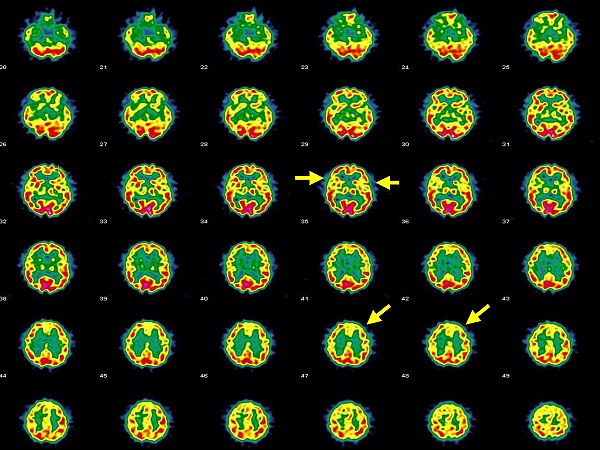
Энцефалопатия Хашимото
Энцефалопати́я Хашимо́то (также известна как стероид-реакти́вная энцефалопати́я, ассоции́рованная с аутоимму́нным тиреоиди́том) — редкое аутоиммунное заболевание, проявляющееся энцефалопатией, очаговой неврологической симптоматикой и повышенным титром аутоантител к щитовидной железе (чаще к тиреопероксидазе и тиреоглобулину). Клиническая картина может носить рецидивирующий и ремиттирующий характер с множеством симптомов, включая миоклонус, судорожные приступы, острое нарушение мозговного кровообращения, снижение когнитивных функций и нейропсихиатрические симптомы. При этом клинически и биохимически функция щитовидной железы часто остаётся в норме. Прогноз ЭХ, как правило, благоприятный: может наблюдаться улучшение даже в случае, если лечение было начато спустя месяцы или годы после появления симптомов[1][2].
Что важно знать
История
Первое описание ЭХ было представлено в 1966 году, когда Лорд Брейн и его коллеги представили клиническое наблюдение 49-летнего мужчины, у которого наблюдались эпизоды инсультоподобных симптомов, затрагивающих несколько сосудистых зон, галлюцинации, изменения уровня сознания и когнитивные нарушения[3].
Классификация
Выделяют два клинических подтипа энцефалопатии Хашимото[3]:
- Эпизодический (васкулитоподобный) подтип: характеризуется рецидивирующими инсультоподобными эпизодами.
- Прогрессирующий подтип: проявляется постепенно нарастающими когнитивными нарушениями и изменениями личности.
Этиология
Этиология ЭХ остаётся до конца невыясненной и служит предметом научного изучения. У пациентов с ЭХ определяются циркулирующие в крови аутоантитела, направленные против тканей собственной щитовидной железы, чаще всего это антитела к тиреопероксидазе или к тиреоглобулину[4].
Патогенез
Патогенез ЭХ до конца не определён. Имеются различные теории, описывающие процессы, лежащие в основе заболевания[3]:
- роль антитиреоидных антител: в отличие от других аутоиммунных неврологических заболеваний, где антитела имеют чёткий патогенный механизм (например, блокада рецепторов), роль антител к тиреопероксидазе и тиреоглобулину в патогенезе ЭХ неизвестна. Они могут быть либо прямым патогенным фактором, либо лишь эпифеноменом, маркером аутоиммунного процесса;
- теория перекрёстной реактивности (общие антигены): эмпирические данные не подтверждают теорию о том, что патогенность антитиреоидных антител обусловлена перекрёстной реакцией с антигенами мозга. Структурного сходства между тиреоидными белками (тиреопероксидаза, тиреоглобулин) и белками центральной нервной системы не обнаружено. Однако есть данные о специфическом связывании антител с астроцитами мозжечка у пациентов с энцефалопатией, что может указывать на опосредованное антителами нарушение функции нейроглии;
- теория аутоиммунного васкулита (альтернативная): данные очаговой гипоперфузии при нейровизуализации и обнаружение антител к альфа-энолазе (ассоциированных с другими васкулитами) косвенно поддерживают эту теорию. Однако периваскулярная лимфоцитарная инфильтрация является неспецифическим признаком и наблюдается при многих нейровоспалительных заболеваниях, поэтому её интерпретация как «истинного васкулита» спорна;
- теория токсического действия тиреотропин-рилизинг-гормона: существует гипотеза, что причиной неврологических симптомов может быть повышенная концентрация церебрального тиреотропин-рилизинг-гормона. В пользу этого свидетельствует единичный случай провокации симптомов с помощью инфузии этого гормона.
Патоморфологические находки in vivo разнообразны и немногочисленны; наиболее часто выявляется слабая лимфоцитарная инфильтрация мелких капилляров. Наличие периваскулярных лимфоцитарных инфильтратов, аналогичных тем, что наблюдаются при экспериментальных моделях, ставит вопрос о возможном внутримозговом васкулите. Однако для классического васкулита характерны повреждение сосудистой стенки и трансмуральная инфильтрация, которые при ЭХ обычно отсутствуют[3].
Эпидемиология
Поскольку ЭХ является редким заболеванием, оценить её заболеваемость и распространённость может быть сложно. Согласно исследования, распространённость, определяемая как выявление антитиреоидных антител у пациентов с необъяснимой энцефалопатией, была оценена в 2,1 случая на 100 000 участников. Случаи заболевания регистрируются во всем мире среди взрослого, пожилого и детского населения. Средний возраст дебюта болезни составляет от 45 до 55 лет, при этом зарегистрированный возрастной диапазон пациентов — от 9 до 86 лет. Наблюдается явное преобладание ЭХ у женщин с соотношением женщин к мужчинам примерно 5:1[3].
Диагностика
ЭХ характеризуется широким спектром неврологических и психиатрических симптомов. К основным клиническим проявлениям относятся поведенческие нарушения, дезориентация, снижение когнитивных функций, инсультоподобные эпизоды, амнестический синдром, атаксия, судорожные приступы, миоклонус, а также различные психиатрические симптомы, такие как депрессия, мания, психозы и галлюцинации. В зрелом возрасте наиболее частыми проявлениями являются эпилептические приступы (фокальные и фокально-генерализованные) и миоклонус, которые наблюдаются у большинства пациентов. У детей преобладают генерализованные тонико-клонические приступы и сложные парциальные припадки[3].
Выделяют два основных клинических подтипа энцефалопатии Хашимото. Первый, эпизодический или васкулитоподобный подтип, характеризуется рецидивирующими инсультоподобными симптомами. Второй подтип проявляется более прогрессирующим течением с выраженным воспалительным началом, быстрым развитием когнитивного дефицита и потерей памяти. Также описаны такие неврологические симптомы, как опсоклонус (хаотичные саккадические движения глаз), который может предшествовать развитию энцефалопатии и сочетаться с атаксией[3].
Иммунохемилюминесцентный анализ крови: у большинства пациентов с ЭХ выявляется повышенный титр антител к щитовидной железе, а именно антител к тиреопероксидазе или антител к тиреоглобулину, что является обязательным критерием для постановки диагноза[1].
Иммуноферментный анализ: могут определяться антитела к тиреотропному гормону в крови и ликворе[1].
Клинический анализ ликвора: частым отклонением является повышение концентрации белка, которое наблюдается примерно у 75 % больных. Умеренный лимфоцитарный плеоцитоз присутствует в 10-25 % случаев[1].
Патологические изменения при магнитно-резонансной томографии включают ишемические поражения, демиелинизацию, отёк, атрофию, а также патологические сигналы в гиппокампе или височной доле[1].
Неспецифические изменения на электроэнцефалограмме наблюдаются более чем у 90 % пациентов и обычно проявляются в виде замедления фоновой ритмики. Также описаны такие паттерны, как фокальные спайки или острые волны, трифазные волны и фронтальная интермиттирующая ритмическая дельта-активность[1].
Дифференциальная диагностика
Дифференциальная диагностика ЭХ проводится с широким спектром заболеваний, имеющих сходную клиническую картину[2][3]:
- аутоиммунные и системные заболевания: системная красная волчанка может проявляться схожими нейропсихиатрическими симптомами, включая судороги и психозы. Отличием служит профиль аутоантител (анти-ДНК, антифосфолипидные, антинейрональные), а также возможное наличие признаков тромбоза или инфаркта при нейровизуализации. Первичный васкулит центральной нервной системы также может проявляться энцефалопатией и очаговой симптоматикой;
- Аутоиммунные энцефалиты: паранеопластический лимбический энцефалит и непаранеопластические энцефалиты (например, с антителами к NMDA-рецептору или LGI1) характеризуются выраженными когнитивными и поведенческими расстройствами. Ключевым отличием от ЭХ является наличие специфических антинейрональных антител (например, анти-Hu, анти-Ma2, анти-NMDA) и, как правило, отсутствие высоких титров антитиреоидных антител. При лимбическом энцефалите при магнитно-резонансной томографии часто выявляет характерные изменения в медиальных отделах височных долей;
- быстропрогрессирующие деменции и нейродегенеративные заболевания: болезнь Крейтцфельдта — Якоба отличается крайне быстрым прогрессированием деменции с выраженным миоклонусом и наличием специфических изменений на электроэнцефалограмме (периодические комплексы), а также отсутствием ответа на терапию глюкокортикостероидами. Деменция с тельцами Леви сопровождается паркинсонизмом, флуктуирующим уровнем сознания и зрительными галлюцинациями, но, как правило, протекает без судорожных припадков и инсультоподобных эпизодов, характерных для ЭХ;
- эндокринные расстройства: для аутоиммунного гипофизита характерны специфические эндокринные нарушения (недостаточность АКТГ, несахарный диабет) и изменения на магнитно-резонансной томографии (объёмное образование в области турецкого седла).
Осложнения
Основным осложнением ЭХ у детей, согласно исследованиям, является рецидивирующий эпилептический статус, причём эти симптомы связаны с вовлечением лобных долей головного мозга. У взрослых пациентов с данным заболеванием также отмечается связь с множественной гиперчувствительностью к противоэпилептическим препаратам и с височной эпилепсией[3].
Лечение
Основой терапии является применение глюкокортикостероидов, таких как преднизолон или высокие дозы метилпреднизолона внутривенно. Примерно у половины пациентов наблюдается полный ответ на такое лечение, а у значительной части достигается стойкая ремиссия после первого курса. Длительность терапии и скорость снижения дозы подбираются индивидуально в зависимости от клинического ответа. Раннее начало лечения способствует регрессу неврологической симптоматики. Однако у части пациентов возможны рецидивы и резистентность к терапии. В случаях резистентности к глюкокортикостероидам или частых рецидивах рекомендовано добавление иммуносупрессивных препаратов, таких как метотрексат, азатиоприн или циклофосфамид. Также в качестве дополнительной терапии показал эффективность ритуксимаб — моноклональное антитело против CD20. Перспективным направлением считается применение препаратов, предотвращающих воспалительное повреждение гематоэнцефалического барьера, например, натализумаба. Пациентам с непереносимостью глюкокортикостероидов или иммуносупрессантов может быть назначен внутривенный иммуноглобулин или плазмаферез. Оба метода демонстрируют значительное клиническое улучшение как у взрослых, так и у детей. Плазмаферез эффективно снижает титр антител к тиреопероксидазе, однако это снижение не всегда коррелирует с улучшением неврологического статуса[3].
Для контроля эпилептических приступов у пациентов с ЭХ применяются противоэпилептические препараты. Особый интерес представляет леветирацетам, который, помимо антиконвульсантного действия, обладает доказанными противовоспалительными свойствами. Он может быть эффективным вариантом лечения для пациентов с непереносимостью глюкокортикостероидов, в том числе при сопутствующем сахарном диабете[3].
Прогноз
Прогноз при ЭХ, как правило, благоприятный. Улучшение состояния возможно даже в случаях, когда лечение начинается спустя месяцы или годы после появления первых симптомов. Примерно у 25 % пациентов с длительным нелеченным заболеванием наблюдаются остаточные когнитивные нарушения. После отмены глюкокортикостероидов большинство пациентов остаются в состоянии ремиссии, однако у части из них возникают рецидивы, требующие повторных курсов терапии, а иногда и назначения иммуносупрессивной терапии. Также в литературе описаны случаи спонтанного выздоровления[1].
Диспансерное наблюдение
Профилактика
Не разработана.
Примечания
Литература
- Croce L., Dal Molin M., Teliti M., Rotondi M. Hashimoto’s encephalopathy: an endocrinological point of view (англ.) // Frontiers in Endocrinology. — 2024. — Vol. 15. — P. 1367817. — doi:10.3389/fendo.2024.1367817.
- Ramesh A., Swaminathan A. Hashimoto’s Encephalopathy: A Review (англ.) // Journal of Experimental Neurology. — 2024. — Vol. 5, no. 2. — P. 95—106. — doi:10.33696/Neurol.5.093.
- Кутлубаев М. А., Гехтман О. В., Закирова Э. Н. Энцефалопатия Хашимото (краткий обзор литературы и клиническое наблюдение) // Неврология, нейропсихиатрия, психосоматика. — 2019. — № 1. — С. 79—83.