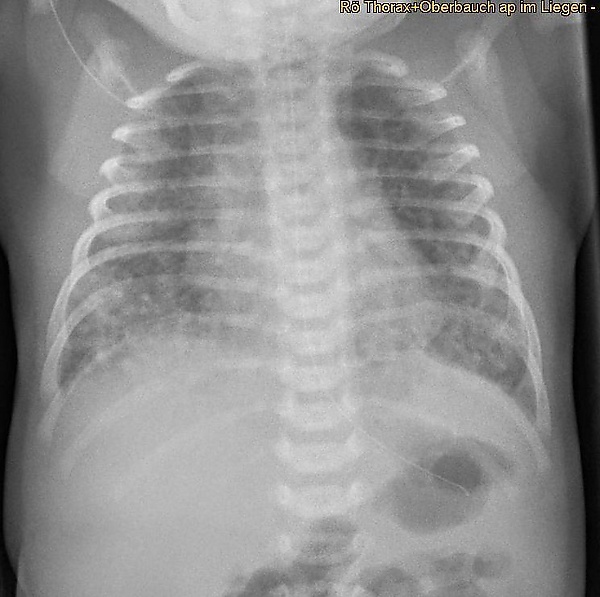
Синдром аспирации мекония
Синдро́м аспира́ции меко́ния (САМ) — респираторное расстройство у новорожденных, возникающее как следствие аспирации мекониальных околоплодных вод и ведущее к развитию дыхательной недостаточности[2].
Общие сведения
История
Ключевую роль в описании САМ как самостоятельного патологического процесса сыграли работы Г. С. Грегори (Gregory G.A.) и его коллег (1974). Они детально описали клиническую картину, рентгенологические данные и патофизиологию синдрома[3].
Классификация
Классификация мекониального окрашивания околоплодных вод по времени появления и характеристикам[4].
| Классификация мекониального окрашивания околоплодных вод | Баллы | ||
|---|---|---|---|
| Тип классификации | Категория | Характеристика | |
| По времени появления | Раннее окрашивание | Излитие околоплодных вод происходит с примесью мекония | |
| Позднее окрашивание | Меконий появляется в водах в процессе родов | ||
| По цвету (баллы) | 1 балл | Зеленоватая окраска | Оценивается отдельно |
| 2 балла | Зелёная окраска | ||
| 3 балла | Желто-коричневая окраска («старый» меконий) | ||
| По консистенции | А | Жидкие | Оценивается отдельно |
| Б | Умеренно густые | ||
| В | Густые | ||
Эпидемиология
Мекониевое окрашивание околоплодных вод (МОВ), которое является предпосылкой для развития САМ, наблюдается примерно в 10—13 % случаев всех родов. Из числа новорожденных, появившихся на свет в мекониевых водах, респираторный дистресс (которым может являться и САМ) развивается примерно у 4 %[5][6].
Риск развития респираторных нарушений у младенцев, рождённых в мекониевых водах, чрезвычайно высок и в 100 раз превышает вероятность их появления у детей, рождённых в прозрачных околоплодных водах. Эта закономерность сохраняется даже при отсутствии явных признаков дистресса плода во время родов или необходимости в реанимационных мероприятиях после рождения[5].
Выявлены четкие группы риска по развитию синдрома аспирации мекония. К ним относятся[6]:
- новорожденные с задержкой внутриутробного развития (ЗВУР);
- определённые этнические группы: чернокожие американцы, африканцы и жители островов Тихого океана.
К факторам, ассоциированным с отхождением мекония и, как следствие, с риском аспирации, относятся состояния, вызывающие дистресс плода: плацентарная недостаточность, сдавливание пуповины, преэклампсия, маловодие, ЗВУР и злоупотребление матери табаком и кокаином[6].
Отмечается положительная тенденция: в развитых странах частота случаев мекониальной аспирации со временем снизилась. Это связывают с совершенствованием акушерской помощи, в частности, с практикой недопущения перенашивания беременности дольше 41 недели[5][6].
Этиология
Первичной причиной развития САМ является гипоксический стресс у плода. В норме выход мекония из кишечника предотвращается низким уровнем мотилина (отсутствие перистальтики) и тоническим сокращением анального сфинктера[5].
Под воздействием гипоксии происходят два ключевых события, приводящих к синдрому:
- выделение мекония в околоплодные воды: Гипоксия вызывает рефлекторное расслабление анального сфинктера и стимулирует перистальтику желудочно-кишечного тракта, что приводит к выходу мекония в амниотическую жидкость;
- аспирация мекониальных вод: гипоксия стимулирует у плода дыхательные движения, в результате которых заглоченные мекониальные околоплодные воды попадают в дыхательные пути.
Таким образом, этиология САМ является двухэтапной: сначала гипоксия приводит к загрязнению околоплодных вод меконием, а затем — к их аспирации в лёгкие плода[5].
Патогенез
Патогенез САМ начинается с внутриутробного стресса плода (гипоксия, ацидоз, инфекция), который вызывает вагусную реакцию. Это приводит к усилению перистальтики кишечника и расслаблению анального сфинктера, в результате чего меконий попадает в околоплодные воды (МОВ)[2].
Аспирация мекониальных вод происходит либо внутриутробно во время эпизодов гипоксии, стимулирующих дыхательные движения, либо во время первых вдохов после рождения. Попадание мекония в лёгкие запускает несколько взаимосвязанных патофизиологических механизмов[2]:
- механическая обструкция дыхательных путей:
- мекониевые пробки закупоривают дыхательные пути;
- частичная обструкция создает клапанный механизм: воздух поступает на вдохе, но не выходит на выдохе, что приводит к гиперинфляции и образованию воздушных ловушек;
- полная обструкция вызывает ателектаз (спадение) участков лёгкого;
- это приводит к несоответствию вентиляции и перфузии (V/Q), тяжелой гипоксемии и может осложниться утечкой воздуха (пневмоторакс, пневмомедиастинум);
- химическое воспаление и активация воспалительного каскада:
- меконий распознается иммунной системой как чужеродный агент, что запускает реакцию врожденного иммунитета (возможно, через толл-подобные рецепторы и систему комплемента);
- меконий является хемоаттрактантом для нейтрофилов и источником провоспалительных цитокинов (ИЛ-1, ИЛ-6, ИЛ-8, ФНО-α), что приводит к массивной клеточной инфильтрации и развитию химического пневмонита;
- воспаление вызывает повреждение легочной ткани, апоптоз клеток и повышает риск бактериальной суперинфекции;
- дисфункция и инактивация сурфактанта:
- компоненты мекония (особенно свободные жирные кислоты, желчные кислоты) непосредственно инактивируют сурфактант, покрывающий альвеолы;
- это нарушает его функцию по снижению поверхностного натяжения, что приводит к коллапсу альвеол (ателектазу);
- развитие персистирующей лёгочной гипертензии (ПЛГН):
- вышеперечисленные механизмы (гипоксия, ацидоз, перерастяжение лёгких) вызывают вазоконстрикцию (сужение) лёгочных сосудов;
- хроническая внутриутробная гипоксия также может приводить к гипертрофии гладкой мускулатуры лёгочных артерий;
- это приводит к резкому повышению сопротивления в малом круге кровообращения, шунтированию крови справа налево (минуя лёгкие) и тяжелой, рефрактерной гипоксемии.
Диагностика
Диагностика синдрома мекониальной аспирации начинается с оценки клинической картины, основанной на анамнезе и физикальном осмотре. Ключевым критерием является развитие респираторного дистресса у новорождённого, который появился на свет в условиях мекониально-окрашенной околоплодной жидкости. Характерным признаком является стойкая дыхательная недостаточность, проявляющаяся в необходимости назначения дополнительного кислорода для поддержания сатурации выше 92 %. Важным диагностическим ориентиром служат временные рамки: потребность в респираторной поддержке возникает в первые 2 часа жизни и сохраняется не менее 12 часов. При этом принципиально важно исключить другие причины дистресса, такие как врождённые аномалии развития дыхательных путей, лёгких или сердца, которые могли бы объяснить симптоматику[5].
Основным методом лабораторной диагностики, позволяющим объективно оценить степень дыхательной недостаточности, является анализ газов артериальной крови. У младенцев с САМ данный анализ типично выявляет сочетание гипоксемии (снижения парциального давления кислорода — PaO₂) и гиперкапнии (повышения парциального давления углекислого газа — PaCO₂). Эти изменения отражают нарушение газообмена в лёгких вследствие обструкции дыхательных путей, воспалительной реакции и спадения альвеол[5].
Инструментальная диагностика играет решающую роль в подтверждении диагноза, оценке тяжести поражения лёгких и выявлении осложнений. На начальном этапе обязательным методом является рентгенография органов грудной клетки. На рентгенограммах вначале могут визуализироваться линейные уплотнения, которые по мере развития патологического процесса прогрессируют до классической картины: гиперинфильтрации (вздутия) лёгких в сочетании с диффузными очаговыми уплотнениями. У 10—30 % младенцев с САМ рентгенологически диагностируется такое осложнение, как утечка воздуха (пневмоторакс, пневмомедиастинум). В качестве высокоинформативного и неинвазивного метода динамического наблюдения в условиях отделения интенсивной терапии все шире применяется ультразвуковое исследование лёгких. Для САМ характерны следующие ультразвуковые признаки: множественные линии В, свидетельствующие об интерстициальном отёке, участки уплотнения легочной ткани, ателектазы и воздушные бронхограммы. Поскольку жизнеугрожающим осложнением САМ является персистирующая легочная гипертензия (ПЛГ), золотым стандартом для её подтверждения служит эхокардиография. Ключевыми эхокардиографическими признаками ПЛГ являются дилатация правого желудочка, трикуспидальная регургитация, которая наблюдается у 60-85 % пациентов, а также визуализация право-левого шунтирования крови через открытый артериальный проток или овальное окно[5].
Дифференциальная диагностика
Дифференциальная диагностика САМ включает в себя выявление других причин дыхательной недостаточности. К ним могут относиться транзиторное тахипноэ новорождённых (возникает у младенцев, рождённых на сроке от 34 до 37 недель беременности, и обычно проходит в течение 24 часов), сепсис, пневмония и врождённый порок сердца[5].
Лечение
Лечение синдрома аспирации мекония представляет собой комплексный многоэтапный процесс, направленный на поддержание адекватного дыхания, стабилизацию состояния новорожденного и профилактику осложнений[7]:
- Первичные реанимационные мероприятия в родильном зале начинаются с немедленной санации верхних дыхательных путей. При рождении ребёнка с мекониальной аспирацией необходимо сразу же отсосать содержимое из ротоглотки и носовых ходов с помощью катетера. Если у новорожденного отмечается угнетение центральной нервной системы, нарушение дыхания или мышечная гипотония, показана интубация трахеи с последующей санацией дыхательных путей через эндотрахеальную трубку.
- Респираторная поддержка является основным компонентом лечения. При умеренной дыхательной недостаточности применяют кислородотерапию через носовые канюли или лицевую маску. При более тяжелых формах показана респираторная поддержка с созданием постоянного положительного давления в дыхательных путях (CPAP). В случаях выраженной дыхательной недостаточности, при нарастающей гипоксемии и гиперкапнии переходят к искусственной вентиляции легких. Современные подходы рекомендуют использование щадящих режимов вентиляции с ограничением пикового давления и дыхательного объёма для минимизации баротравмы. При рефрактерной дыхательной недостаточности может применяться высокочастотная осцилляторная вентиляция.
- Медикаментозная терапия включает назначение антибактериальных препаратов широкого спектра действия, поскольку меконий создает благоприятную среду для развития бактериальной инфекции, а клиническая и рентгенологическая картина часто неотличима от пневмонии. При выраженном болевом синдроме и для синхронизации с аппаратом ИВЛ применяют седативные и анальгезирующие средства. Для стабилизации гемодинамики могут использоваться инотропные препараты. При развитии персистирующей легочной гипертензии применяют ингаляции оксида азота, который обладает селективным сосудорасширяющим действием на легочные сосуды.
- Адъювантная терапия включает применение сурфактанта, который может частично нивелировать инактивирующее действие мекония на эндогенный сурфактант. При тяжелых формах САМ с развитием рефрактерной дыхательной недостаточности рассматривается возможность проведения экстракорпоральной мембранной оксигенации (ЭКМО). Важное значение имеет поддерживающая терапия, включающая коррекцию метаболических нарушений, поддержание адекватного теплового режима и нутритивной поддержки.
Длительность и интенсивность терапии определяются тяжестью состояния ребёнка и степенью дыхательной недостаточности. Прогноз зависит от своевременности начатого лечения, наличия сопутствующих осложнений и адекватности проводимой респираторной поддержки[7].
Прогноз
Внедрение в клиническую практику таких методов лечения, как терапия сурфактантом и экстракорпоральная мембранная оксигенация (ЭКМО), позволило существенно снизить показатели смертности. Так, ретроспективные исследования демонстрируют снижение уровня летальности с 4,2 %, отмечавшегося в период с 1973 по 1987 год, до 1,2 % в период с 1997 по 2007 год[5].
Несмотря на обнадеживающие данные о выживаемости, долгосрочные последствия и заболеваемость среди выживших младенцев остаются серьёзной проблемой. К независимым факторам, ассоциированным с повышенным риском смертности, относятся[5]:
- низкие показатели по шкале Апгар (<3);
- необходимость в искусственной вентиляции легких (ИВЛ) продолжительностью более 48 часов;
- потребность в повторном назначении вазопрессорных препаратов для поддержания гемодинамики;
- назначение антибиотиков широкого спектра действия (например, цефотаксима), что может отражать тяжесть состояния и сопутствующие осложнения.
Что касается отдаленных последствий, у выживших детей наблюдается повышенная распространенность респираторной патологии. У младенцев, перенесших длительную искусственную вентиляцию легких, существует риск развития бронхолегочной дисплазии (БЛД). Исследования также показывают повышенную частоту астматических симптомов и аномальной бронхиальной реактивности в этой группе пациентов[5].
Наиболее серьёзную обеспокоенность вызывают неврологические исходы. Примерно у 21 % выживших после САМ в отдаленном периоде наблюдаются такие последствия, как детский церебральный паралич (ДЦП) или задержка общего развития, что подчеркивает важность последующего длительного наблюдения за этими пациентами[5].
Профилактика
Профилактикой САМ является уменьшение частоты переношенной беременности — индукция родов после 41 недели связана со значительным уменьшением частоты САМ по сравнению с выжидательной тактикой. Используемые профилактические стратегии малоэффективны в связи с тем, что аспирация мекония обычно происходит в пренатальном периоде[8].
Примечания
Литература
- Буштырева И. О., Чернавский В. В., Колганова А. А. Синдром аспирации мекония // Саратовский научно-медицинский журнал. — 2010. — № 2.
- Dini G., Ceccarelli S., Celi F., and other. Meconium aspiration syndrome: from pathophysiology to treatment (англ.) // Ann Med Surg.— 2024.— February (vol. 4, no. 86).— P. 2023—2031.— doi:10.1097/MS9.0000000000001835.