Врождённая мышечная дистрофия Ульриха
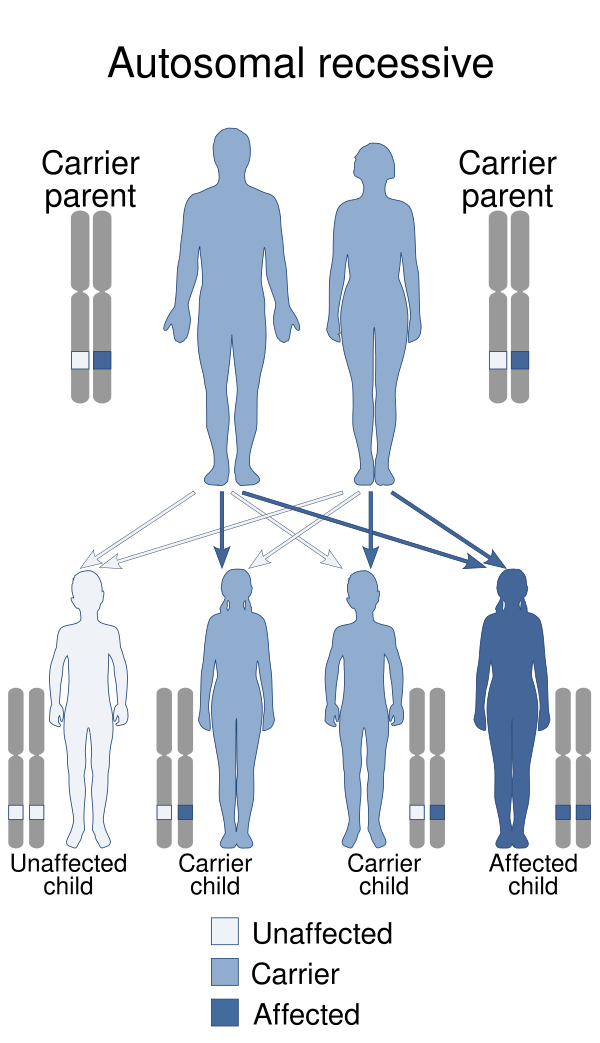
Врождённая мы́шечная дистрофи́я У́льриха (ВМДУ) — это генетически гетерогенное и клинически тяжёлое заболевание из группы врождённых мышечных дистрофий, в основе которого лежит дефект синтеза или структуры белка внеклеточного матрикса — коллагена VI типа. Патология обусловлена мутациями в генах COL6A1, COL6A2 или COL6A3 и может наследоваться как по аутосомно-доминантному, так и по аутосомно-рецессивному типу. Ключевые клинические критерии заболевания, проявляющиеся с рождения, включают триаду: врождённую мышечную слабость и гипотонию, контрактуры крупных суставов (тазобедренных, коленных, локтевых) и дистальную гипермобильность суставов кистей и стоп. Характерны также снижение двигательной активности плода, деформации позвоночника (кифосколиоз) и кожные изменения (келоидные рубцы, фолликулярный кератоз). Течение болезни прогрессирующее. Прогноз неблагоприятный[1][2].
Что важно знать
История
В 1930 году Отто Ульрих описал двух мальчиков с необычной врождённой миопатией, характеризующейся мышечной слабостью и истощением, выраженной гипермобильностью дистальных суставов и контрактурами проксимальных суставов, присутствующими с рождения или раннего младенческого возраста. Это новое состояние он обозначил термином «врождённая, атонически-склеротическая мышечная дистрофия, ещё один тип наследственно-дегенеративных заболеваний нервно-мышечной системы». Последующие исследованияподтвердили наследственный характер заболевания[3].
Классификация
Согласно международной классификации болезней 10-го пересмотра ВМДУ относится к мышечным дистрофиям (G71.2)[4].
Согласно международной классификации болезней 11-го пересмотра ВМДУ относится к врождённым миодистрофиям (8C70.6)[5].
Этиология
Патогенез
Патогенез ВМДУ связан с нарушениями в структуре коллагена VI типа. Этот белок является критически важным компонентом внеклеточного каркаса, или «миоматрикса», окружающего мышечные волокна и обеспечивающего им структурную поддержку[2].
Заболевание развивается по двум основным механизмам[2]:
- первый и наиболее распространённый — доминантно-негативный эффект. В этом случае даже одна мутантная копия гена производит аномальную молекулу коллагена. Эта молекула включается в процесс сборки белка и нарушает формирование всей структуры. Такой эффект вызывают конкретные типы мутаций, например, небольшие делеции в пределах экзона или замена критически важных аминокислот в цепи белка;
- второй механизм — полная потеря функции белка. Он характерен для рецессивной формы болезни и возникает, когда обе копии гена (унаследованные от отца и матери) неработоспособны. Это происходит из-за мутаций, которые приводят к полному прекращению производства нормального коллагена, например, нонсенс-мутаций, приводящих к синтезу укороченного и нестабильного белка[2].
Независимо от исходной генетической причины, конечный результат всегда один: структура внеклеточного матрикса мышц оказывается грубо нарушенной. Без прочной поддержки мышечные волокна становятся уязвимыми, повреждаются при нагрузке и постепенно замещаются рубцовой тканью. Этот процесс лежит в основе прогрессирующей мышечной слабости, потери двигательной функции и дыхательной недостаточности, характерных для ВМДУ[2].
Эпидемиология
ВМДУ является редким заболеванием с распространённостью 0.13 случая на 100 000 человек[7].
Диагностика
Первые признаки заболевания обычно отмечаются ещё во внутриутробном периоде в виде снижения двигательной активности плода. Характерные особенности при рождении включают мышечную гипотонию (сниженный тонус), кривошею, контрактуры проксимальных суставов, гипермобильность дистальных суставов кистей и стоп, кифосколиоз, аномальное положение рук и ног, вывих бёдра и выступающие пяточные кости. Часто наблюдается характерный округлый овал лица с лёгкой эритемой на щеках. Двигательные функции серьёзно нарушены. Не все пациенты достигают способности к самостоятельной ходьбе. У тех же, кто начинает ходить, прогрессирование мышечной слабости и контрактур приводит к потере этой способности к возрасту 10—11 лет. Примерно к 7 годам формируется ригидность (жёсткость) позвоночника с сопутствующим прогрессирующим сколиозом, что часто требует хирургической коррекции к 11 годам. Дыхательная система поражается у всех пациентов. Прогрессирующая дыхательная недостаточность неизбежно приводит к необходимости начала ночной неинвазивной вентиляции лёгких в режиме BiPAP. К 20-ти годам многим пациентам требуется и дневная респираторная поддержка. Типичными кожными проявлениями являются фолликулярный кератоз («гусиная кожа»), наиболее выраженный на разгибательных поверхностях конечностей, а также склонность к образованию келоидных и атрофических рубцов[6].
Магнитно-резонансная томография мышц: у пациентов с ВМДУ обычно наблюдается диффузное поражение мышц. Характерным признаком является относительное сохранение определённых мышц бедра, таких как портняжная мышца, тонкая мышца и длинная приводящая мышца. Также могут выявляться специфические паттерны жировой инфильтрации в других мышцах. В частности, в латеральной широкой мышце бедра часто описывают паттерн «извне-внутрь», а в прямой мышце бедра — паттерн «центрального облака». Однако по мере прогрессирования заболевания эти характерные находки могут становиться менее отчётливыми, поскольку жировое перерождение мышц становится более распространённым и однородным[2].
Электромиография выявляет типичную картину первичного мышечного поражения (миопатический паттерн). Характерно снижение амплитуды и укорочение длительности потенциалов двигательных единиц, повышенная полифазность. При максимальном усилии регистрируется низкоамплитудная, «пёстрая» интерференционная кривая. Признаки выраженной спонтанной активности обычно отсутствуют[8].
При гистологическом исследовании биоптата скелетной мышцы обычно выявляются дистрофические изменения, включающие дегенерацию и регенерацию мышечных волокон, а также их замещение жировой и соединительной тканью. Важно отметить, что у детей младше 30 месяцев изменения в биопсии могут быть минимальными и ограничиваться атрофией волокон или их типовой диспропорцией, без явных дистрофических признаков[2].
Иммуногистохимическое исследование на коллаген VI в мышечной ткани демонстрирует спектр аномалий: от полного отсутствия белка до его неправильного расположения в базальной мембране, что подтверждается отсутствием ко-локализации с другими маркерами, такими как перлекан, ламинин или коллаген IV[2].
Дополнительным диагностическим методом является иммуноцитохимический анализ культуры фибробластов кожи. Этот тест позволяет выявить нарушение отложения коллагена VI во внеклеточном матриксе, а также образование его аномальной структуры. При доминантно действующих патогенных вариантах часто наблюдается сильная внутриклеточная иммунореактивность после пермеабилизации клеток. Данный метод служит полезным вспомогательным инструментом для подтверждения диагноза[2].
Молекулярно-генетический анализ методом секвенирования: позволяет выявить мутации в генах COL6A1, COL6A2 и COL6A3[6].
Биохимический анализ крови: возможно повышение активности креатинфосфокиназы[8].
Дифференциальная диагностика
Дифференциальная диагностика ВМДУ проводится со следующими заболеваниями[6]:
- синдром Элерса — Данлоса;
- синдром Марфана;
- врождённая контрактурная арахнодактилия;
- другие формы врождённых мышечных дистрофий;
- спинальная мышечная атрофия;
- врождённая миотония;
- миопатия Бетлема.
Лечение
Этиологической терапии ВМДУ не существует. Однако комплексный поддерживающий уход, направленный на контроль ключевых проявлений болезни, позволяет существенно повысить качество жизни пациентов и улучшить прогноз. Ведущей и неотложной задачей является поддержка дыхательной функции. У всех пациентов примерно к 11 годам развивается тяжёлая дыхательная недостаточность, что делает обязательным использование ночной неинвазивной вентиляции лёгких, как правило, в режиме BiPAP. Без такой респираторной поддержки прогрессирующая дыхательная недостаточность приводит к летальному исходу в подростковом возрасте. Для очистки дыхательных путей от секрета активно используется механический инсуффлятор-экссуффлятор (кашлевой аппарат)[6].
Прогрессирующий кифосколиоз требует своевременной хирургической коррекции по показаниям. Физическая терапия играет ключевую роль в поддержании подвижности суставов. Применяются регулярные занятия по растяжке, плавание и акватерапия. Для коррекции контрактур ахиллова сухожилия применяются ортезы (шины) или, при необходимости, оперативное вмешательство (тенотомия). Также необходим контроль за питанием и нутритивная поддержка для борьбы с отставанием в физическом развитии[6].
Прогноз
ВМДУ это тяжёлое прогрессирующее заболевание. Прогноз в отношении двигательной функции неблагоприятный: большинство пациентов либо никогда не могут ходить самостоятельно, либо теряют эту способность в детском возрасте, становясь полностью зависимыми от кресла-коляски примерно к 10-11 годам. Ключевым фактором, определяющим прогноз для жизни, является поражение дыхательной мускулатуры. У всех больных развивается прогрессирующая дыхательная недостаточность. Без респираторной поддержки заболевание приводит к летальному исходу в подростковом возрасте[6].
Диспансерное наблюдение
Диспансерное наблюдение за пациентами с ВМДУ является комплексным и пожизненным, направленным на мониторинг и своевременную коррекцию угрожающих жизни осложнений. Ключевым направлением является мониторинг дыхательной функции. Для этого каждые шесть месяцев проводятся исследования функции внешнего дыхания (спирометрия) в положениях сидя и лёжа для выявления постурального снижения дыхательных объёмов, а также полисомнография для оценки ночной гиповентиляции. Полисомнография является критически важным исследованием для определения момента начала неинвазивной вентиляции лёгких (НИВЛ) в режиме BiPAP. После начала респираторной поддержки контрольные полисомнографии выполняются каждые один-два года[2].
Ежегодно проводится клинический и рентгенологический контроль сколиоза, а также кардиологическое обследование, включающее эхокардиографию и электрокардиографию, для оценки состояния сердца. Физиотерапевт и эрготерапевт должны оценивать мышечную слабость, контрактуры суставов и потребность в средствах передвижения также каждые полгода. Столь же часто необходимы консультации диетолога для оценки статуса питания и коррекции дефицита веса, который напрямую связан с дыхательной недостаточностью[2].
Профилактика
Генетическое консультирование является ключевым методом профилактики ВМДУ в семьях с установленным диагнозом. После выявления патогенных вариантов в генах коллагена VI у заболевшего родственника, становится возможным проведение пренатальной диагностики для будущей беременности, а также преимплантационное генетическое тестирование в рамках процедуры экстракорпорального оплодотворения[6].
Примечания
Литература
- Topaloğlu H., Poorshiri B. The congenital muscular dystrophies (англ.) // Annals of the Child Neurology Society. — 2024. — Vol. 2. — P. 27—39. — doi:10.1002/cns3.20050.
- Sirisena N. D., Samaranayake U. M. J. E., Neto O. L. A. et al. A novel variant in the COL6A1 gene causing Ullrich congenital muscular dystrophy in a consanguineous family: a case report (англ.) // BMC Neurology. — 2021. — Vol. 21. — P. 105. — doi:10.1186/s12883-021-02134-7.
- Yonekawa T., Nishino I. Ullrich congenital muscular dystrophy: clinicopathological features, natural history and pathomechanism(s) (англ.) // Journal of Neurology, Neurosurgery and Psychiatry. — 2015. — March (vol. 86, no. 3). — P. 280—287. — doi:10.1136/jnnp-2013-307052.