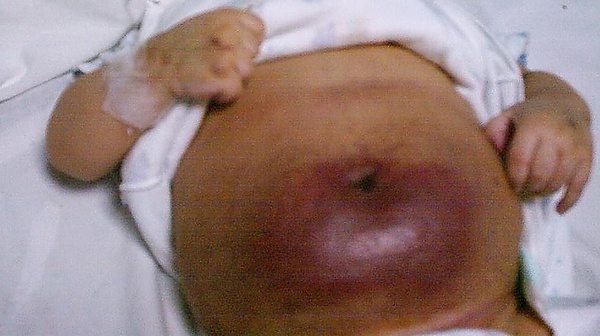
Синдром Казабаха ― Мерритт
Синдро́м Казаба́ха ― Мерри́тт (СКМ, синдро́м гемангио́мы с тромбоци́топени́ей) — редкое, но угрожающее жизни нарушение свёртываемости крови. Проявляется тромбоцитопенией, микроангиопатической гемолитической анемией и коагулопатией потребления на фоне быстрорастущей сосудистой опухоли. Этот феномен исключительно связан с сосудистыми опухолями — капошиформной гемангиоэндотелиомой и пучковой ангиомой, которые относятся к одному спектру неопластических заболеваний[1].
Общие сведения
История
В 1940 году американские педиатры Казабах и Мерритт впервые описали это заболевание, которое впоследствии получило название синдром Казабаха — Мерритт[2].
Классификация
Согласно классификации Международного общества изучения сосудистых аномалий, синдром Казабаха ― Мерритт относится к доброкачественным сосудистым опухолям, ассоциированным с мутацией в гене GNA14[2].
Этиология
СКМ развивается исключительно на фоне капошиформной гемангиоэндотелиомы (КГ) и пучковой ангиомы (ПА) — редких сосудистых опухолей, возникающих преимущественно у младенцев. Эти образования относятся к опухолям с промежуточным злокачественным потенциалом: они проявляют местно-агрессивный рост, но не склонны к метастазированию[1].
Современные исследования выявили генетическую природу заболевания. Установлена связь между развитием КГ и хромосомными аномалиями, включая транслокации в 13-й и 16-й хромосомах. Ключевым фактором в патогенезе этих сосудистых опухолей считается мутация гена GNA14, что подтверждается данными генетических исследований[2].
Патогенез
В основе развития СКМ лежит особая структура сосудов опухоли, представленная множеством извитых капилляров, отходящих непосредственно от крупных сосудов. Такое строение создаёт условия для турбулентного кровотока, что приводит к активации и агрегации тромбоцитов с образованием микротромбов. Этот процесс способствует развитию тромбоцитопении и коагулопатии потребления[1].
Согласно одной из гипотез, тромбоциты захватываются изменёнными эндотелиальными клетками опухоли, что провоцирует их активацию и агрегацию. Важную роль в этом процессе играет взаимодействие рецептора CLEC-2 (C-type lectin-like receptor-2) с подопланином — белком, участвующим в ангио- и лимфангиогенезе. Это взаимодействие дополнительно стимулирует активацию тромбоцитов. Параллельно в крови повышается уровень ангиопоэтина-2 — фактора роста, усиливающего ангиогенез, что приводит к неконтролируемой пролиферации сосудистых клеток[2].
Гистологически КГ и ПА представлены узлами, состоящими из веретенообразных эндотелиальных клеток и перицитов, формирующих щелевидные сосуды, а также участками с более дифференцированными капиллярными структурами. В просвете капилляров часто обнаруживаются микротромбы, агрегаты тромбоцитов и скопления эритроцитов[3].
Для КГ характерен инфильтративный рост в окружающие мышцы, тогда как при ПА дольчатые структуры расположены более поверхностно и дискретно. Это сходство гистологической архитектоники позволяет некоторым исследователям рассматривать ПА как «малую» форму КГ[3].
Иммуногистохимически на мембране эндотелиальных клеток выявляются панэндотелиальный маркер CD31, а также маркеры лимфатических сосудов — D2-40, PROX1 и подопланин. В ряде случаев опухоли, клинически соответствующие ПА, гистологически практически неотличимы от КГ, что подчёркивает их тесную патогенетическую связь[3].
Эпидемиология
Точная распространённость КГ и ПА остаётся неизвестной, однако эти опухоли считаются крайне редкими: их частота оценивается приблизительно в 0,07 случая на 100 000 населения. При этом СКМ развивается у 70 % пациентов с КГ и у 10 % больных с ПА. Заболевание встречается с одинаковой частотой у обоих полов и во всех этнических группах. В большинстве случаев опухоли проявляются в раннем младенческом возрасте — средний возраст постановки диагноза составляет около 2 месяцев. Крайне редко КГ может дебютировать во взрослом возрасте, однако в таких случаях она, как правило, не сопровождается развитием СКМ. Частота встречаемости СКМ в Российской Федерации достоверно не установлена. Заболевание в большинстве случаев манифестирует на первом году жизни. Примерно у половины пациентов связанная с этим состоянием сосудистая опухоль присутствует уже при рождении[1][2][3].
Диагностика
КГ проявляется в двух основных формах: кожной и висцеральной, причём висцеральная форма чаще всего локализуется в забрюшинном пространстве.
При кожной форме, поражающей мягкие ткани, клиническая картина достаточно характерна. В отличие от классических объёмных образований, выступающих над поверхностью кожи, КГ представляет собой инфильтративную опухоль, приводящую к диффузному увеличению поражённого участка тела. Опухоль может располагаться на любом участке, однако наиболее часто встречается на туловище и проксимальных отделах конечностей, с особым предпочтением естественных кожных складок.
Характерные признаки КГ включают:
- изменение цвета кожи над опухолью — от ярко-красного до багрового. При развитии СКМ появляются признаки локального геморрагического синдрома: петехии, экхимозы или индуративное пропитывание тканей кровью;
- отсутствие чётких границ опухоли, хотя в некоторых случаях пальпируются отдельные дольчатые структуры;
- выраженный локальный отёк поражённой области;
- плотная, иногда бугристая консистенция изменённых тканей;
- при СКМ в большинстве случаев (около 70 %) отмечается интенсивный болевой синдром, обусловленный как компрессией сосудисто-нервных пучков, так и повторяющимися кровоизлияниями в опухоль и окружающие ткани;
- повышение локальной температуры кожи над опухолью на 0,5—0,8 °C по сравнению с окружающими участками;
- возможны сопутствующие изменения кожи в виде локального гипергидроза и гипертрихоза;
- при расположении вблизи суставов может наблюдаться значительное ограничение движений[4].
При ПА клинические проявления обычно начинаются с небольшого пятна, которое постепенно прогрессирует в красно-фиолетовые бляшки или узлы размером 2—10 см. В отдельных случаях поражение может быть более обширным, достигая 7×12 см. Наиболее типичная локализация включает шею, плечи, верхнюю часть туловища и реже — проксимальные отделы конечностей[5].
СКМ проявляется характерной триадой гематологических нарушений, которые имеют яркие клинические проявления. В первую очередь развивается выраженный геморрагический синдром: на коже и слизистых появляются множественные точечные кровоизлияния (петехии) и обширные синяки (экхимозы), отмечается повышенная кровоточивость из мест инъекций, носовые и десневые кровотечения. В тяжёлых случаях возможны опасные для жизни желудочно-кишечные кровотечения или кровоизлияния в жизненно важные органы. Параллельно развиваются симптомы анемии: кожа и слизистые становятся бледными, появляется учащённое сердцебиение, слабость, у младенцев наблюдается вялость и плохая прибавка массы тела. Особенностью СКМ является сочетание кровоточивости с признаками диссеминированного внутрисосудистого свёртывания, что проявляется одновременным образованием микротромбов в области сосудистой опухоли, приводящим к ишемии окружающих тканей[6][7].
- Общий анализ крови: выявляет выраженную тромбоцитопению, анемию.
- Коагулограмма: удлинение протромбинового времени и активированного частичного тромбопластинового времени, гипофибриногенемия, повышение D-димера[1].
- При проведении магнитно-резонансной или компьютерной томографии обычно выявляется сосудистое образование с контрастным усилением, которое требует дифференциальной диагностики с сосудистыми мальформациями, солидными опухолями и другими пролиферативными сосудистыми поражениями[6].
- Ультразвуковое исследование с допплерографией является важным инструментом дифференциальной диагностики, позволяя отличить солидные образования от сосудистых поражений. КГ имеют ряд характерных особенностей: они располагаются в более глубоких слоях тканей, отличаются повышенной плотностью сосудистой сети и проявляют большую жёсткость при эластографическом исследовании. Наиболее показательным диагностическим признаком является значительное увеличение пиковой систолической скорости кровотока в образованиях. Трёхмерная цветная доплерография выявляет принципиальные различия в характере кровотока: для КГ характерно древовидное ветвление сосудов, в то время как ПА демонстрируют точечный или полосатый тип сосудистого рисунка. Эти диагностические особенности имеют ключевое значение для точной верификации диагноза и выбора оптимальной тактики лечения[6].
- Дополнительную диагностическую ценность представляют радионуклидные методы диагностики. Сканирование с использованием изотопов хрома-51, индия-111 или меченного йодом-131 фибриногена может обладать большей чувствительностью по сравнению со стандартными лучевыми методами при определении размеров и количества сосудистых образований[6].
- гистологическое исследование опухоли: может быть полезна для верификации типа опухоли. Однако биопсия сосудистой опухоли связана с высоким риском кровотечения[1].
Дифференциальная диагностика
Дифференциальную диагностику проводят со следующими состояниями[1][4]:
- ангиосаркома;
- артериовенозные мальформации;
- гемангиобластома;
- гемангиома печени;
- иммунная тромбоцитопеническая пурпура;
- тератома;
- нейробластома;
- RICH (rapidly involuting congenital hemangioma) синдром;
- мультифокальный лимфангиоэндотелиоматоз с тромбоцитопенией;
- капошиформный лимфангиоматоз;
- венозные сосудистые мальформации.
Осложнения
К осложнениями СКМ относятся[4][6]:
- изъязвление и кровоизлияние в сосудистое образование;
- кровотечение на фоне ДВС-синдрома, резистентное к переливанию тромбоцитов;
- сердечная недостаточность;
- инфекции вследствие повреждения кожи с риском сепсиса;
- деструкция костных структур;
- функциональные расстройства: вовлечение в патологический процесс суставов или мышц, может привести к нарушениям движения и контрактурам в этих суставах;
- некроз мягких тканей;
- сдавление регионарных нервных волокон (синдром Горнера, парез руки, парез гортани)
- Нарушение развития органов (гипоплазия почки, крипторхизм).
Лечение
Консервативная терапия СКМ включает два основных направления[3]:
- куративная терапия — воздействие на сосудистую опухоль;
- сопроводительная терапия — коррекция нарушений гемостаза.
Куративная терапия проводится поэтапно с применением трёх линий лечения:
1-я линия — неселективные β-блокаторы:
- назначаются всем пациентам перорально, начиная с низкой дозы с постепенным увеличением под кардиологическим контролем;
- при отсутствии эффекта в течение месяца или ухудшении состояния — переход на 2-ю линию.
2-я линия — метрономная химиотерапия:
- применяется при неэффективности β-блокаторов или при распространённых опухолях с инвазией в окружающие ткани;
- включает комбинацию цитостатиков курсами с интервалами.
3-я линия — липосомальные антрациклины:
- используется при резистентности к иным методам;
- вводится внутривенно циклами с контролем кумулятивной дозы.
Сопроводительная терапия
- гемотрансфузионная терапия: переливание тромбоцитарной массы, плазмы и эритроцитарной массы — при кровотечениях;
- ингибиторы фибринолиза: назначаются при выраженном геморрагическом синдроме с последующей отменой после стабилизации;
- антикоагулянты: показаны при микротромбообразовании в опухоли, несмотря на тромбоцитопению.
Радикальное лечение СКМ требует устранения первичной сосудистой опухоли. Хирургическое иссечение является оптимальным методом, однако часто оказывается невозможным из-за инфильтративного характера роста опухоли с вовлечением окружающих тканей и отсутствием чётких границ. При развитии СКМ оперативное вмешательство становится особенно рискованным в связи с выраженными гемодинамическими нарушениями[1].
Альтернативным методом может служить эмболизация питающих сосудов, однако её применение ограничено из-за наличия множественных источников кровоснабжения опухоли. Кроме того, процедура сопряжена с риском некроза окружающих тканей[1].
Лучевая терапия способна вызывать регресс опухоли, но её использование у детей имеет существенные ограничения из-за потенциальных отдалённых осложнений, включая задержку физического развития, нарушение роста и риск вторичных злокачественных новообразований[1].
Прогноз
СКМ характеризуется значительной вариабельностью показателей летальности — по данным различных исследований, смертность пациентов колеблется от 12 до 30 %. Прогноз заболевания определяется тремя ключевыми характеристиками опухоли: глубиной прорастания в окружающие ткани, анатомической локализацией и размерами образования. Наиболее опасными в плане прогноза считаются забрюшинные опухоли, тогда как поверхностные локализации имеют относительно более благоприятное течение. Основными причинами летальных исходов выступают жизнеугрожающие осложнения: профузные кровотечения, инвазия опухоли в критически важные анатомические структуры, развитие сердечной недостаточности, полиорганной недостаточности и сепсиса. При длительном наблюдении отмечается постепенное уменьшение выраженности опухолевых проявлений, хотя кожные изменения в виде стойкой пигментации могут сохраняться в течение многих лет. Важно подчеркнуть, что современные подходы к терапии позволяют существенно улучшить прогноз у большинства пациентов при условии своевременной диагностики и комплексного лечения[8].
Диспансерное наблюдение
Не разработано.
Профилактика
Не разработана.
Примечания
Литература
- Гунченко И. В. Синдром Казабаха — Меррит у новорождённого ребёнка // FORCIPE. — 2022. — № S3.
- Хачатрян Лили Альбертовна. Первый опыт монотерапии пропранололом синдрома Казабаха — Мерритт у детей // Педиатрия. Журнал им. Г. Н. Сперанского. — 2017. — № 4.
- Артамонов Рудольф Георгиевич, Глазунова Людмила Владиславовна, Бусова Елена Сергеевна, Поляков Михаил Викторович, Кирнус Наталия Игоревна. Синдром Казабаха — Мерритт, обусловленный каверномой воротной вены у мальчика 7 лет // Российский вестник перинатологии и педиатрии. — 2014. — № 6.