Дефицит фактора XII
Дефици́т фа́ктора XII (боле́знь Ха́гемана) представляет собой крайне редкое нарушение гемостаза, характеризующееся значительным снижением активности плазменного фактора XII, который играет важную роль в процессе свёртывания крови. Заболевание встречается чрезвычайно редко — его частота в популяции оценивается не более чем в 1 случай на 1 миллион человек[2][3]. В большинстве случаев болезнь наследуется по аутосомно-рецессивному типу, однако в отдельных семьях наблюдается аутосомно-доминантный тип передачи.
Общие сведения
История
Фактор Хагемана был впервые обнаружен в 1955 году, когда при плановом предоперационном анализе крови у 37-летнего железнодорожного тормозного кондуктора Джона Хагемана выявили удлинённое время свёртывания, хотя в анамнезе у него не было геморрагических симптомов. Гематолог Оскар Ратнофф установил, что у Хагемана отсутствовал ранее неизвестный фактор свёртывания. Позже Ратнофф выяснил, что дефицит фактора Хагемана наследуется по аутосомно-рецессивному типу[4].
Этиология
Фактор XII является β-глобулином из класса сериновых протеаз с молекулярной массой 80—84 кДа. Этот белок синтезируется в печени и нейтрофилах. Его структура включает 596 аминокислот, образующих две полипептидные цепи: тяжёлую и лёгкую, соединённые между собой дисульфидной связью. Фактор XII является продуктом экспрессии гена F12, расположенным на длинном плече 5-й хромосомы (локус 5q35.3). Мутация гена F12 вызывает снижение функциональной активности фактора XII в кровеносном русле. В научной литературе описано порядка 50 различных мутаций[5].
Патогенез
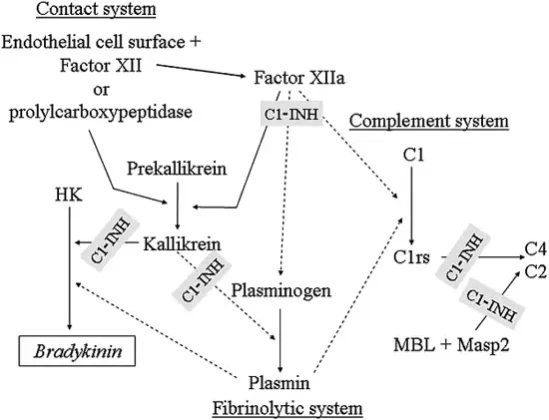
Функции фактора XII в системе свёртывания крови и его влияние на другие физиологические процессы остаются недостаточно изученными. Установлено, что данный белок играет ключевую роль в активации внутреннего пути коагуляции и фибринолиза, а также участвует в воспалительных реакциях через калликреин-кининовую систему с образованием брадикинина и систему комплемента. Кроме того, фактор XII вовлечён в процессы ангиогенеза[5].
При связывании с высокомолекулярным кининогеном активированный фактор XII инициирует каскад реакций свёртывания через активацию фактора XI, что в конечном итоге приводит к образованию тромбина. Тромбин выполняет ключевую роль в гемостазе, преобразуя фибриноген в фибрин и активируя тромбоциты. Параллельно взаимодействие фактора XII с калликреином способствует превращению плазминогена в плазмин, обеспечивая связь между калликреин-кининовой системой и фибринолизом. Мутация в гене F12 приводит к снижению активности фактора XII, что нарушает каскад процессов в системе гемостаза: возникает дисбаланс между свертывающей и фибринолитической системами. Снижение активации плазминогена через фактор XII может приводить к недостаточному фибринолизу. Кроме того, дефицит фактора XII может влиять на активацию тромбоцитов и воспалительные процессы, потенциально способствуя гиперкоагуляции[5].
Эпидемиология
Точные данные о распространённости дефицита фактора XII в популяции отсутствуют. Согласно ориентировочным оценкам, частота выявления этого заболевания составляет примерно 1 случай на 1 миллион человек. Однако предполагается, что реальная распространённость патологии может быть существенно выше, поскольку у большинства носителей мутации в гене F12 заболевание протекает бессимптомно и не диагностируется. Исследования показывают, что данный дефект чаще встречается среди представителей монголоидной расы[5].
Диагностика
Дефицит фактора XII в большинстве случаев протекает бессимптомно. Имеются данные о том, что дефицит фактора XII может повышать риск развития тромбоэмболических явлений. У таких пациентов теоретически может быть повышенная вероятность развития тромбоза глубоких вен или приобретённых тромботических нарушений по сравнению с общей популяцией. Однако эта взаимосвязь остаётся недоказанной[6].
В медицинской литературе также встречаются сообщения о возможной связи между дефицитом фактора XII и повторными необъяснимыми выкидышами у женщин. Однако эта взаимосвязь остаётся спорной и не имеет достаточных доказательств[6].
Спонтанные кровотечения при дефиците фактора XII наблюдаются крайне редко. В единичных случаях могут появляться мелкие кожные кровоизлияния (петехии), подкожные гематомы, носовые кровотечения или кровоточивость дёсен. При этом даже выраженный дефицит фактора XII не вызывает опасных кровопотерь и не приводит к развитию анемии. Характерно, что при травмах у таких пациентов не возникает патологической кровоточивости[5].
Коагулограмма: характерно удлинённое активированное частичное тромбопластиновое время, которое нормализуется при коррекционной пробе (смешивании с нормальной плазмой); нормальные показатели протромбинового времени, тромбинового времени и времени кровотечения.
Определение мутации в гене F12 посредством полимеразной цепной реакции или секвенирования нового поколения[7].
Дифференциальная диагностика
Дифференциальная диагностика дефицита фактора XII проводится со следующими состояниями[6][7]:
- гемофилия A (дефицит фактора VIII);
- гемофилия B (дефицит фактора IX);
- гемофилия C (дефицит фактора XI);
- дефицит фактора XIII;
- дефицит фибриногена;
- дефицит протромбина (фактора II);
- дефицит фактора V;
- дефицит фактора VII;
- дефицит фактора X;
- приобретённый дефицит фактора XII (при нефротическом синдроме, трансплантации печени, аутоиммунных заболеваниях);
- передозировка гепарином;
- дефицит высокомолекулярного кининогена;
- коагулопатии на фоне хронических заболеваний печени;
- коагулопатия на фоне системной красной волчанки;
- дефицит прекалликреина;
- коагулопатия на фоне антифосфолипидного синдрома.
Осложнения
К возможным осложнениям при дефиците фактора XII относятся[8]:
- инфаркт миокарда;
- выкидыши;
- острые нарушения мозгового кровообращения;
- тромбоэмболические явления.
Лечение
Дефицит фактора XII не требует специфического лечения. Существуют рекомендации, предостерегающие от необоснованного применения антифибринолитических средств (например, транексамовой кислоты) в данной группе пациентов из-за теоретической возможности провокации тромбозов. Особые сложности могут возникать при кардиохирургических операциях с искусственным кровообращением, поскольку изменения в коагулограмме затрудняют оценку адекватности гепаринизации.
Прогноз, как правило, благоприятный: пациенты имеют нормальную продолжительность жизни и не нуждаются в специальной терапии. Данные о возможной связи этого состояния с повышенным тромботическим риском остаются противоречивыми. Крупные клинические исследования не выявили значительного увеличения частоты тромботических осложнений у таких пациентов[9].
Примечания
Литература
- Яковлева Е. В., Зозуля Н. И. Физиологическая и патологическая роль фактора свёртывания крови XII // Гематология и трансфузиология. — 2022. — Т. 67, № 4. — С. 570—578. — doi:10.35754/0234-5730-2022-67-4-570-578.
- Н А. Воробьёва, М В. Елизаров, А В. Аверьянова, М А. Путанов, Н Я. Шемякина. Периоперационное ведение пациента с наследственным дефицитом фактора свёртывания крови XII при кардиохирургической операции (клинический случай) // Анестезиология и реаниматология. — 2019. — № 3. — doi:10.17116/anaesthesiology201903197.