Подопланин
Что важно знать
Структура и функция
Подопланин — интегральный мембранный белок типа I, сильно O-гликозилированный гликопротеин типа муцинов, с молекулярной массой 36—43 кДа. В царстве животных это достаточно консервативный белок: его гомологи есть у человека, мышей, крыс, собак и хомяков[8].
Подопланин широко распространён в тканях человека. Гомологи данного белка у других видов выполняют функцию антигенов дифференцировки и рецепторов вируса гриппа. Конкретная функция белка у человека не идентифицирована, но предполагается, что он может быть маркером повреждения лёгких. Были получены альтернативно сплайсированные варианты, кодирующие разные изоформы[7].
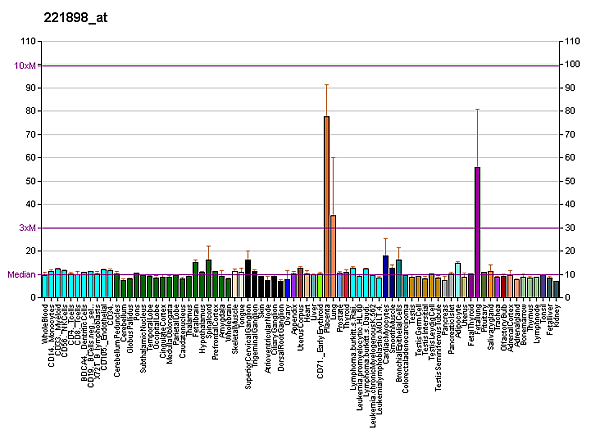
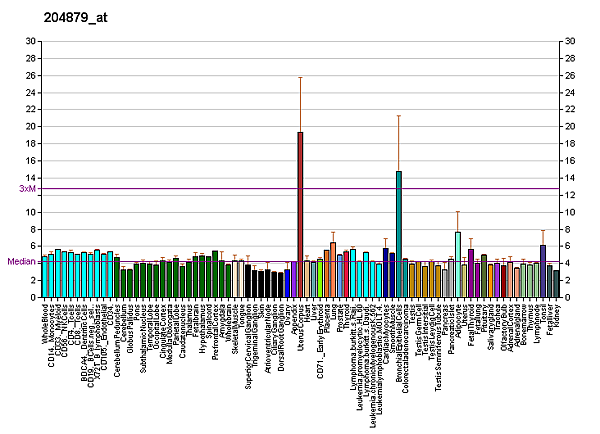
Было обнаружено, что подопланин функционирует в альвеолярных клетках лёгких, подоцитах почек и клетках эндотелия лимфатической системы. Также этот белок был обнаружен в образцах нервной ткани мышей и человека[9]. Кроме того, было продемонстрировано, что подопланин играет роль в разделении лимфатической и кровеносной системе во время эмбрионального развития, а его дефицит приводит к стеатозу печени у мышей[9].
Хотя конкретная функция подопланина неизвестна, была отмечена его колокализация с белком промежуточных филаментов нестином, который экспрессируется практически исключительно в нервной ткани[10]. По состоянию на 2013 год, единственный белок, с которым как известно взаимодействует подопланин — это лектин-подобный рецептор CLEC-2 (англ. C-type lectin-like receptor 2)[11]. Оба этих белка играют роль в правильном формировании связей лимфатической и кровеносной систем во время эмбрионального развития.
Клиническое значение
Подопланин активно изучается онкологами. Он является специфичным маркером лимфатических сосудов. Поскольку лимфангиогенез (формирование новых лимфатических сосудов) коррелирует с плохим прогнозом у раковых больных, подопланин может быть полезным диагностическим маркером[8]. Отмечена положительная регуляция подопланина в различных видах опухолей, например в нескольких видах карциномы плоского эпителия, злокачественной мезотелиоме и опухолях мозга[8]. Кроме того, он положительно регулируется ассоциированными с опухолью фибробластами (англ. cancer-associated fibroblasts (CAFs)) в опухолевой строме[8][12], что ассоциируется с неблагоприятным прогнозом течения болезни[13].
В карциномах плоского эпителия подопланин играет ключевую роль в инвазивности раковых клеток, контролируя инвадоподии, что обеспечивает эффективную деградацию внеклеточного матрикса[14].