Врождённый дефицит фактора XIII
Врождённый дефици́т фа́ктора свёртывания кро́ви XIII (врождённый дефици́т фа́ктора Ла́ки — Ло́ранда, дефици́т фибри́н-стабилизи́рующего фа́ктора, дефици́т фа́ктора XIII) — редкое наследственное заболевание системы гемостаза, характеризующееся нарушением стабилизации фибринового сгустка вследствие снижения активности фактора XIII[2][3]. Заболевание вызывается мутациями в генах F13A1 (кодирует A-субъединицу) или F13B (кодирует B-субъединицу), ответственных за синтез функционального комплекса фактора XIII[2]. Наследуется по аутосомно-рецессивному типу. Клинические проявления включают пупочные, подкожные, мышечные, суставные и внутричерепные кровоизлияния, замедленное заживление ран, склонность к дефектному формированию рубцовой ткани[2][4]. У женщин часто наблюдается повторные эпизоды невынашивания беременности[5]. Стандартные коагуляционные тесты обычно не выявляют патологии, поэтому для диагностики требуются специфические исследования активности фактора XIII и молекулярно-генетическое тестирование[5][6]. Основу лечения составляет заместительная терапия препаратами, содержащими фактор XIII. При своевременной диагностике и адекватном лечении прогноз благоприятный[6].
Что важно знать
История
Первые предположения о существовании XIII фактора свёртывания крови были выдвинуты в 1948 году. В начале 1960-х годов американские учёные Кальман Лаки и Ласло Лоранд, работая в лаборатории Альберта Сент-Дьёрдьи, при изучении процессов коагуляции выявили вещество, обладающее способностью стабилизировать фибриновый сгусток за счёт образования поперечных связей между фибриновыми мономерами. Открытый ими фактор был первоначально назван фактором Лаки — Лоранда, а впоследствии был официально обозначен как фактор XIII[2].
Классификация
Классификация по степени тяжести[4]:
- лёгкая — активность фактора свёртывания XIII > 30 %;
- средняя — активность фактора свёртывания XIII — 5—10 %;
- тяжёлая — активность фактора свёртывания XIII — 1—5 %.
В зависимости от соотношения активности антигена FXIII-A и FXIII-B различают 3 типа дефицита[5]:
- I тип — снижение активности фактора XIII вследствие малого количества антигена А-субъединицы;
- II тип — антиген А-субъединицы функционально неактивен;
- III тип — снижение активности фактора XIII вследствие малого количества В-субъединицы.
Этиология
Врождённый дефицит фактора свёртывания крови XIII — аутосомно-рецессивное заболевание, вызванное мутациями в генах F13A1 или F13B. Ген F13A1, расположенный на коротком плече 6-й хромосомы (6p24.2-p23), состоит из 15 экзонов и кодирует каталитическую субъединицу фактора XIII (FXIII-A), которая синтезируется в мегакариоцитах, моноцитах и макрофагах. Ген F13B, расположенный на длинном плече 1-й хромосомы (1q31-q32.1), состоит из 12 экзонов и кодирует некаталитическую субъединицу (FXIII-B), синтезируемую в гепатоцитах. В зрелой циркулирующей форме фактор XIII представлен в виде гетеротетрамера FXIII-A2B2, состоящего из двух А-субъединиц и двух В-субъединиц[5][6][7].
По данным на 2016 год описано более 150 мутаций[8], ассоциированных с дефицитом фактора свёртывания XIII, среди которых преобладают миссенс-мутации, преимущественно в гене F13A1. Мутации в F13B выявляются реже (менее 5 % случаев) и обычно протекают клинически легче. FXIII-B функционирует как носитель и стабилизатор субъединицы A, препятствуя её спонтанной активации. Дефекты субъединицы B приводят к нестабильности комплекса FXIIIA2B2 и относительному дефициту активной формы субъединицы A[6][7].
Большинство мутаций вызывают снижение активности фактора XIII ниже 5 % от нормы, что клинически сопровождается нарушением стабилизации фибринового сгустка[9].
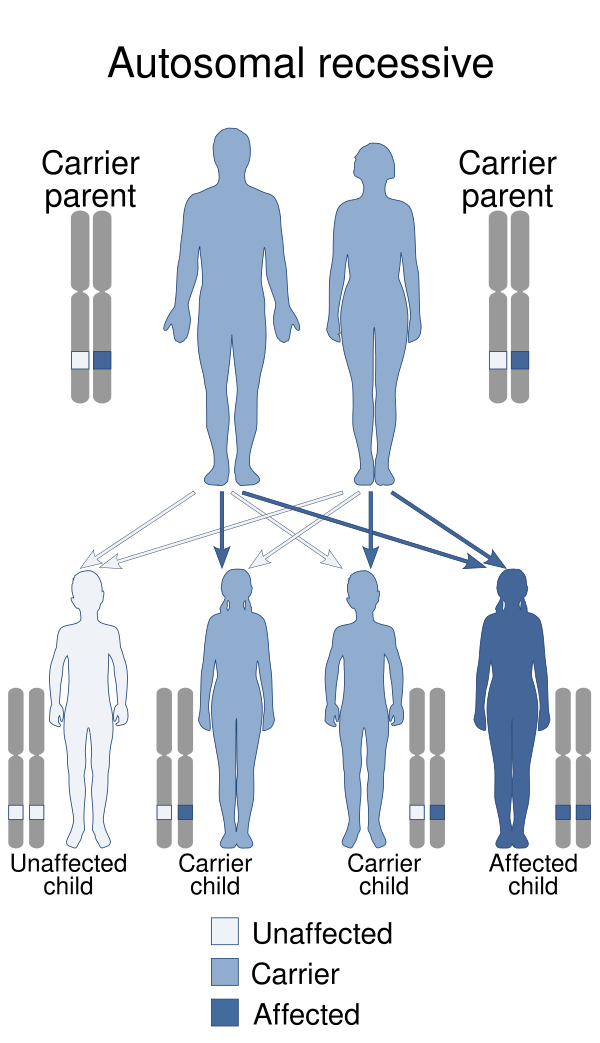
Клинически дефицит фактора свёртывания крови XIII манифестирует только в случае гомозиготного или компаунд-гетерозиготного носительства патогенных вариантов. Родственные браки увеличивают вероятность рождения больного ребёнка, так как повышается шанс совпадения мутаций у обоих родителей[7].
Патогенез
Фактор свёртывания крови XIII представляет собой зимоген, циркулирующий в плазме в виде гетеротетрамера FXIIIA2B2. После активации тромбином в присутствии ионов кальция FXIII-A превращается в активную трансглутаминазу (FXIIIa). В активной форме FXIIIa катализирует образование ковалентных связей между мономерами фибрина, стабилизируя фибриновый сгусток и обеспечивая его устойчивость к протеолитическому лизису (фибринолизу)[5][6][7].
При дефиците фактора свёртывания крови XIII нарушается третий этап гемостаза — стабилизация сформированного сгустка. Первоначально образовавшийся сгусток остаётся рыхлым и легко разрушается, что приводит к замедленным или повторным кровотечениям[5][6].
Фактор свёртывания крови XIII также участвует в[5][6]:
- заживлении ран (через сшивание компонентов внеклеточного матрикса — фибронектина, тромбоспондина, коллагена);
- ангиогенезе (через активацию рецептора VEGFR-2 на эндотелиальных клетках);
- регуляции воспаления и иммунного ответа (модулируя активность моноцитов и макрофагов);
- поддержании беременности, остеогенезе и кардиопротекции.
В связи с этим дефицит фактора свёртывания крови XIII сопровождается не только геморрагическим синдромом, но и нарушениями репарации тканей, замедленным заживлением ран и склонностью к выкидышам[5][6].
Эпидемиология
Распространённость врождённого дефицита фактора свёртывания крови XIII составляет, по данным разных исследований, от 1 до 3 случаев на 1 миллион населения[2][9]. В отдельных публикациях указывается более низкий уровень — около 1 случая на 2—3 миллиона человек[5][6]. Согласно данным Всемирной федерации гемофилии и национальных регистров, дефицит фактора XIII составляет приблизительно 6,5 % среди всех редких нарушений свёртывания крови[2].
Наибольшая частота заболевания отмечается в регионах с высокой долей родственных браков, например, в Иране. При этом существенных различий по расовым или этническим признакам не зафиксировано[6].
Клиническая картина
Врождённый дефицит фактора свёртывания крови XIII может проявляться с рождения и сопровождается широким спектром геморрагических симптомов, выраженность которых коррелирует с активностью фактора XIII в плазме[4]. При активности менее 1 % заболевание, как правило, дебютирует в неонатальном периоде. Одним из наиболее характерных признаков является кровотечение из пуповинного остатка, которое наблюдается примерно у 80 % новорождённых[2][9][10].
У младенцев и детей раннего возраста могут развиваться внутричерепные кровоизлияния (около 30 % случаев[4]), кровоизлияния в спинной мозг, внутримышечные гематомы, гемартрозы, кровотечения из слизистых оболочек и отсроченное кровотечение после незначительных травм или хирургических вмешательств. Внутричерепные кровоизлияния представляют особую клиническую и прогностическую значимость, являясь одной из ведущих причин смертности и инвалидизации при дефиците фактора свёртывания XIII. Внутричерепные кровоизлияния у детей первого года жизни могут вызвать джексоновскую эпилепсию. Возможны рецидивы таких кровотечений[2][3][9].
У детей старшего возраста и взрослых часто наблюдаются носовые кровотечения, кровоизлияния в мягкие ткани, склонность к образованию гематом, отсроченное послеоперационное кровотечение. В некоторых случаях возникают кровотечения из желудочно-кишечного тракта, мочевыводящих путей или в брюшную полость и забрюшинное пространство[2][9]. Редко встречаются кровоизлияния в селезёнку, лёгкие, уши или глаза[3]. Важной особенностью заболевания является замедленное заживление ран и дефектное формирование рубцовой ткани[4].
У женщин заболевание может проявляться в виде тяжёлых и длительных менструаций (меноррагии), а также повторных эпизодов невынашивания беременности[5][9]. У мужчин с дефицитом фактора свёртывания крови XIII могут наблюдаться фертильные нарушения[10].
При более высоком уровне активности фактора свёртывания XIII (1—4 %) симптомы, как правило, менее выражены и ограничиваются посттравматическими или послеоперационными кровотечениями. У гетерозиготных носителей заболевание, как правило, протекает бессимптомно[2].
Диагностика
- Коагулограмма — нормальные показатели протромбинового времени, активированного частичного тромбопластинового времени, тромбинового времени и концентрации фибриногена, проводится для дифференциальной диагностики с другими заболеваниями[6].
- Определение концентрации фактора свёртывания XIII в сыворотке крови[6].
- Молекулярно-генетическое исследование генов F13A1 и F13B — секвенирование генов F13A1 и F13B для исключения приобретённого дефицита фактора XIII[5][6].
- Тромбоэластография — позволяет оценивать состояние системы свёртывания крови. Однако тромбоэластография не является надёжным диагностическим методом для выявления врождённого дефицита фактора свёртывания крови XIII[6].
Дифференциальная диагностика
- Врождённая афибриногенемия
- Дисфибриногенемия
- Дефицит ингибитора альфа-2-антиплазмина
- Врождённый дефицит ингибитора активатора плазминогена 1-го типа
- Гемофилия A
- Гемофилия В
- Болезнь Виллебранда
- Тромбастения Гланцмана
- Синдром Бернара — Сулье
- Дефицит фактора II
- Дефицит фактора V
- Дефицит фактора VII
- Дефицит фактора X
- Дефицит фактора IX
- Дефицит фактора XI
- Приобретённый дефицит фактора XIII[6]
Осложнения
Лечение
Основным методом лечения врождённого дефицита фактора свёртывания XIII является заместительная терапия, направленная на восстановление его концентрации в плазме крови. Предпочтительно использование концентратов фактора XIII, полученных из донорской плазмы или с помощью рекомбинантных технологий. Эти препараты обеспечивают эффективное купирование кровотечений и профилактику их возникновения[5].
Плазменные концентраты содержат обе субъединицы фактора XIII (A и B) и поэтому подходят для всех типов дефицита. Рекомбинантные препараты содержат только A-субъединицу и применяются при наиболее распространённой форме — дефиците A-субъединицы, который встречается примерно в 95 % случаев. На 2025 год ни плазменные, ни рекомбинантные концентраты фактора XIII не зарегистрированы на территории Российской Федерации, что ограничивает их использование в рутинной клинической практике[5].
В условиях отсутствия специализированных препаратов в качестве альтернативы применяются[3][7]:
- криопреципитат, содержащий фактор XIII, но в меньшем объёме по сравнению с концентратами;
- свежезамороженная плазма — содержит все факторы свёртывания, но требует введения больших объёмов и сопровождается повышенным риском побочных эффектов (инфекции, аллергические реакции).
Антифибринолитические препараты могут применяться при лёгких кровотечениях, а также в периоперационном периоде. У женщин с чрезмерными менструальными кровотечениями могут использоваться гормональные контрацептивы в качестве поддерживающей терапии[3].
В редких случаях у пациентов могут развиваться ингибиторы (аутоантитела) к фактору XIII, что приводит к снижению эффективности заместительной терапии. В таких ситуациях проводится иммуносупрессивная терапия[5][6].
Прогноз
Профилактика
Профилактическое лечение рекомендовано пациентам с тяжёлой формой заболевания или активностью фактора XIII менее 5 %, поскольку при таких показателях значительно возрастает риск развития спонтанных, в том числе внутричерепных, кровоизлияний. Цель терапии — поддерживать активность фактора на безопасном уровне для предотвращения жизнеугрожающих кровотечений[5][6].
В качестве основного средства профилактики применяются концентраты фактора свёртывания крови XIII. При их недоступности допустимо использование криопреципитата или свежезамороженной плазмы[5][6]. Профилактика может быть[6]:
- долгосрочной — с регулярным введением препаратов для поддержания безопасного уровня фактора XIII;
- краткосрочной — перед оперативными вмешательствами или родами.
У беременных женщин с тяжёлым дефицитом фактора XIII профилактика является обязательной. Цель — поддержание активности фактора свёртывания крови XIII выше 10 %, особенно во втором и третьем триместрах. Лечение подбирается индивидуально и продолжается на протяжении всей беременности с коррекцией схемы во втором и третьем триместрах. Это позволяет существенно снизить риск выкидышей и осложнений при родах[5][6].