Оксид азота(I)
Окси́д азо́та(I) (окси́д диазо́та, за́кись азо́та, веселя́щий газ) — химическое соединение. Бесцветный негорючий газ.
Закись азота является третьим по значимости парниковым газом, накопление которого в атмосфере Земли — одна из причин глобального потепления, так как оксид азота является веществом, разрушающим стратосферный озон[2].
С 1 января 2021 года в Российской Федерации действует Федеральный закон от 29.12.2020 г. № 472-ФЗ «Об ограничении оборота закиси азота». Запрещаются нелегальное производство, закупка, поставка, хранение, перевозка, пропаганда использования не в целях производства пищевой продукции, продовольственных товаров, продуктов питания, медицинского, промышленного применения[3][4][5].
Общие сведения
| Оксид азота(I) | |
|---|---|
| Общие | |
| Систематическое наименование |
Оксонитрид азота(I) |
| Хим. формула | N2O |
| Физические свойства | |
| Состояние | бесцветный газ |
| Молярная масса | 44,0128 г/моль |
| Плотность | 1,98 г/л (при н. у.) |
| Энергия ионизации | 12,89 ± 0,01[1] |
| Термические свойства | |
| Температура | |
| • плавления | -90,86 °C |
| • кипения | -88,48 °C |
| • разложения | выше +500 °C |
| Давление пара | 51,3 ± 0,1[1] |
| Классификация | |
| Рег. номер CAS | 10024-97-2 |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 948 |
| UNII | K50XQU1029 |
| CompTox Dashboard EPA | DTXSID8021066 |
| Рег. номер EINECS | 233-032-0 |
| SMILES | |
| InChI | |
| Кодекс Алиментариус | E942 |
| RTECS | QX1350000 |
| ChEBI | 17045 |
| ChemSpider | 923 |
| ECHA InfoCard | 100.030.017 |
| Безопасность | |
| Пиктограммы СГС |
|
| NFPA 704 | |
История
Впервые был получен в 1772 году Джозефом Пристли, который назвал его «дефлогистированным нитрозным воздухом»[6]. В 1799 году его исследовал английский химик Гемфри Дэви.
Строение молекулы
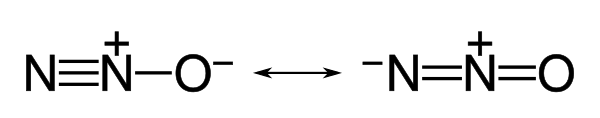
Строение молекулы оксида азота(I) описывается следующими резонансными формами:
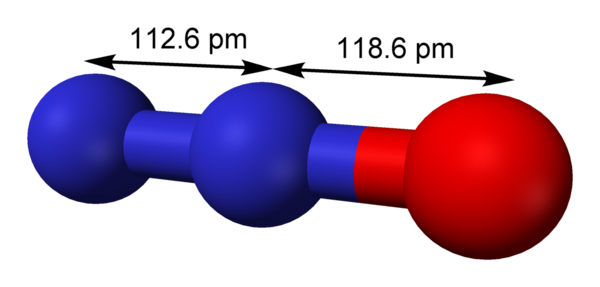
Наибольший вклад вносит N-оксидная форма оксида азота(I). Порядок связи N-N оценивается как 2,73, порядок связи N-O — как 1,61. Резонансная структура с возможностью противоположного расположения зарядов в молекуле N2O обусловливает низкий дипольный момент молекулы, равный 0,161 Д.
Физические свойства
Бесцветный газ, тяжелее воздуха (относительная плотность 1,527), с характерным сладковатым запахом. Растворим в воде (0,6 объёма N2O в 1 объёме воды при 25 °C, или 0,15 г/100 мл воды при 15 °C), растворим также в этиловом спирте, эфире, серной кислоте. При 0 °C и давлении 30 атм, а также при комнатной температуре и давлении 40 атм сгущается в бесцветную жидкость. Из 1 кг жидкой закиси азота образуется 500 л газа. Молекула закиси азота имеет дипольный момент 0,161 Д, коэффициент преломления в жидком виде равен 1,330 (для жёлтого света с длиной волны 589 нм). Давление паров жидкого N2O при 20 °C равно 5 150 кПа.
Химические свойства
Относится к несолеобразующим оксидам, с водой, с растворами щелочей и кислот не взаимодействует. Не воспламеняется, но поддерживает горение: тлеющая лучина, опущенная в него, загорается, как в чистом кислороде. Смеси с эфиром, циклопропаном, хлорэтаном в определённых концентрациях взрывоопасны. Оксид азота(I) является озоноразрушающим веществом, а также парниковым газом. В нормальных условиях N2O химически инертен, при нагревании проявляет свойства окислителя:
При взаимодействии с сильными окислителями N2O может проявлять свойства восстановителя:
При нагревании выше +500 °C N2O разлагается:
Оксид азота(I) реагирует с амидами металлов с образованием соответствующих неорганических азидов:
При взаимодействии с аммиаком над катализатором образуется азид аммония:
Биологическое значение
Закись азота образуется как при ферментативном, так и при неферментативном восстановлении из окиси азота (II)[7]. В организме бактерий закись азота образуется в ходе процесса денитрификации, катализируемого нитрооксид-редуктазой. Ранее этот процесс предполагался специфичным для некоторых видов бактерий и отсутствующим у млекопитающих, но новые данные заставляют предполагать, что это не так. Было показано, что физиологически релевантные концентрации закиси азота ингибируют как ионные токи, так и опосредуемые эксайтотоксичностью нейродегенеративные процессы, происходящие при чрезмерном возбуждении NMDA-рецепторов[8]. Также закись азота ингибирует биосинтез метионина, угнетая активность метионин-синтетазы и скорость превращения гомоцистеина в метионин и повышая концентрацию гомоцистеина в культурах лимфоцитов[9] и в биоптатах человеческой печени[10]. Хотя закись азота не является лигандом для гема, и не реагирует с тиоловыми группами, она обнаруживается во внутренних структурах гемосодержащих белков, таких, как гемоглобин, миоглобин, цитохромоксидаза[11]. Способность закиси азота нековалентно, обратимо изменять структуру и функции гемосодержащих белков была показана исследованием сдвига инфракрасных спектров тиоловых групп цистеинов гемоглобина[12] и тем, что закись азота способна частично и обратимо ингибировать функцию цитохромоксидазы C[13]. Точные механизмы этого нековалентного взаимодействия закиси азота с гемосодержащими белками и биологическое значение этого явления заслуживают дальнейших исследований. Обладает нейротоксическими свойствами.
Применение
Существует два вида закиси азота — пищевая, или медицинская для медицинского применения (высокой степени очистки), и техническая — технический оксид диазота, в котором есть примеси, количество которых указывается в соответствующих техусловиях (ТУ) на данный газ. «Медицинская» закись азота используется в основном как средство для ингаляционного наркоза, находит применение и в пищевой промышленности (например, для изготовления взбитых сливок) в качестве пропеллента. Также иногда используется для улучшения технических характеристик двигателей внутреннего сгорания. Может использоваться в ракетных двигателях в качестве окислителя, а также как единственное топливо в монокомпонентных ракетных двигателях.
В атмосфере
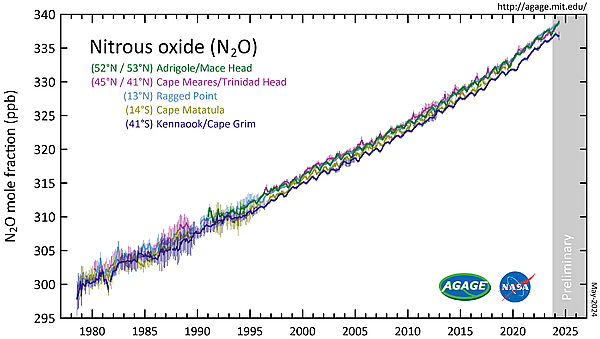
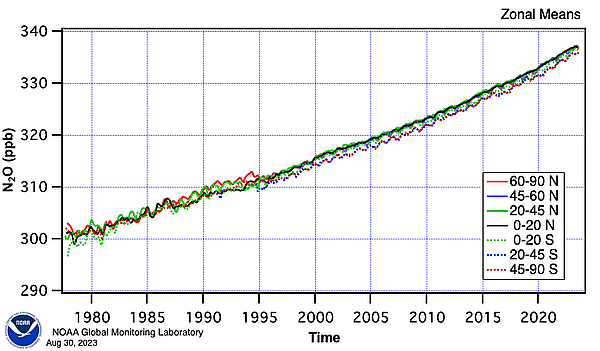
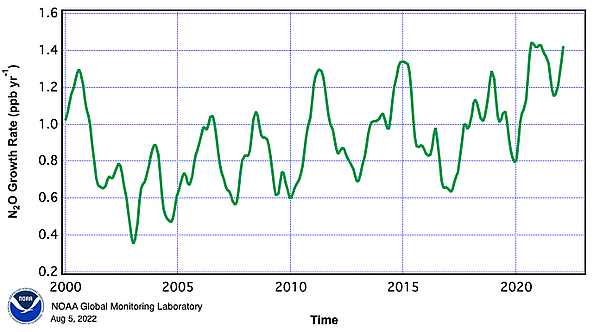
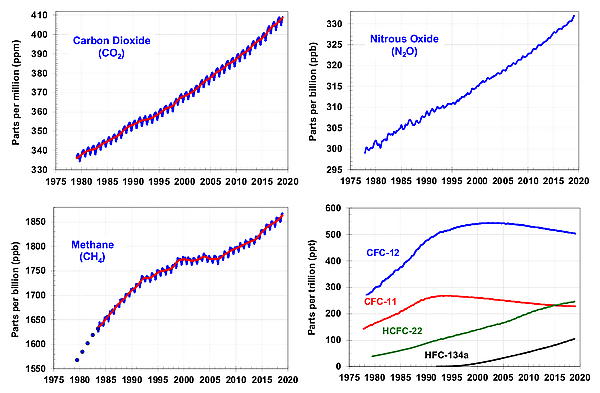
Закись азота является незначительным компонентом земной атмосферы и активно участвует в планетарном круговороте азота. Согласно анализу проб воздуха, взятых в разных точках мира, его концентрация в 2017 году превысила 330 частей на миллиард[14]. Темпы роста, составляющие около 1 части на миллиард в год, в последние десятилетия также ускорились[15].
Содержание закиси азота в атмосфере выросло более чем на 20 % по сравнению с базовым уровнем около 270 частей на миллиард в 1750 году[16].
Важные атмосферные свойства N2O представлены в следующей таблице:
| Собственность | Значение |
|---|---|
| Потенциал разрушения озонового слоя (ПРОС) | 0.017[18] (CCl3F = 1) |
| Потенциал глобального потепления (ПГП: 100-летний период) | 273[19] (CO2 = 1) |
| Срок службы в атмосфере | 116 ± 9 лет[20] |
В 2022 году МГЭИК сообщила, что: «Антропогенное нарушение естественного цикла азота в результате использования синтетических удобрений и навоза, а также осаждение азота в результате наземного земледелия и сжигания ископаемого топлива стало крупнейшей причиной увеличения содержания N2O в атмосфере на 31,0 ± 0,5 ppb (10 %) в период с 1980 по 2019 год»[20].
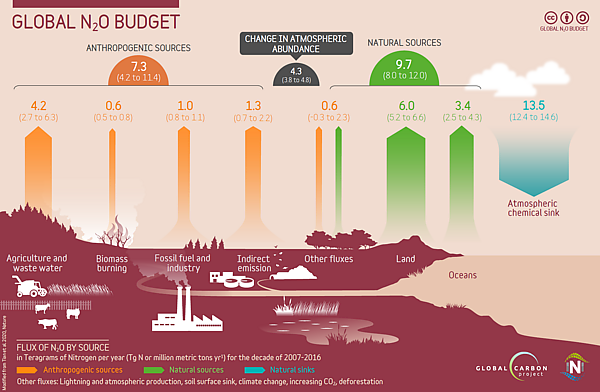
В 2007—2016 годах в среднем на планете за год выбрасывалось 17,0 (от 12,2 до 23,5) млн тонн в N2O. Около 40 % выбросов приходится на долю человека, а остальные является частью естественного круговорота азота[21][22].
Основными компонентами антропогенных выбросов являются удобренные сельскохозяйственные почвы и навоз домашнего скота (42 %), стоки и выщелачивание удобрений (25 %), сжигание биомассы (10 %), сжигание ископаемого топлива и промышленные процессы (10 %), биологическая деградация других азотсодержащих атмосферных выбросов (9 %) и сточные воды человека (5 %)[23][24].
Среди промышленных выбросов крупнейшим источником выбросов закиси азота является производство азотной кислоты и адипиновой кислоты. Выбросы адипиновой кислоты происходят в результате разложения нитроловой кислоты, образующейся при нитровании циклогексанона[25][26][27].
Глобальный учёт источников и поглотителей N2O за десятилетие, закончившееся в 2016 году, показывает, что около 40 % из среднегодовых 17 ТгN/год (тераграммов, или миллионов метрических тонн, азота в год) выбросов были вызваны деятельностью человека, и что рост выбросов в основном связан с развитием сельского хозяйства[28].
Закись азота обладает значительным потенциалом глобального потепления как парниковый газ. Если рассматривать каждую молекулу в отдельности за 100-летний период, то окажется, что закись азота в 265 раз сильнее удерживает тепло в атмосфере, чем углекислый газ (CO2). Однако из-за его низкой концентрации (менее 1/1000 от концентрации CO2) его вклад в парниковый эффект составляет менее трети от вклада углекислого газа, а также меньше, чем у метана[29]. С другой стороны, поскольку около 40 % N2O, попадающего в атмосферу, является результатом деятельности человека, контроль над выбросами закиси азота является частью усилий по сдерживанию выбросов парниковых газов[30].
Повышение концентрации закиси азота в атмосфере могло стать одной из причин чрезвычайно сильного глобального потепления во время граничного между сеноманом и туром события[31].
Закись азота также причастна к истончению озонового слоя. Исследование, проведённое в 2009 году, показало, что выбросы N2O являются самым важным фактором, разрушающим озоновый слой, и ожидается, что они останутся самыми значительными в XXI веке[32].
Примечания
Литература
- Леонтьев А. В., Фомичёва О. А., Проскурнина М. В., Зефиров Н. С. Современная химия оксида азота(I) // Успехи химии. — Российская академия наук, 2001. — Т. 70, № 2. — С. 107—122.
- Машковский М. Д. Закись азота // Лекарственные средства. — 15-е изд. — М.: Новая Волна, 2005. — 1200 с. — ISBN 5-7864-0203-7.






![{\displaystyle {\mathsf {2NH_{3}+N_{2}O{\xrightarrow[{}]{Ni-Al_{2}O_{3}}}NH_{4}N_{3}+H_{2}O}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/15abbaecda2c68518b6ec0f22e7bf16956327c9c)