Аутоиммунный лимфопролиферативный синдром
Аутоимму́нный лимфопролиферати́вный синдро́м (АЛПС; синдро́м Кана́ле — Сми́та) — редкое наследственное заболевание из группы первичных иммунодефицитов. Для него характерны хроническое увеличение лимфатических узлов, печени и селезёнки, обусловленное нарушением механизма апоптоза — запрограммированной гибели клеток. Хотя болезнь может начаться в любом возрасте, её первые признаки чаще всего проявляются уже в первые два года жизни пациента. В основе заболевания лежат мутации в ряде генов: FAS, FASLG, CASP10, CASP8, PRKCD, NRAS и CTLA4. Лечение обычно начинают лишь при развитии аутоиммунной цитопении. Более чем у 20 % пациентов заболевание приводит к летальному исходу из-за развития злокачественных опухолей. Если же опухолевые процессы не возникают, с течением времени наблюдается постепенное ослабление клинических проявлений синдрома[2].
Что важно знать
История
История изучения АЛПС начинается в 1967 году, когда исследователи Канале и Смит впервые описали пять пациентов со сходной клинической картиной. Она включала увеличение лимфоузлов, селезёнки и аутоиммунное поражение клеток крови, что внешне напоминало лимфоидную опухоль, однако патоморфологическое исследование эту гипотезу опровергло. В последующие годы в научной литературе периодически появлялись описания аналогичных случаев. Значительный вклад в понимание болезни внесла работа 1992 года, авторы которой не только описали двух пациентов с прогрессирующим лимфопролиферативным синдромом, но и обнаружили ключевую иммунологическую аномалию. У больных было выявлено значительное увеличение особой популяции Т-лимфоцитов, которые экспрессировали Т-клеточный рецептор, но при этом не имели на своей поверхности маркеров CD4 и CD8. Эта популяция получила название «двойные негативные Т-клетки»[3].
Вскоре генетическая природа синдрома у человека была подтверждена, и было установлено, что он связан с мутациями в гене FAS. Дальнейшие исследования показали, что АЛПС может быть результатом мутаций не только в гене FAS, но и в генах других белков, участвующих в механизме апоптоза. Хронология открытия этих генов такова: первым в 1983 году был картирован ген NRAS, за ним последовал ген CTLA4 в 1988-м. Гены FASLG и PRKCD были идентифицированы в 1994 году, CASP10 — в 1996-м, а CASP8 — в 1998 году[2][3].
Классификация
Классификация АЛПС, предложенная в 1999 году, основана на типе молекулярно-генетического дефекта и включает следующие типы[4]:
- АЛПС 0 типа: характеризуется полным дефицитом белка CD95 (FAS-рецептора) вследствие гомозиготной нуль-мутации в гене FAS.
- АЛПС I типа: подразделяется на несколько подтипов в зависимости от поражённого гена:
- Ia тип: наиболее распространённая форма, вызванная гетерозиготной мутацией в гене FAS, приводящей к дефекту FAS-рецептора;
- Ib тип: связан с дефектом FAS-лиганда (FASL) из-за гетерозиготной мутации в гене FASLG;
- Ic тип: обусловлен дефектом FAS-лиганда в результате гомозиготной мутации в гене FASLG.
- АЛПС II типа: связан с дефектами внутриклеточных механизмов апоптоза и включает:
- IIa тип: вызван мутацией в гене каспазы-10 (CASP10);
- IIb тип: вызван мутацией в гене каспазы-8 (CASP8).
- АЛПС III типа: диагностируется в случаях, когда клиническая картина соответствует синдрому, но конкретный генетический дефект остаётся неуточнённым.
Согласно классификации первичных иммунодефицитов, утверждённой экспертами Международного союза иммунологических обществ в 2015 году, АЛПС подразделяется на несколько генетических вариантов. К ним относятся формы, обусловленные дефектами в генах TNFRSF6 (кодирующем FAS-рецептор), TNFRSF6 (для FAS-лиганда), CASP10, CASP8, FADD и PRKCD. Отдельно в классификации выделены АЛПС-подобные заболевания, которые рассматриваются как фенокопии первичных иммунодефицитов. Эти состояния клинически напоминают АЛПС, но вызваны соматическими, а не наследственными мутациями, в частности, в генах FAS, KRAS и NRAS[4].
Этиология
АЛПС имеет генетическую этиологию и напрямую связан с мутациями в генах, регулирующих процесс апоптоза. Все эти гены кодируют белки, критически важные для запуска и осуществления апоптоза. Возникающие мутации приводят к нарушению этого механизма, что, в свою очередь, вызывает потерю контроля над размножением лимфоцитов. Результатом является патологическое накопление активированных лимфоцитов в лимфоидных органах[2].
Различные генетические формы АЛПС наследуются по разным механизмам. Для большинства типов заболевания (мутации в генах FAS, FASLG, CASP10 и CTLA4) характерен аутосомно-доминантный тип наследования. В то же время формы, связанные с мутациями генов CASP8 и PRKCD, наследуются по аутосомно-рецессивному типу[2].
Патогенез
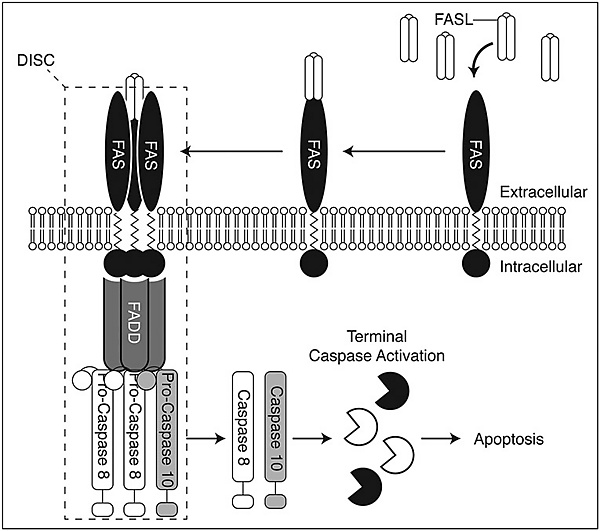
В основе развития АЛПС лежит нарушение механизма апоптоза лимфоцитов, в первую очередь затрагивающее ключевой FAS-опосредованный путь. В норме активация FAS-рецептора на поверхности лимфоцита его лигандом (FASL) запускает внутриклеточный каскад реакций. Этот сигнал передаётся через внутриклеточный «домен смерти» на адапторный белок FADD, который, в свою очередь, активирует каспазы-8 и -10 (инициаторные каспазы). Активированные каспазы запускают протеолитический каскад, приводящий к необратимому апоптозу клетки, что является основным механизмом контроля за числом прошедших активацию лимфоцитов и поддержания иммунологической толерантности. Мутации в любом из генов, кодирующих белки этого пути, нарушают передачу сигнала, блокируя апоптоз. Это приводит к двум ключевым последствиям: неконтролируемому накоплению активированных лимфоцитов и экспансии особой популяции — так называемых двойных негативных Т-клеток (DNT-клеток), имеющих фенотип TCRα/β+CD3+CD4-CD8-[4].
Именно инфильтрация органов и тканей, особенно селезёнки, этими DNT-клетками напрямую повреждает их архитектонику и нарушает функцию. Например, в селезёнке это вызывает дезорганизацию маргинальной зоны, сокращение пула В-клеток и недостаточную выработку антител. Параллельно дефект апоптоза В-лимфоцитов способствует выживанию аутореактивных В-клеток, что ведёт к гипергаммаглобулинемии и производству аутоантител[4].
Эпидемиология
Точная распространённость АЛПС не установлена. В исследовании с анализом более 208 миллионов пациентов было выявлено 2288 пациентов с АЛПС, средний возраст которых составил 48 лет. Среди них преобладали женщины, в то время как доля мужчин составила 40,5 %. Все пять основных расовых групп были представлены в выборке, при этом примерно 77 % пациентов принадлежали к белой расе[5].
Диагностика
Клиническая картина АЛПС характеризуется значительным разнообразием. Возраст начала заболевания вариабелен, но при наиболее распространённой форме с герминогенной мутацией гена FAS манифестация чаще всего происходит в возрасте 3—5 лет, хотя описаны случаи и более позднего дебюта — между 18 и 35 годами[4].
Наиболее типичными и часто первыми проявлениями болезни являются стойкое увеличение лимфатических узлов (лимфаденопатия) и селезёнки (спленомегалия), которые отмечаются более чем у половины пациентов. Гепатомегалия наблюдается у свыше 50 % больных. Важной особенностью является то, что лимфопролиферативные проявления с возрастом имеют тенденцию к уменьшению и после 20 лет значительно ослабевают у большинства пациентов[4].
Аутоиммунные нарушения являются второй ключевой составляющей клинической картины, возникая у большинства пациентов в молодом возрасте (до 30 лет). Наиболее частыми из них являются аутоиммунные цитопении, такие как аутоиммунная гемолитическая анемия и иммунная тромбоцитопения. Рецидивирующие инфекции — достаточно частое явление при АЛПС, в то время как лихорадка неясного генеза встречается редко[4].
Помимо характерной лимфопролиферации и аутоиммунных цитопений, АЛПС может затрагивать практически любые органы и системы. Со стороны нервной системы поражения могут проявляться в виде аутоиммунной мозжечковой атаксии, синдрома Гийена — Барре, поперечного миелита и эпилептического синдрома. Часто встречаются поражения желудочно-кишечного тракта, такие как аутоиммунные эзофагиты, гастриты, колиты и панкреатиты, а также поражения печени, включающие аутоиммунный гепатит и первичный билиарный цирроз[3].
Кожные проявления обычно развиваются по типу рецидивирующей крапивницы, геморрагического васкулита или панникулита. Со стороны дыхательной системы патология может протекать в форме облитерирующего бронхоальвеолита или лёгочных инфильтратов, которые, как правило, не приводят к выраженной дыхательной недостаточности. Кроме того, в ряде случаев АЛПС сочетается с поражениями почек с развитием к аутоиммунного гломерулонефрита и нефротического синдрома[3].
Отдельные генетические варианты АЛПС имеют свои клинические особенности. Например, для дефицита каспазы-8 характерна гипогаммаглобулинемия. Дефицит FADD может проявляться сочетанием рецидивирующих инфекций с энцефалопатией, дисфункцией печени и пороками сердца. Дефицит PKCD, в свою очередь, часто сопровождается тяжёлыми аутоиммунными поражениями, такими как гломерулонефрит с нефротическим синдромом, полихондрит и антифосфолипидный синдром, а также склонностью к инфекциям, вызванным герпесвирусами[4].
Иммуноферментный анализ: характерно поликлональное повышение концентрации IgG, IgA в сыворотке крови и присутствие аутоантител, направленных против клеток крови. Также возможно повышение концентрации интерлейкина 10 и 18[3].
Проточная цитометрия: при анализе популяции Т-клеток, экспрессирующих CD45 и CD3, выявляется отчётливая субпопуляция, лишённая маркеров CD4 и CD8, что соответствует патологическим двойным негативным Т-клеткам[6].
Биопсия лимфатического узла с гистологическим исследованием: наиболее яркими изменениями являются фолликулярная гиперплазия и выраженное расширение паракортикальной зоны за счёт скопления мелких пролиферирующих лимфоцитов, иммунобластов и плазматических клеток. В паракортикальных зонах часто обнаруживаются митотические фигуры, что отражает активное размножение этих клеток. Важным диагностическим признаком служит сохранение общей архитектоники лимфатического узла, что позволяет дифференцировать это состояние от Т-клеточной лимфомы. Помимо этого, в лимфоузлах может наблюдаться значительное расширение синусов, заполненных гистиоцитами, которые не имеют признаков клеток Лангерганса и проявляют явления эмпериполеза — фагоцитоза лимфоцитов[6].
При иммуногистохимическом исследовании гистологического материала выявляется увеличение количества двойных негативных Т-клеток в паракортикальной зоне, которые экспрессируют CD3, но не несут маркеров CD4 и CD8. Эти двойные негативные Т-клетки демонстрируют позитивность к HLA-DR, что указывает на их предшествующую активацию, однако при этом они часто экспрессируют CD45RA — маркер наивных Т-лимфоцитов. При АЛПС не наблюдается потери пан-Т-клеточных антигенов, таких как CD2, CD5 и CD7. Окрашивание на Ki67 показывает повышенный индекс пролиферации в паракортикальных зонах[6].
Биопсия костного мозга с гистологическим исследованием: костный мозг при данном заболевании, как правило, имеет нормальную клеточность, хотя в литературе описаны случаи как гиперклеточного, так и гипоклеточного костного мозга. Наиболее часто регистрируемым признаком является лимфоцитоз, который в почти половине случаев может сопровождаться слабо выраженной эозинофильной гиперплазией. Важно отметить, что диспластические изменения и явления гемофагоцитоза при этом отсутствуют[5].
Для установления диагноза АЛПС используют критерии, разработанные Европейским обществом иммунодефицитов (англ. European Society for Immunodeficiencies, ESID). Для постановки диагноза АЛПС требуется наличие как минимум одного большого и одного малого критерия[4].
- Большие критерии (необходим хотя бы один):
- спленомегалия;
- лимфаденопатия (увеличение трёх и более лимфатических узлов в течение более трёх месяцев при отсутствии инфекции или злокачественного новообразования);
- аутоиммунная цитопения (поражение двух и более клеточных линий крови);
- наличие лимфомы в анамнезе;
- положительный семейный анамнез (наличие АЛПС у близких родственников).
- Малые критерии (необходим хотя бы один):
- повышенное количество двойных негативных Т-клеток (с фенотипом TCRα/β+CD3+CD4-CD8-), составляющих более 6 % от общего числа CD3+ T-лимфоцитов;
- повышенная концентрация не менее двух из перечисленных биомаркеров:
- растворимый FAS-лиганд (sFASL) > 200 пг/мл;
- витамин B12 > 1500 нг/л;
- интерлейкин-10 > 20 пг/мл;
- нарушение FAS-опосредованного апоптоза in vitro.
Дифференциальная диагностика
Дифференциальная диагностика АЛПС проводится со следующими заболеваниями:
- инфекционные заболевания (например, вирус Эпштейна — Барр);
- злокачественные лимфопролиферативные заболевания (в особенности Т-клеточная лимфома);
- лизосомные болезни накопления;
- саркоидоз;
- системные заболевания соединительной ткани с лимфаденопатией;
- гемофагоцитарный лимфогистиоцитоз;
- синдром Эванса;
- синдром серых тромбоцитов;
- общий вариабельный иммунодефицит;
- Х-сцепленный лимфопролиферативный синдром;
- синдром Вискотта — Олдрича;
- синдром Гипер-IgM;
- дефект CTLA4;
- дефект PI3K;
- RAS-ассоциированное аутоиммунное лейкопролиферативное заболевание;
- аутоиммунная цитопения (идиопатическая иммунная тромбоцитопения, аутоиммунная гемолитическая анемия, аутоиммунная нейтропения).
Лечение
Лечение АЛПС требуется до 50 % пациентов, преимущественно для контроля аутоиммунных проявлений. Главной целью терапии является купирование угрожающих жизни цитопений. В острой ситуации обычно эффективна краткосрочная терапия кортикостероидами в высоких дозах. Для долгосрочного контроля и минимизации побочных эффектов от длительного приёма стероидов пациентов переводят на альтернативную иммуносупрессию. С этой целью успешно применяется микофенолата мофетил, который улучшает исходы у пациентов с АЛПС. Ритуксимаб также может быть эффективен, однако его следует по возможности избегать из-за уникального для пациентов с АЛПС риска развития пролонгированной гипогаммаглобулинемии. При необходимости к терапии как стероидами, так и другими иммуносупрессантами можно добавлять внутривенный иммуноглобулин. Для коррекции изолированной нейтропении может использоваться рекомбинантный гранулоцитарный колониестимулирующий фактор[6].
Спленэктомию рекомендуется избегать, так как она ассоциирована со значительным ухудшением прогноза для пациентов с АЛПС, в отличие от других рефрактерных аутоиммунных цитопений. Медикаментозная терапия цитопений обычно успешно устраняет проявления гиперспленизма. Если же спленэктомия становится необходимой из-за неконтролируемого гиперспленизма, резистентного к лечению, таким пациентам показана длительная антибиотикопрофилактика и вакцинация[6].
Исследования показывают, что ингибитор mTOR сиролимус имеет эффективность в лечении рефрактерных цитопений, связанных с АЛПС. Единственным известным методом радикального излечения АЛПС остаётся трансплантация гемопоэтических стволовых клеток, которая проводится только в тяжёлых случаях, не поддающихся стандартной иммуносупрессивной терапии[6].
Прогноз
Основными причинами летального исхода при АЛПС являются развитие лимфом и сепсис, связанный с перенесённой спленэктомией. При этом общая летальность считается относительно невысокой: около 85 % пациентов доживают до 50 лет по сравнению с 93—95 % в здоровой популяции. Главным онкологическим риском является значительное — в десятки и даже сотни раз — повышение вероятности развития лимфом, которые в среднем манифестируют в возрасте 18—28 лет. Несмотря на этот риск, многие пациенты с АЛПС, особенно с мутациями в гене FAS, с возрастом отмечают уменьшение лимфаденопатии, спленомегалии и аутоиммунных проявлений. При длительном лечении и контроле заболевания возможна стабилизация состояния с полным или частичным исчезновением симптомов. Прогноз может варьироваться в зависимости от типа генетической мутации. Пациенты с мутациями во внутриклеточном домене белка FAS имеют более тяжёлый прогноз, в то время как мутации в его внеклеточном домене часто ассоциированы с более мягким течением болезни[4][6].
Примечания
Литература
- Гамисония А. М. Аутоиммунный лимфопролиферативный синдром (рус.). Генокарта — генетическая энциклопедия (9 ноября 2020). Дата обращения: 6 октября 2025.
- Paskiewicz A., Niu J., Chang C. Autoimmune lymphoproliferative syndrome: A disorder of immune dysregulation (англ.) // Autoimmunity Reviews. — 2023. — November (vol. 22, no. 11). — P. 103442. — doi:10.1016/j.autrev.2023.103442.
- Швец О.А., Щербина А.Ю. Аутоиммунный лимфопролиферативный синдром (обзор литературы) // Вопросы гематологии/онкологии и иммунопатологии в педиатрии. — 2016. — Т. 15, № 1. — С. 34—40. — doi:10.24287/1726-1708-2016-15-1-34-40.
- Ковынев И. Б., Поспелова Т. И., Мишенин А. В., Нечунаева И. Н., Тарновский Р. В. Аутоиммунный лимфопролиферативный синдром в гематологической клинике: обзор литературы и собственное наблюдение // Клиническая онкогематология. Фундаментальные исследования и клиническая практика. — 2013. — № 2.